Clear Sky Science · tr
TRPM1’in kriyo‑EM yapısı, ters dönmüş bir transmembran bölgesiyle kanonik olmayan bir mimariyi ortaya koyuyor
Karanlıkta görme
Karanlık bir odada tökezleyen herkes, gece görmeyi mümkün kılan gözdaki hassas moleküllere güvenmiştir. Bunlardan biri olan TRPM1 adlı protein, retinadaki sinir hücrelerinde küçük bir kapı görevi görerek yüklü atomların akmasına izin verdiği ve loş ışıkla ilgili sinyalleri taşıdığı uzun zamandır düşünülen bir adaydır. Yine de bilim insanları TRPM1’in tam olarak nasıl yapılandığını ve gerçekten bağımsız bir iyon kanalı olarak işleyip işlemediğini göstermek için zorluk yaşadı. Bu çalışma, gelişmiş görüntüleme ve hücre deneylerini birleştirerek TRPM1’in sıra dışı yapısını ve muhtemelen gece görüşünü nasıl desteklediğini ortaya koyuyor.
Gece görüş sinyalleri nasıl iletilir
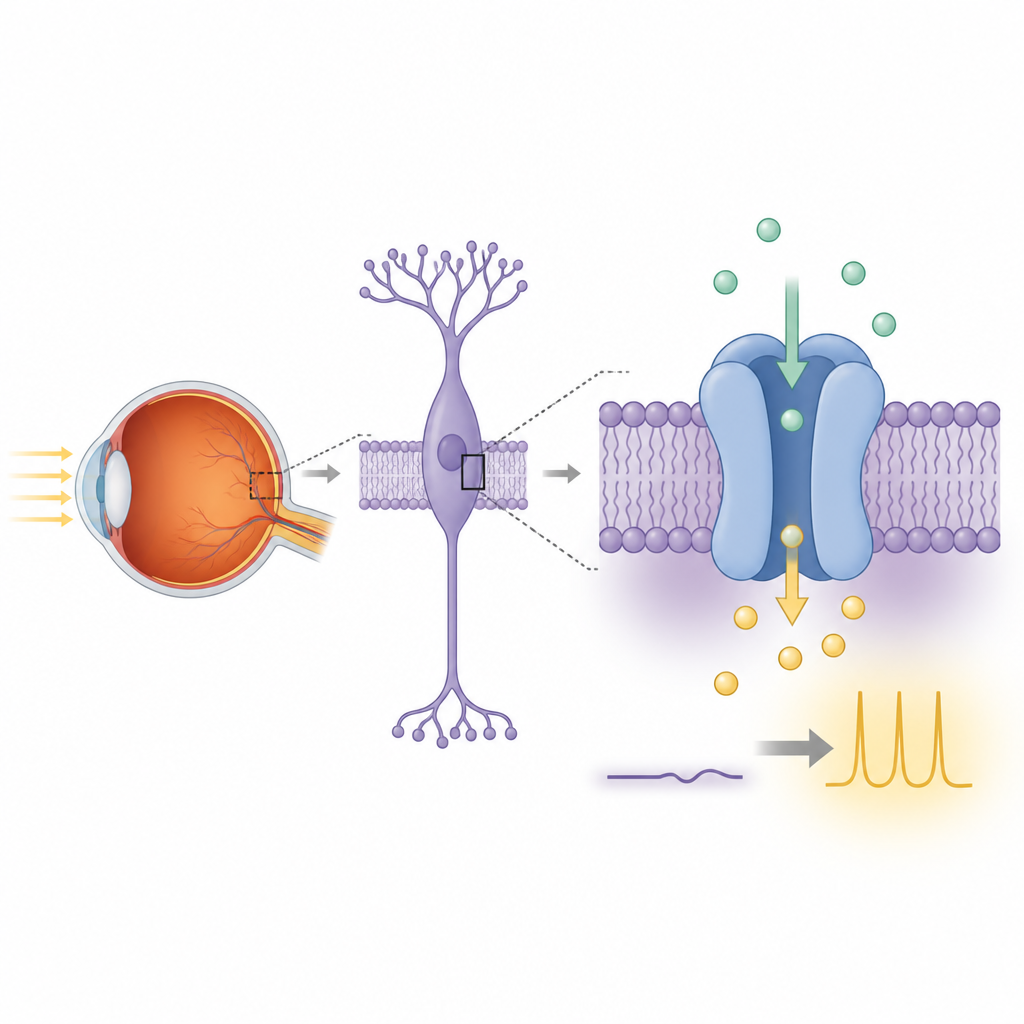
Gece görüşü, retinadaki çubuk fotoreseptörlerin tek fotonları algılayıp bu bilgiyi yakınlardaki bipolar hücrelere iletmesiyle başlar. Bu bipolar hücrelerin içinde, mGluR6 adlı bir glutamat reseptörünü TRPM1’e bağlayan bir sinyal zinciri bulunur. Işıkta, TRPM1 pozitif yüklü iyonların içe doğru sürekli bir akımıyla ilişkilidir ve bu hücrelerin depolarize kalmasını sağlar. Karanlıkta, mGluR6’nın aktivasyonu G‑protein alt birimlerini serbest bırakarak bu akımı kapatır, hücreyi repolarize eder ve sinyali sonlandırır. TRPM1 veya ortaklarından biri genetik mutasyonlarla hasar gördüğünde, bu ışığa bağlı iletişim bozulur ve kişiler tamamen konjenital sabit gece körlüğü geliştirebilir; bu durum, zayıf ışıkta görmenin ciddi şekilde etkilenmesiyle karakterizedir.
TRPM1’in gerçek bir kanal olup olmadığını test etmek
Diğer TRPM aile kanallarına yakın benzerliğine rağmen, TRPM1’in gerçek işlevi yıllardır tartışmalı kaldı çünkü elektriksel aktivitesi standart laboratuvar hücre hatlarında yeniden üretmekte zordur. Yazarlar önce yapısal çalışmalar için uygun, fare kaynaklı bir TRPM1 yapılandırması oluşturdular; katlanma için gerekli olmayan gevşek bir kuyruk bölgesini kestiler. Tam uzunlukta veya kırpılmış TRPM1’i, kalsiyum girişi olduğunda ışıldayan şekilde mühendislik yapılmış insan HEK293 hücrelerinde eksprese ettiler. Hücrelerin dışına kalsiyum eklendiğinde, TRPM1 ifade eden hücrelerin kontrol hücrelerine kıyasla çok daha fazlası ışıldadı ve floresansları çok daha güçlü arttı. Bu gözlemler, TRPM1’in tek başına membranı geçecek bir kalsiyum yolu oluşturabildiğini ve gerçek bir iyon kanalı olduğu fikrini desteklediğini gösteriyor.
Şaşırtıcı bir kanal şekli
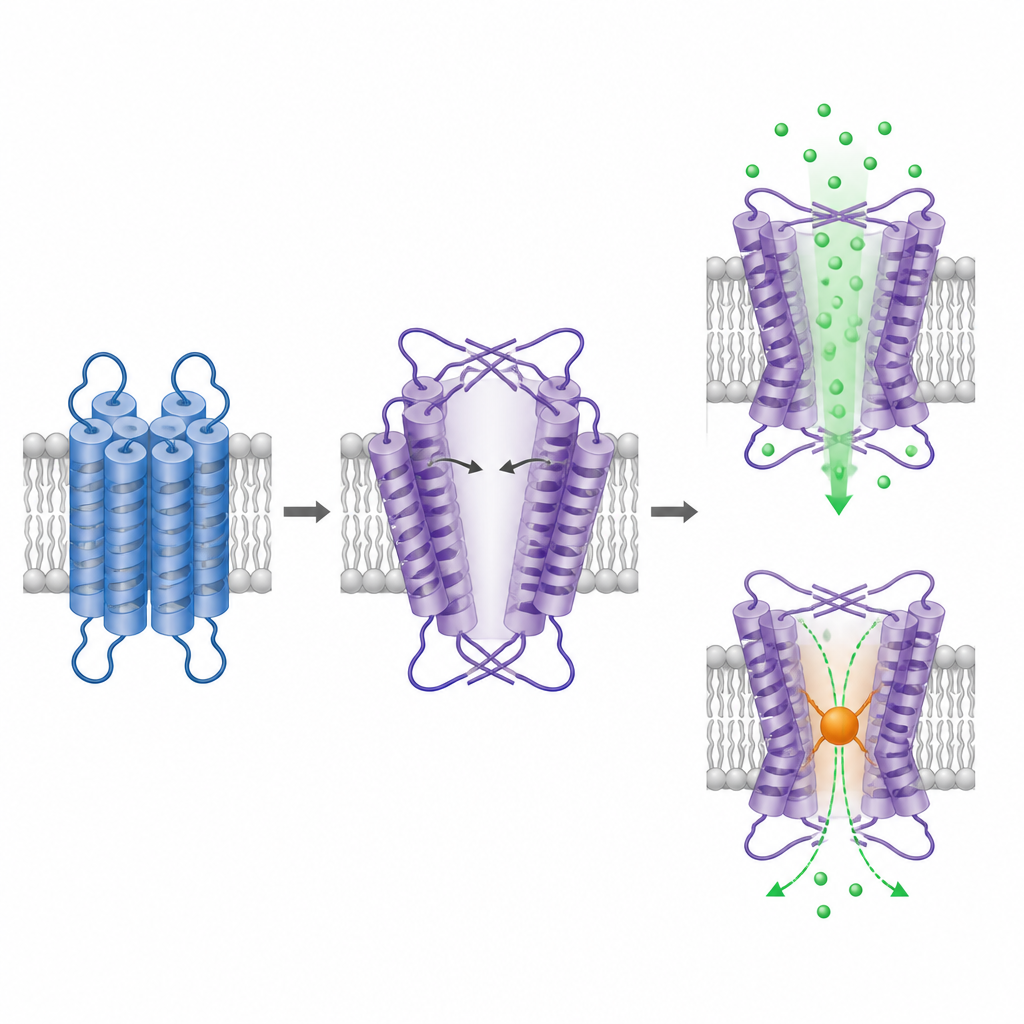
TRPM1’in nasıl yapılandığını görmek için ekip kırpılmış proteini saflaştırdı ve kriyojenik elektron mikroskobisi ile görüntüledi; bu yöntem tek partikülleri ince bir buz tabakası içinde dondurulmuş halde görselleştirir. TRPM1’in hücre içi kısmı, diğer TRPM kanallarına benzer şekilde tanıdık dört katlı simetrik bir düzen oluşturur ve onun tetramerik bir kanal olduğunu pekiştirir. Sürpriz, membranı geçen bölümde yatar. Burada voltaj sensörüne benzer bölge ile gözenek bölgesi hâlâ domain‑swapped (alan değiştirmiş) bir düzen gösteriyor, ancak şimdiye kadar incelenen tüm ilişkili iyon kanallarına kıyasla ters el hakimiyeti taşıyor. Bu ters düzen, iki gözenek heliksinin sığ açılarla bükülüp gerilmesine neden oluyor ve geniş, açık bir gözenek benzeri büyük bir merkezi boşluk oluşturuyor.
İyonların gözenekten izlenmesi
TRPM1’in membran bölgesindeki genişlemiş boşluğun dar noktasında en az yaklaşık bir nanometre çapa sahip olduğu tahmin ediliyor; bu, diğer TRPM kanallarının aktif hallerindeki açıklıklarla karşılaştırılabilir. Bu durum, TRPM1’in genellikle konstitüatif olarak açık olma eğiliminde olduğu önceki önerileri destekliyor. Önerilen gözenek gerçekten kalsiyumu taşıyıp taşımadığını test etmek için araştırmacılar dar noktaya bir sistein yerleştirdiler ve açığa çıkan sisteinlere bağlanıp hacim ekleyen bir kimyasal reaktif uyguladılar. Bu işlem, yalnızca mutant kanalda kalsiyuma bağlı floresansı güçlü biçimde azalttı; bu da bu pozisyonun bloke edilmesinin iyon geçişini engellediğini gösteriyor. Yapı ve bloke etme deneyi bir arada, gözlemlenen boşluğun TRPM1’de işlevsel iyon yolunu oluşturduğunu savunuyor.
İlaç tepkileri ve hastalık için ipuçları
TRPM1, yapısal olarak çeşitli küçük molekül ligandlarıyla karakterize edilmiş TRPM3 ile yakından ilişkili olduğundan, yazarlar iki kanal arasındaki bilinen bağlanma ceplerini karşılaştırdılar. TRPM3’te aktivatörleri ve inhibitörleri bağlayan voltaj sensörüne benzer bölgedeki yerler TRPM1’de iyi korunmuş durumda ve inhibitör primidon gerçekten TRPM1’e bağımlı kalsiyum girişini azalttı. Buna karşılık, sensör ile gözenek arasındaki bir cepte TRPM3’ü aktive eden bir steroid, TRPM1’in ters mimarisi nedeniyle yerleşemedi ve TRPM1 aktivitesini artırmadı. Ekip ayrıca insan gece körlüğü mutasyonlarını yapıya haritaladı; bunların çoğu proteinin katlanmasını stabilize eden veya retinal hücrelerde doğru yere taşınmasını kontrol eden bölgelerde yer alıyor gibi görünüyor.
Gece görüşü için bunun anlamı
Basitçe söylemek gerekirse, bu çalışma TRPM1’in gerçekten bir iyon kanalı olduğunu gösteriyor; ancak membranı geçiren bölümü beklenmedik, ters bir şekilde düzenlenmiş ve buna rağmen iyonların geçmesine izin veren geniş bir gözenek sağlıyor. Bu alışılmadık şekil, TRPM1’in akrabalarından farklı davranmasının ve bazı ilaçlara yanıt verip diğerlerine cevap vermemesinin nedenini açıklayabilir. TRPM1’in üç boyutlu mimarisini kalsiyum taşıma yeteneğiyle bağlayarak çalışma, kalıtsal gece körlüğünü anlamak ve bu özel kanalın en loş ışıkta gözümüzün görmesine nasıl yardımcı olduğunu keşfetmek için yapısal bir temel sunuyor.
Atıf: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
Anahtar kelimeler: TRPM1, iyon kanalı, gece görüşü, retina, kriyo‑EM