Clear Sky Science · es
Estructura por crio‑EM de TRPM1 revela una arquitectura no canónica con un dominio transmembrana invertido
Ver en la oscuridad
Cualquiera que haya tanteado en una habitación a oscuras ha dependido de un conjunto delicado de moléculas en el ojo que hacen posible la visión nocturna. Una de ellas, una proteína llamada TRPM1, se sospechaba desde hace tiempo que actúa como una pequeña puerta en las células nerviosas de la retina, permitiendo el paso de átomos cargados y transmitiendo señales sobre la luz tenue. Sin embargo, los científicos han tenido dificultades para mostrar exactamente cómo se construye TRPM1 y si realmente funciona como un canal iónico autónomo. Este estudio combina imágenes avanzadas y experimentos celulares para revelar la inusual estructura de TRPM1 y cómo probablemente respalda la visión nocturna.
Cómo viajan las señales de la visión nocturna
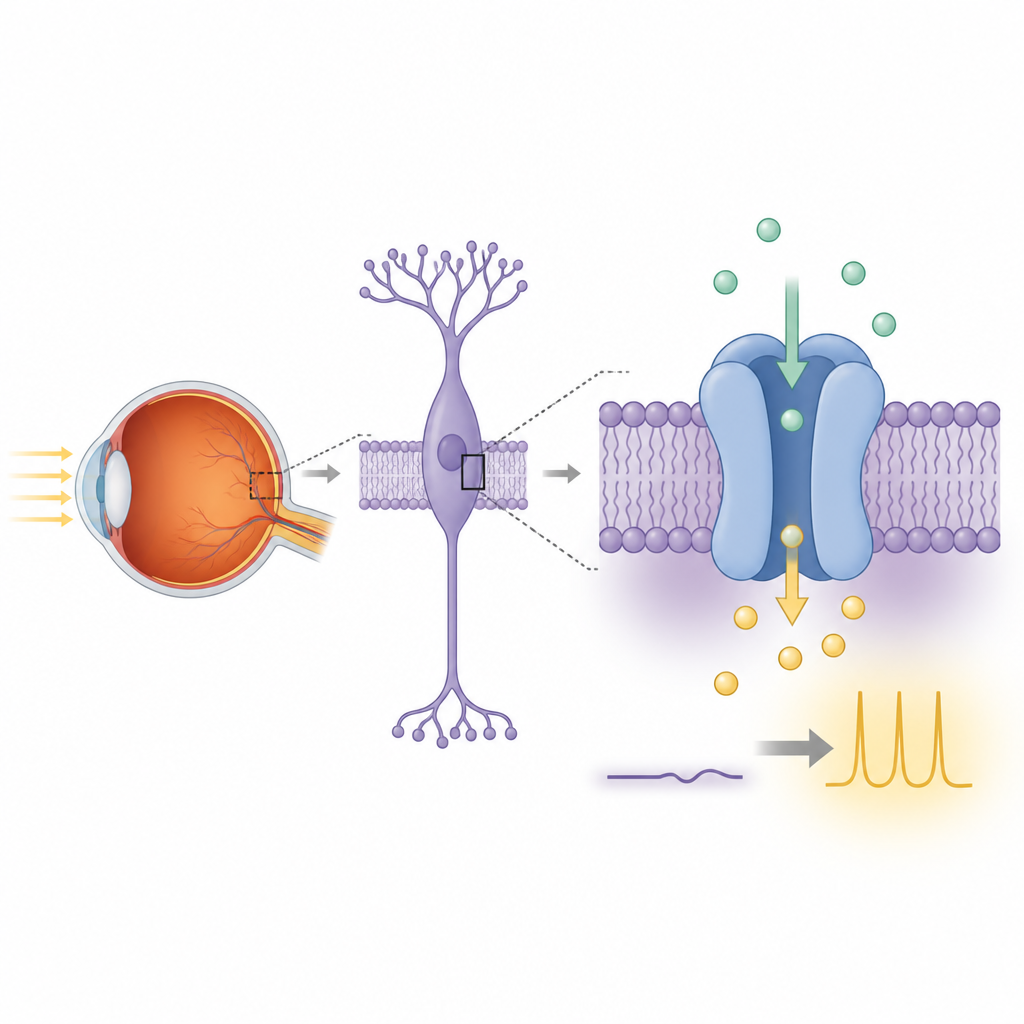
La visión nocturna comienza cuando los fotorreceptores de bastón en la retina detectan fotones individuales y transmiten esa información a las células bipolares cercanas. Dentro de estas células bipolares, una cadena de señalización conecta un receptor de glutamato llamado mGluR6 con TRPM1. Con luz, TRPM1 está asociado a una corriente interna sostenida de iones positivamente cargados que mantiene estas células despolarizadas. En la oscuridad, la activación de mGluR6 libera subunidades de proteína G que cierran esta corriente, repolarizando la célula y terminando la señal. Cuando TRPM1 o sus asociados resultan dañados por mutaciones genéticas, esta comunicación dependiente de la luz falla y las personas pueden desarrollar ceguera nocturna estacionaria congénita completa, una condición en la que la visión con poca luz está gravemente afectada.
Comprobar si TRPM1 es un canal real
A pesar de su gran similitud con otros canales iónicos de la familia TRPM, la función real de TRPM1 ha sido objeto de debate durante años porque su actividad eléctrica es difícil de reproducir en líneas celulares estándar de laboratorio. Los autores primero crearon un constructo de TRPM1 de rata adecuado para trabajo estructural, recortando una región terminal flexible que no es necesaria para el plegamiento. Expresaron TRPM1 de longitud completa o truncado en células HEK293 humanas diseñadas para emitir brillo cuando entra calcio. Al añadir calcio fuera de las células, muchas más células que expresaban TRPM1 se iluminaron en comparación con las de control, y su fluorescencia aumentó con mucha más intensidad. Estas observaciones indican que TRPM1 por sí solo puede crear una vía para que los iones de calcio crucen la membrana, apoyando la idea de que es un canal iónico genuino.
Una forma de canal sorprendente
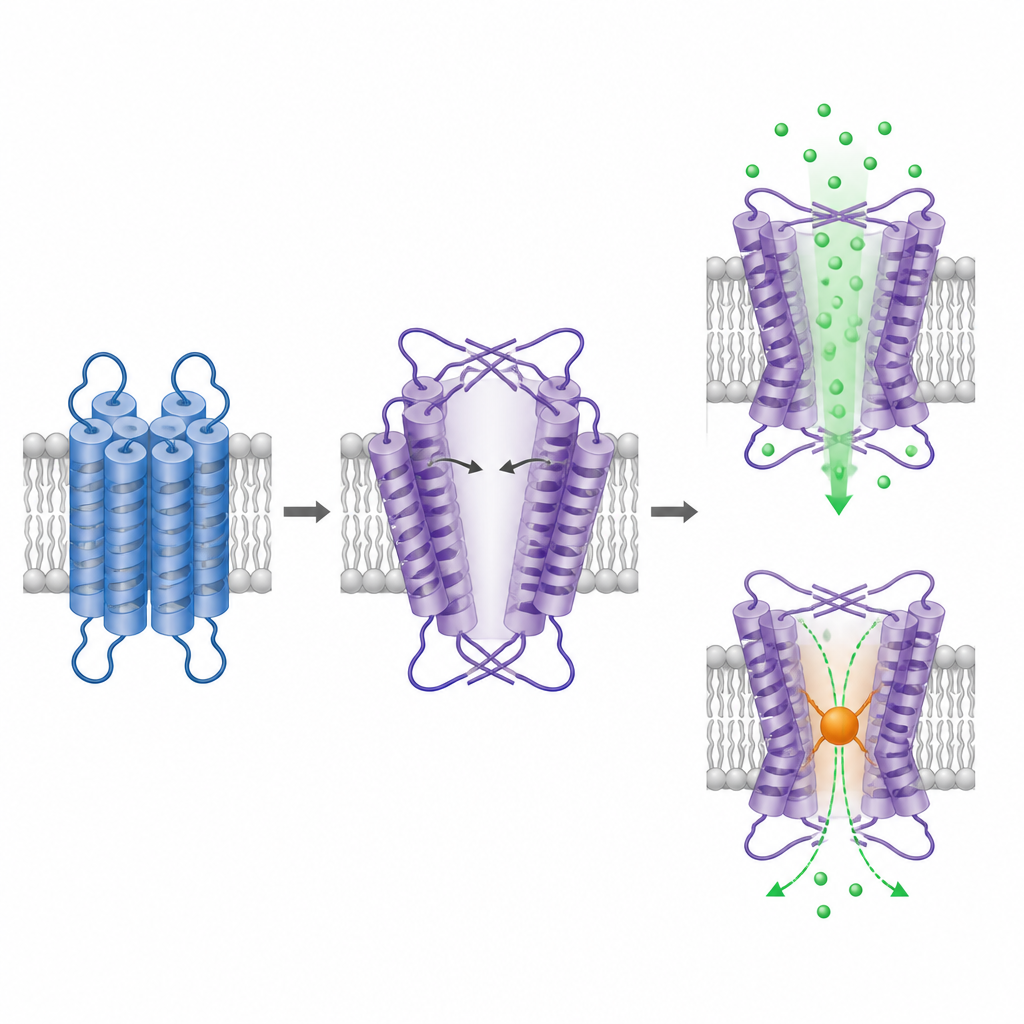
Para ver cómo está construido TRPM1, el equipo purificó la proteína truncada y la obtuvo por microscopía electrónica criogénica, una técnica que visualiza partículas individuales congeladas en una fina capa de hielo. La porción intracelular de TRPM1 forma una disposición simétrica de cuatro subunidades familiar, similar a otros canales TRPM, lo que refuerza su identidad como un canal tetramérico. La sorpresa está en la parte que atraviesa la membrana. Aquí, la región semejante a un sensor de voltaje y la región del poro todavía están organizadas de forma intercambiada entre dominios, pero con una quiralidad opuesta en comparación con todos los canales iónicos relacionados estudiados hasta ahora. Esta disposición invertida obliga a dos de las hélices del poro a doblarse y estirarse en ángulos poco pronunciados, creando una gran cavidad central que se asemeja a un poro amplio y abierto.
Seguir a los iones a través del poro
La cavidad ampliada en el dominio de membrana de TRPM1 se estima en al menos aproximadamente un nanómetro de diámetro en su punto más estrecho, comparable a las aberturas de otros canales TRPM en su estado activo. Esto respalda sugerencias previas de que TRPM1 tiende a estar constitutivamente abierto. Para probar si el supuesto poro realmente transporta calcio, los investigadores introdujeron una cisteína en el punto más estrecho y aplicaron un reactivo químico que se une a cisteínas expuestas y añade volumen. Este tratamiento redujo fuertemente la fluorescencia dependiente de calcio solo en el canal mutante, lo que indica que bloquear esta posición interfiere con la permeación iónica. En conjunto, la estructura y el experimento de bloqueo apoyan que la cavidad observada es la vía iónica funcional en TRPM1.
Pistas sobre respuestas a fármacos y enfermedad
Como TRPM1 está estrechamente relacionado con TRPM3, que ha sido caracterizado estructuralmente con varios ligandos de pequeña molécula, los autores compararon los bolsillos de unión conocidos entre los dos canales. Los sitios en la región semejante a sensor de voltaje que unen activadores e inhibidores en TRPM3 están bien conservados en TRPM1, y el inhibidor primidona sí atenuó la entrada de calcio dependiente de TRPM1. En contraste, un esteroide que activa TRPM3 en un bolsillo entre el sensor y el poro no pudo alojarse en la arquitectura invertida de TRPM1 y no aumentó la actividad de TRPM1. El equipo también mapeó mutaciones humanas vinculadas a la ceguera nocturna sobre la estructura; la mayoría se sitúan en regiones que parecen estabilizar el plegamiento de la proteína o controlar su tráfico hacia el lugar correcto en las células de la retina.
Qué significa esto para la visión nocturna
En términos sencillos, este trabajo demuestra que TRPM1 es realmente un canal iónico, pero con una región que atraviesa la membrana dispuesta de manera inesperada e invertida que aun así permite un poro grande por el que pasan iones. Esta forma inusual puede explicar por qué TRPM1 se comporta de manera diferente a sus parientes y responde a algunos fármacos pero no a otros. Al vincular la arquitectura tridimensional de TRPM1 con su capacidad para transportar calcio, el estudio ofrece una base estructural para comprender la ceguera nocturna hereditaria y para explorar cómo este canal especial ayuda a nuestros ojos a ver con la luz más tenue.
Cita: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
Palabras clave: TRPM1, canal iónico, visión nocturna, retina, crio‑EM