Clear Sky Science · it
Struttura in Cryo-EM di TRPM1 rivela un’architettura non canonica con un dominio transmembrana invertito
Vedere al buio
Chiunque si sia mosso a tentoni in una stanza buia ha fatto affidamento su un insieme delicato di molecole nell’occhio che rendono possibile la visione notturna. Una di queste, una proteina chiamata TRPM1, è da tempo ritenuta fungere da piccolo cancello nelle cellule nervose della retina, lasciando passare atomi carichi e trasmettendo segnali relativi alla luce fioca. Tuttavia gli scienziati hanno faticato a mostrare esattamente come sia costruita TRPM1 e se funzioni davvero come un canale ionico autonomo. Questo studio combina tecniche avanzate di imaging ed esperimenti cellulari per rivelare la struttura insolita di TRPM1 e come essa probabilmente supporti la visione notturna.
Come viaggiano i segnali della visione notturna
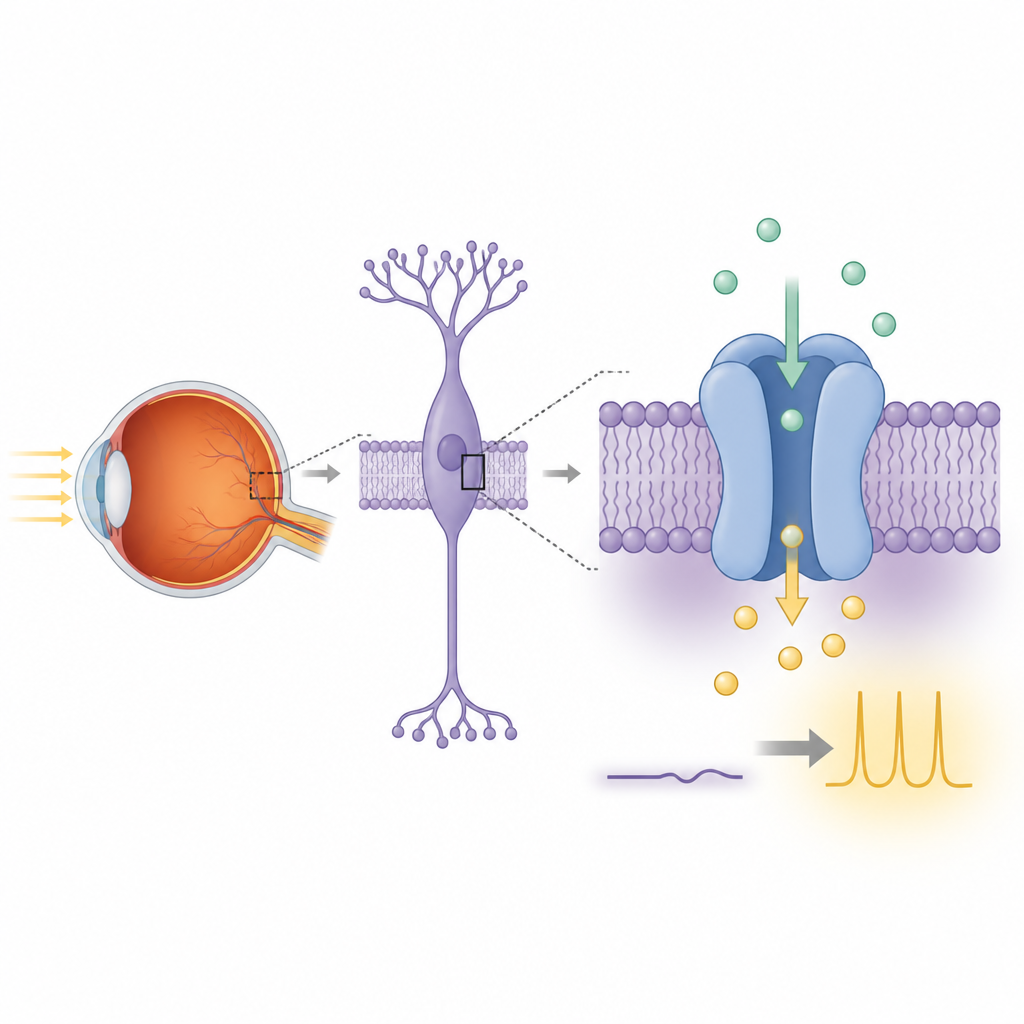
La visione notturna inizia quando i fotorecettori a bastoncelli della retina rilevano singoli fotoni e trasmettono l’informazione alle cellule bipolari vicine. All’interno di queste cellule bipolari, una catena di segnalazione collega un recettore del glutammato chiamato mGluR6 a TRPM1. Alla luce, TRPM1 è associato a una corrente costante entrante di ioni positivi che mantiene queste cellule depolarizzate. Nel buio, l’attivazione di mGluR6 libera subunità di proteine G che spengono questa corrente, ripolarizzando la cellula e terminando il segnale. Quando TRPM1 o i suoi partner sono danneggiati da mutazioni genetiche, questa comunicazione indotta dalla luce fallisce e le persone possono sviluppare la cecità notturna stazionaria congenita completa, una condizione in cui la visione in bassa luminosità è gravemente compromessa.
Verificare se TRPM1 è un vero canale
Nonostante la sua stretta somiglianza con altri canali ionici della famiglia TRPM, la funzione reale di TRPM1 è stata discussa per anni perché la sua attività elettrica è difficile da riprodurre nelle linee cellulari standard da laboratorio. Gli autori hanno innanzitutto creato un costrutto di TRPM1 di ratto adatto al lavoro strutturale, accorciando una coda floscia non necessaria per il ripiegamento. Hanno espresso TRPM1 a lunghezza intera o tronco in cellule umane HEK293 ingegnerizzate per illuminarsi quando entra calcio. Quando è stato aggiunto calcio all’esterno delle cellule, molte più cellule che esprimevano TRPM1 si sono illuminate rispetto alle cellule di controllo, e la loro fluorescenza è aumentata molto di più. Queste osservazioni indicano che TRPM1 da solo può creare un percorso perché gli ioni calcio attraversino la membrana, supportando l’idea che sia un autentico canale ionico.
Una forma sorprendente del canale
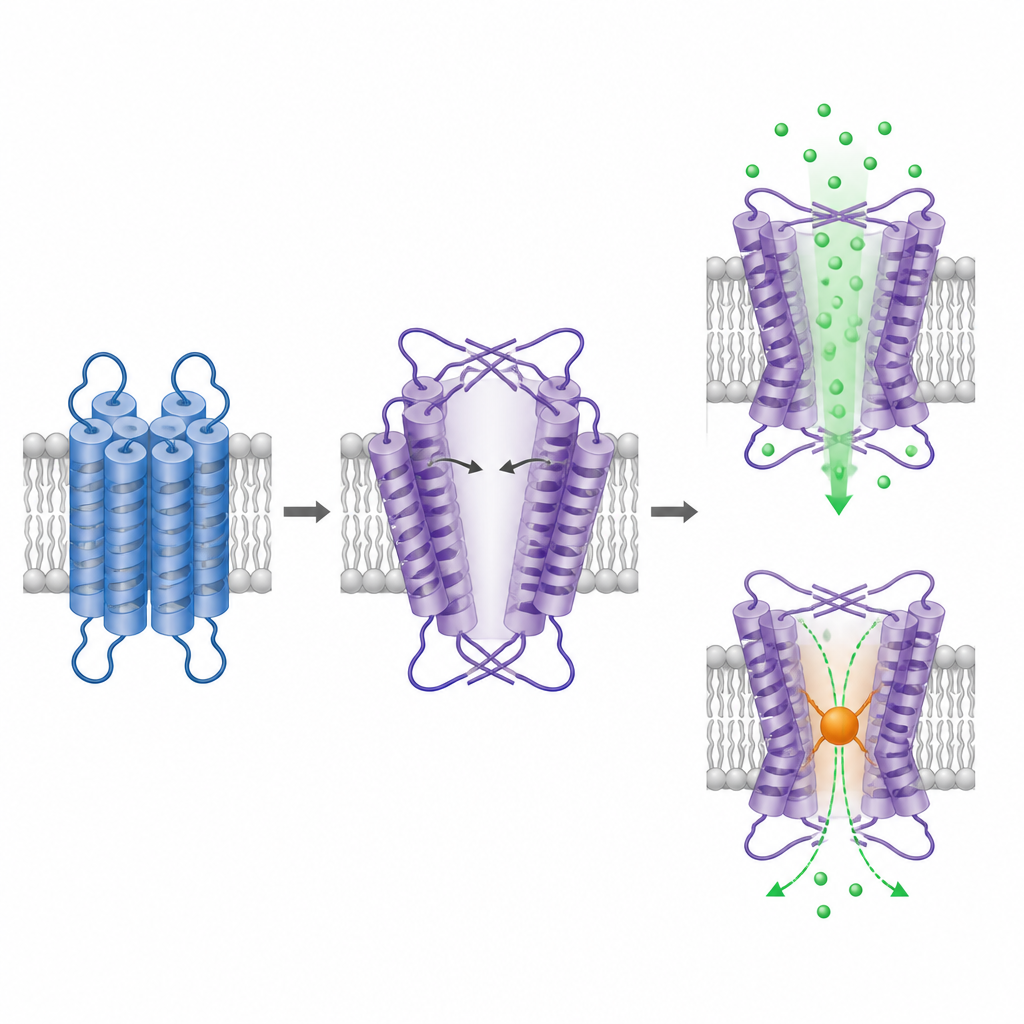
Per vedere come è costruito TRPM1, il gruppo ha purificato la proteina tronca e l’ha immaginata con microscopia crioelettronica, una tecnica che visualizza particelle individuali congelate in uno strato sottile di ghiaccio. La porzione intracellulare di TRPM1 forma un noto arrangiamento a simmetria quadruplicata simile ad altri canali TRPM, rafforzando la sua identità come canale tetramerico. La sorpresa riguarda la parte che attraversa la membrana. Qui, la regione simile a un sensore di voltaggio e la regione del poro sono ancora disposte in modo scambiato tra domini, ma con la mano opposta rispetto a tutti i canali ionici correlati studiati finora. Questo layout invertito costringe due delle eliche del poro a piegarsi ed estendersi con angoli ridotti, creando una grande cavità centrale che somiglia a un poro ampio e aperto.
Seguire gli ioni attraverso il poro
La cavità ingrandita nel dominio transmembrana di TRPM1 è stimata essere almeno di circa un nanometro nel punto più stretto, comparabile alle aperture di altri canali TRPM nel loro stato attivo. Ciò supporta precedenti suggerimenti secondo cui TRPM1 tende a rimanere costitutivamente aperto. Per verificare se il presunto poro conduca davvero il calcio, i ricercatori hanno introdotto una cisteina nel punto più stretto e applicato un reagente chimico che si lega alle cisteine esposte aggiungendo ingombro. Questo trattamento ha ridotto fortemente la fluorescenza dipendente dal calcio solo nel canale mutante, indicando che il blocco in quella posizione interferisce con la permeazione ionica. Insieme, la struttura e l’esperimento di blocco sostengono che la cavità osservata sia il percorso funzionale degli ioni in TRPM1.
Indizi sulle risposte ai farmaci e sulle malattie
Poiché TRPM1 è strettamente correlato a TRPM3, che è stato caratterizzato strutturalmente con vari ligandi di piccole dimensioni, gli autori hanno confrontato le tasche di legame note tra i due canali. I siti nella regione simile al sensore di voltaggio che legano attivatori e inibitori in TRPM3 sono ben conservati in TRPM1, e l’inibitore primidone ha infatti attenuato l’ingresso di calcio dipendente da TRPM1. Al contrario, uno steroide che attiva TRPM3 in una tasca tra sensore e poro non poteva essere alloggiato nell’architettura invertita di TRPM1 e non è riuscito ad aumentare l’attività di TRPM1. Il gruppo ha anche mappato le mutazioni umane associate alla cecità notturna sulla struttura; la maggior parte ricade in regioni che sembrano stabilizzare il ripiegamento della proteina o controllarne il traffico verso la posizione corretta nelle cellule retiniche.
Che cosa significa per la visione notturna
In termini semplici, questo lavoro dimostra che TRPM1 è realmente un canale ionico, ma con una regione transmembrana disposta in modo inaspettato e invertito che comunque permette un ampio poro per il passaggio degli ioni. Questa forma insolita può spiegare perché TRPM1 si comporta diversamente dai suoi parenti e risponde ad alcuni farmaci ma non ad altri. Collegando l’architettura tridimensionale di TRPM1 alla sua capacità di trasportare calcio, lo studio offre una base strutturale per comprendere la cecità notturna ereditaria e per esplorare come questo canale speciale aiuti i nostri occhi a vedere nella luce più fioca.
Citazione: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
Parole chiave: TRPM1, canale ionico, visione notturna, retina, cryo-EM