Clear Sky Science · pt
Estrutura por crio‑EM de TRPM1 revela uma arquitetura não canônica com um domínio transmembrana invertido
Ver no escuro
Qualquer pessoa que já trombou em um quarto escuro dependeu de um conjunto delicado de moléculas no olho que tornam a visão noturna possível. Uma delas, uma proteína chamada TRPM1, há muito tempo é suspeita de funcionar como um pequeno portão em células nervosas da retina, permitindo o fluxo de átomos carregados e transmitindo sinais sobre luz fraca. Ainda assim, os cientistas tiveram dificuldade em mostrar exatamente como o TRPM1 é montado e se ele realmente funciona como um canal iônico independente. Este estudo combina imagens avançadas e experimentos em células para revelar a estrutura incomum do TRPM1 e como ele provavelmente sustenta a visão noturna.
Como os sinais da visão noturna viajam
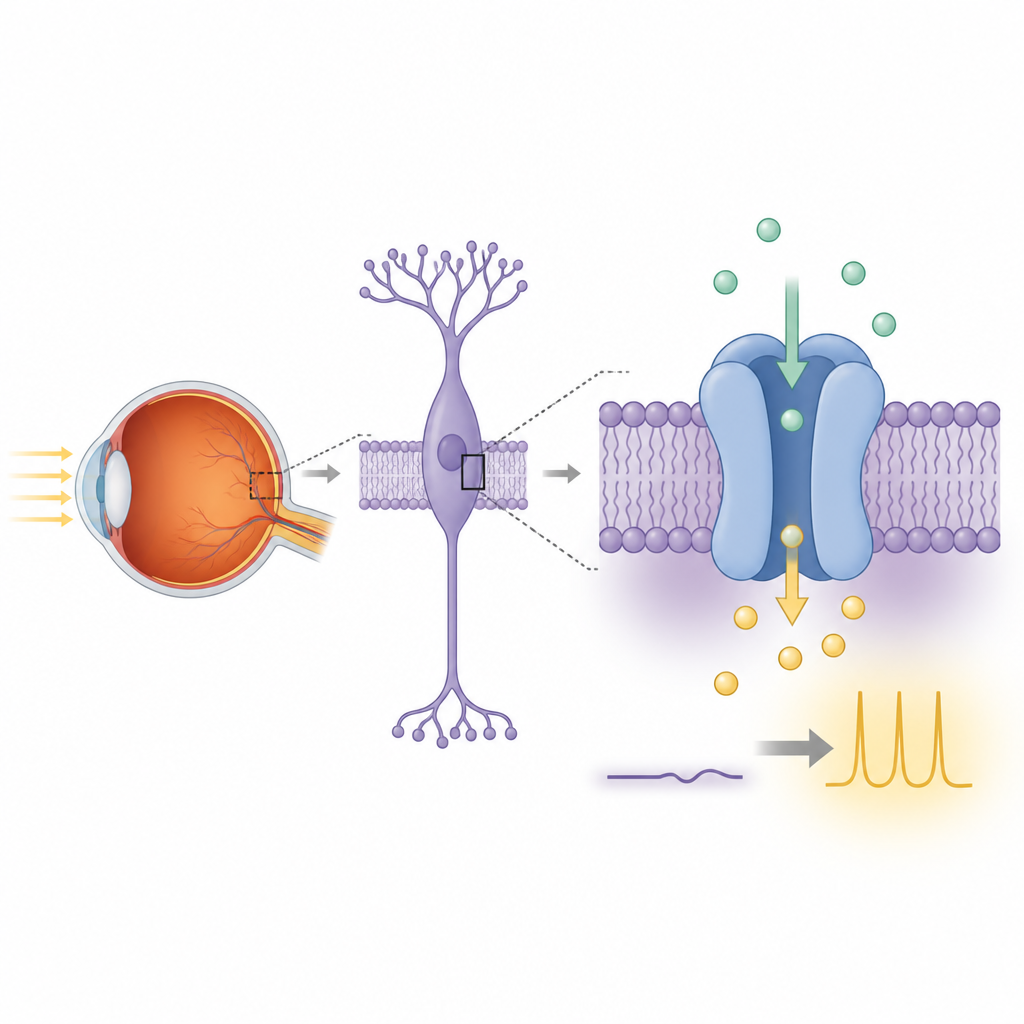
A visão noturna começa quando os fotorreceptores bastonetes da retina detectam fótons individuais e passam essa informação para células bipolares próximas. Dentro dessas células bipolares, uma cadeia de sinalização liga um receptor de glutamato chamado mGluR6 ao TRPM1. Na luz, o TRPM1 está associado a uma corrente interna constante de íons positivamente carregados que mantém essas células despolarizadas. No escuro, a ativação de mGluR6 libera subunidades de proteína G que desligam essa corrente, repolarizando a célula e encerrando o sinal. Quando o TRPM1 ou seus parceiros são danificados por mutações genéticas, essa comunicação mediada pela luz falha e as pessoas podem desenvolver cegueira noturna estacionária congênita completa, uma condição em que ver em baixa luminosidade é severamente prejudicado.
Testando se o TRPM1 é um canal de verdade
Apesar de sua grande semelhança com outros canais iônicos da família TRPM, a função verdadeira do TRPM1 tem sido debatida por anos porque sua atividade elétrica é difícil de reproduzir em linhagens celulares laboratoriais padrão. Os autores primeiro criaram um construto de TRPM1 de rato adequado para trabalho estrutural, aparando uma região terminal flexível que não é necessária para o dobramento. Eles expressaram TRPM1 em versão completa ou truncada em células HEK293 humanas modificadas para fluorescer quando o cálcio entra. Quando cálcio foi adicionado fora das células, muito mais células que expressavam TRPM1 acenderam do que as células controle, e sua fluorescência aumentou muito mais intensamente. Essas observações indicam que o TRPM1 por si só pode criar uma via para íons de cálcio atravessarem a membrana, apoiando a ideia de que ele é um canal iônico genuíno.
Uma forma surpreendente do canal
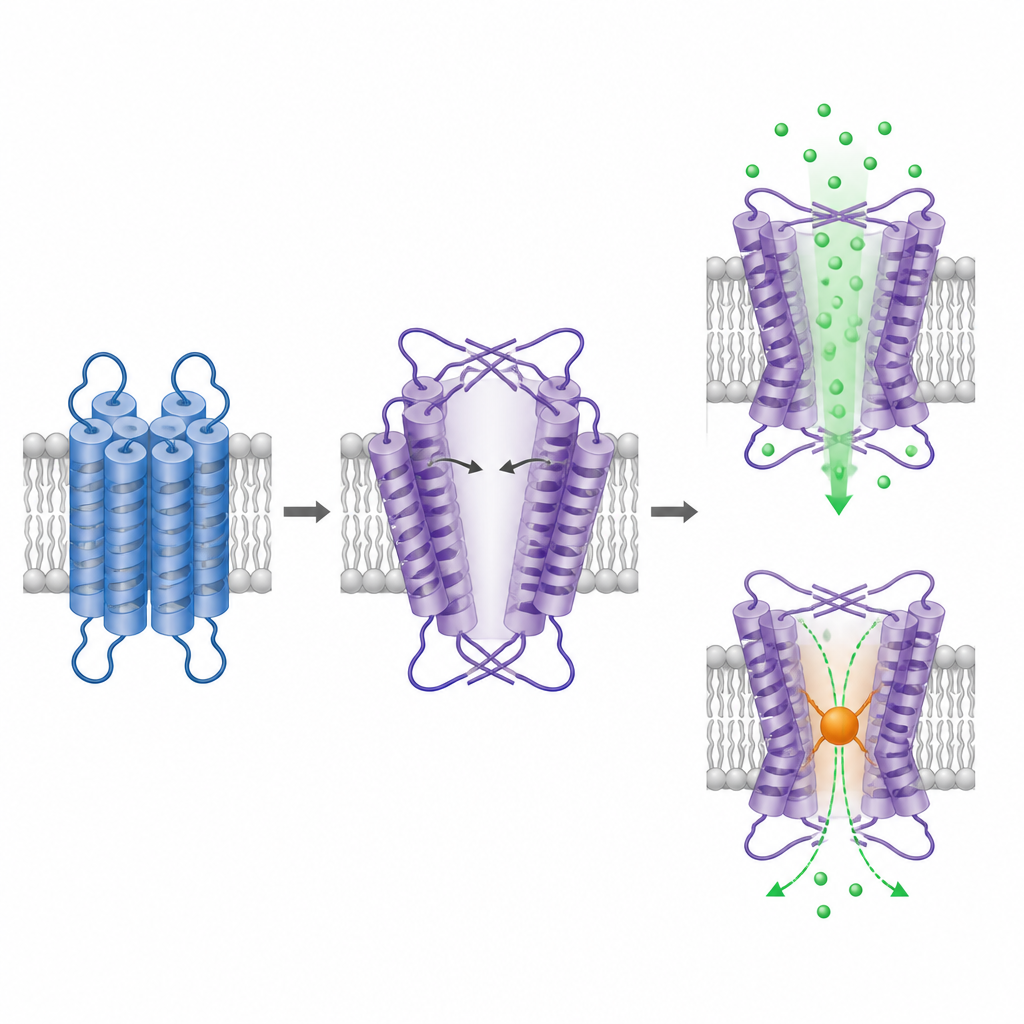
Para ver como o TRPM1 é construído, a equipe purificou a proteína truncada e a imageou com microscopia eletrônica criogênica, uma técnica que visualiza partículas individuais congeladas em uma fina camada de gelo. A porção intracelular do TRPM1 forma um arranjo simétrico em quatro partes familiar, semelhante a outros canais TRPM, reforçando sua identidade como um canal tetramérico. A surpresa está na parte que atravessa a membrana. Aqui, a região semelhante a sensor de voltagem e a região do poro ainda estão dispostas de forma trocada entre domínios, mas com a mão oposta em comparação com todos os canais iônicos relacionados estudados até agora. Esse layout invertido força duas das hélices do poro a dobrar e alongar em ângulos rasos, criando uma grande cavidade central que se assemelha a um poro largo e aberto.
Seguindo íons através do poro
A cavidade ampliada no domínio de membrana do TRPM1 é estimada em pelo menos cerca de um nanômetro na sua parte mais estreita, comparável às aberturas de outros canais TRPM em seu estado ativo. Isso sustenta sugestões anteriores de que o TRPM1 tende a permanecer constitutivamente aberto. Para testar se o putativo poro realmente conduz cálcio, os pesquisadores produziram uma cisteína no ponto mais estreito e aplicaram um reagente químico que se liga a cisteínas expostas e adiciona volume. Esse tratamento reduziu fortemente a fluorescência dependente de cálcio apenas no canal mutante, indicando que bloquear essa posição interfere na permeação iônica. Em conjunto, a estrutura e o experimento de bloqueio argumentam que a cavidade observada é a via iônica funcional no TRPM1.
Pistas sobre respostas a fármacos e doença
Porque o TRPM1 é intimamente relacionado ao TRPM3, que foi caracterizado estruturalmente com vários ligantes de pequena molécula, os autores compararam bolsões de ligação conhecidos entre os dois canais. Sítios na região semelhante a sensor de voltagem que ligam ativadores e inibidores no TRPM3 estão bem conservados no TRPM1, e o inibidor primidona de fato reduziu a entrada de cálcio dependente de TRPM1. Em contraste, um esteroide que ativa o TRPM3 em um bolso entre o sensor e o poro não pôde ser acomodado na arquitetura invertida do TRPM1 e falhou em aumentar a atividade do TRPM1. A equipe também mapeou mutações humanas de cegueira noturna na estrutura; a maioria fica em regiões que parecem estabilizar o dobramento da proteína ou controlar seu tráfego para o local correto nas células da retina.
O que isso significa para a visão noturna
Em termos claros, este trabalho mostra que o TRPM1 realmente é um canal iônico, mas com uma região transmembrana arranjada de maneira inesperada e invertida que ainda permite um poro amplo para a passagem de íons. Essa forma incomum pode explicar por que o TRPM1 se comporta de modo diferente de seus parentes e responde a alguns fármacos, mas não a outros. Ao ligar a arquitetura tridimensional do TRPM1 à sua capacidade de conduzir cálcio, o estudo oferece uma base estrutural para entender a cegueira noturna hereditária e para explorar como esse canal especial ajuda nossos olhos a ver na luz mais fraca.
Citação: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
Palavras-chave: TRPM1, canal iônico, visão noturna, retina, crio‑EM