Clear Sky Science · de
Cryo‑EM-Struktur von TRPM1 zeigt eine unkonventionelle Architektur mit invertierter transmemraner Domäne
Sehen im Dunkeln
Wer schon einmal durch einen dunklen Raum getappt ist, hat sich auf ein filigranes Ensemble von Molekülen im Auge verlassen, das das Sehen bei Dunkelheit ermöglicht. Eines dieser Moleküle, das Protein TRPM1, wurde seit Langem verdächtigt, als winziges Tor in Nervenzellen der Netzhaut zu fungieren, das geladene Atome passieren lässt und Signale über schwaches Licht überträgt. Dennoch fiel es Wissenschaftlern schwer, genau zu zeigen, wie TRPM1 aufgebaut ist und ob es tatsächlich als eigenständiger Ionenkanal arbeitet. Diese Studie kombiniert hochauflösende Bildgebung und Zellversuche, um TRPM1s ungewöhnliche Struktur und wie sie vermutlich das Nachtsehen unterstützt, zu enthüllen.
Wie Signale des Nachtsehens weitergeleitet werden
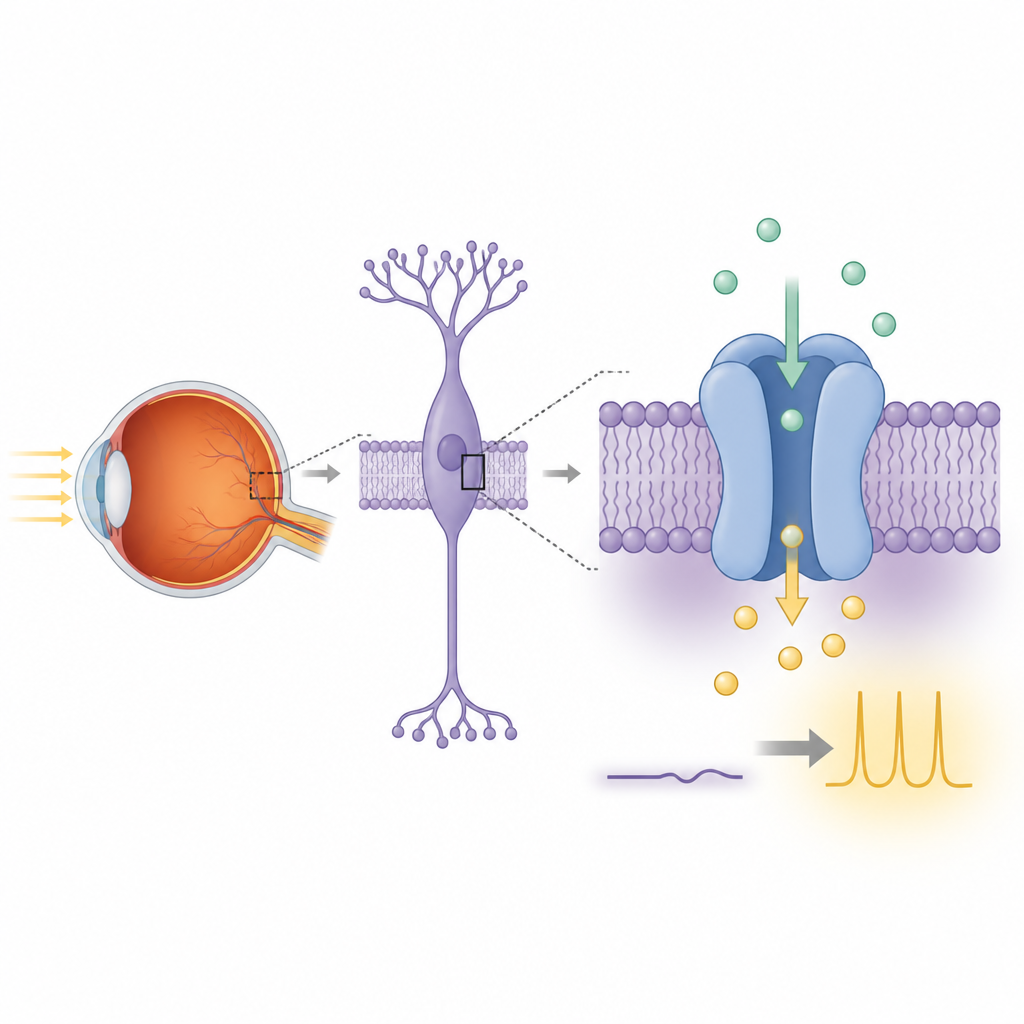
Das Nachtsehen beginnt, wenn Stäbchen in der Netzhaut einzelne Photonen detektieren und diese Information an benachbarte Bipolarzellen weitergeben. In diesen Bipolarzellen verbindet eine Signalkette den Glutamatrezeptor mGluR6 mit TRPM1. Im Licht ist TRPM1 mit einem stetigen Einstrom positiver Ionen verbunden, der diese Zellen depolarisiert hält. In der Dunkelheit führt die Aktivierung von mGluR6 zur Freisetzung von G‑Proteinsubunits, die diesen Strom abschalten, die Zelle repolarisieren und das Signal beenden. Wenn TRPM1 oder seine Partner durch genetische Mutationen geschädigt sind, bricht diese lichtgetriebene Kommunikation zusammen und betroffene Personen können eine komplette kongenitale stationäre Nachtblindheit entwickeln, bei der das Sehen bei schwachem Licht stark beeinträchtigt ist.
Prüfung, ob TRPM1 ein echter Kanal ist
Trotz seiner engen Ähnlichkeit zu anderen TRPM‑Familienkanälen ist die wahre Funktion von TRPM1 seit Jahren umstritten, weil seine elektrische Aktivität in üblichen Zelllinien schwer zu reproduzieren ist. Die Autoren erstellten zuerst ein Ratten‑TRPM1‑Konstrukt für strukturelle Arbeiten, indem sie eine flexible Schwanzregion entfernten, die für das Falten nicht nötig ist. Sie exprimierten entweder das voll‑längige oder das gekürzte TRPM1 in humanen HEK293‑Zellen, die so verändert waren, dass sie bei Calciumeinstrom zu leuchten beginnen. Als Calcium außerhalb der Zellen zugegeben wurde, leuchteten deutlich mehr TRPM1‑exprimierende Zellen auf als Kontrollzellen, und ihre Fluoreszenz stieg deutlich stärker an. Diese Befunde deuten darauf hin, dass TRPM1 alleine einen Weg für Calciumionen durch die Membran schaffen kann und stützen die Vorstellung, dass es sich um einen echten Ionkanal handelt.
Eine überraschende Kanalgestalt
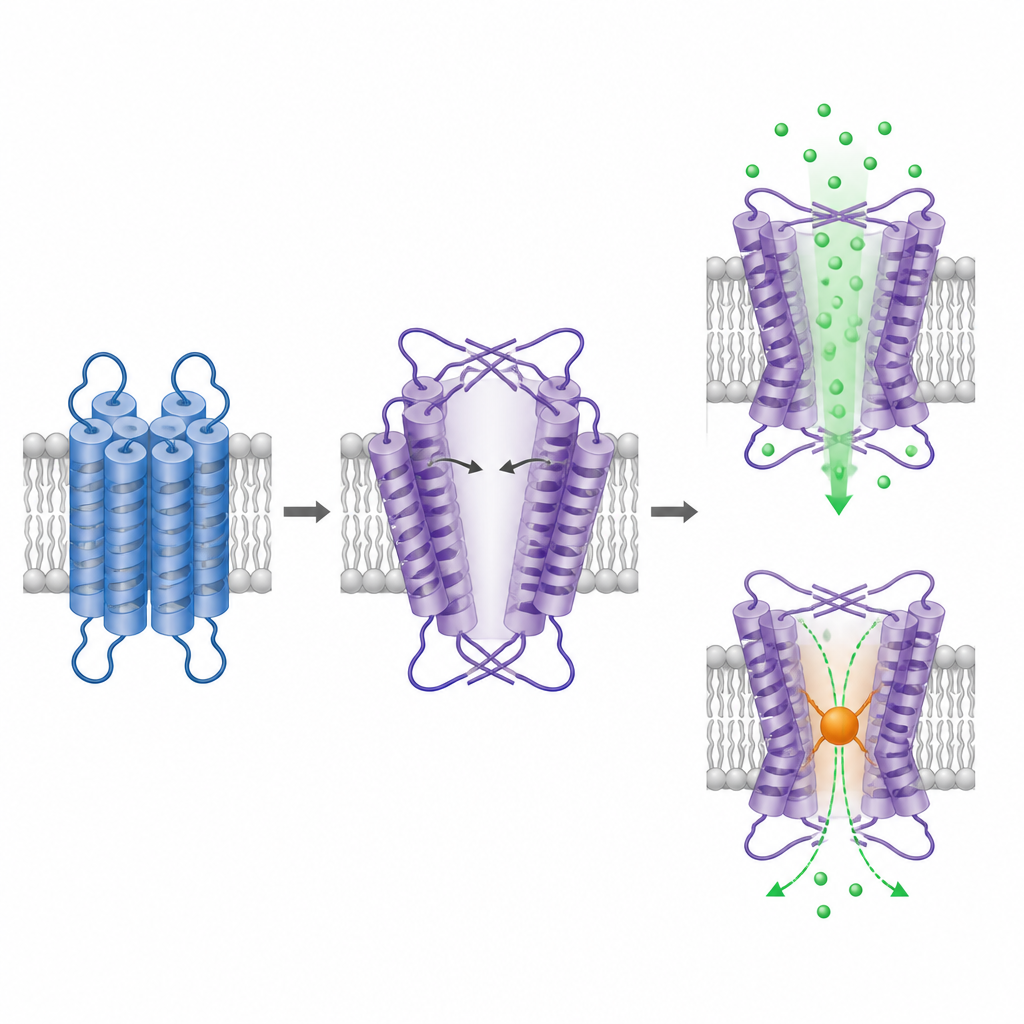
Um zu sehen, wie TRPM1 aufgebaut ist, reinigte das Team das gekürzte Protein und bildete es mittels kryogener Elektronenmikroskopie ab, einer Technik, die einzelne Partikel eingefroren in einer dünnen Eisschicht visualisiert. Der intrazelluläre Anteil von TRPM1 bildet eine vertraute vierfache symmetrische Anordnung, ähnlich wie bei anderen TRPM‑Kanälen, und bestätigt damit seine Identität als tetramerer Kanal. Die Überraschung liegt im membranüberspannenden Teil. Hier sind die spannungssensorähnliche Region und die Porenregion zwar noch domänenvertauscht angeordnet, aber mit entgegengesetzter Händigkeit im Vergleich zu allen bisher untersuchten verwandten Ionkanälen. Diese invertierte Anordnung zwingt zwei der Porenhelices, sich flach zu biegen und zu strecken, wodurch eine große zentrale Kavität entsteht, die einer weiten, offenen Pore ähnelt.
Ionen durch die Pore folgen
Die vergrößerte Kavität in TRPM1s Membrandomäne wird auf mindestens etwa ein Nanometer an ihrer engsten Stelle geschätzt, vergleichbar mit den Öffnungen anderer TRPM‑Kanäle im aktiven Zustand. Das stützt frühere Hinweise darauf, dass TRPM1 tendenziell konstitutiv offen ist. Um zu prüfen, ob die vermutete Pore tatsächlich Calcium leitet, bauten die Forscher eine Cysteinstelle an der engsten Position ein und setzten ein chemisches Reagenz zu, das an exponierte Cysteine bindet und Volumen hinzufügt. Diese Behandlung reduzierte die calciumabhängige Fluoreszenz stark nur im Mutantenkanal, was darauf hinweist, dass das Blockieren dieser Position die Ionenpermeation stört. Zusammengenommen sprechen Struktur und Blockierexperiment dafür, dass die beobachtete Kavität der funktionale Ionenpfad in TRPM1 ist.
Hinweise auf Wirkstoffreaktionen und Erkrankungen
Da TRPM1 eng mit TRPM3 verwandt ist, der bereits strukturell mit verschiedenen kleinen Molekülen charakterisiert wurde, verglichen die Autoren bekannte Bindungstaschen der beiden Kanäle. Stellen in der spannungssensorähnlichen Region, die in TRPM3 Aktivatoren und Inhibitoren binden, sind in TRPM1 gut konserviert, und der Inhibitor Primidon dämpfte tatsächlich TRPM1‑abhängigen Calciumeinstrom. Im Gegensatz dazu konnte ein Steroid, das TRPM3 über eine Tasche zwischen Sensor und Pore aktiviert, in TRPM1s invertierter Architektur nicht untergebracht werden und steigerte TRPM1‑Aktivität nicht. Das Team kartierte außerdem humane Mutationen, die Nachtblindheit verursachen, auf die Struktur; die meisten liegen in Bereichen, die offenbar die Proteinfaltung stabilisieren oder seinen Transport an den richtigen Ort in Netzhautzellen steuern.
Was das für das Nachtsehen bedeutet
Einfach ausgedrückt zeigt diese Arbeit, dass TRPM1 tatsächlich ein Ionkanal ist, dessen membranüberspannender Bereich jedoch unerwartet invertiert angeordnet ist, dabei aber trotzdem eine große Pore für Ionen zulässt. Diese ungewöhnliche Gestalt könnte erklären, warum sich TRPM1 anders verhält als seine Verwandten und auf einige Wirkstoffe reagiert, auf andere jedoch nicht. Indem die dreidimensionale Architektur von TRPM1 mit seiner Fähigkeit, Calcium zu leiten, verknüpft wird, liefert die Studie eine strukturelle Grundlage, um erbliche Nachtblindheit zu verstehen und zu untersuchen, wie dieser spezielle Kanal unseren Augen hilft, im schwächsten Licht zu sehen.
Zitation: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
Schlüsselwörter: TRPM1, Ionkanal, Nachtsehen, Netzhaut, cryo‑EM