Clear Sky Science · pl
Struktura TRPM1 w kriogenicznej EM ujawnia niekanoniczną architekturę z odwróconą domeną błonową
Widzenie w ciemności
Każdy, kto potykał się w ciemnym pokoju, polegał na delikatnym zestawie cząsteczek w oku, które umożliwiają widzenie nocne. Jedna z nich, białko o nazwie TRPM1, od dawna podejrzewana jest o działanie jak maleńska bramka w komórkach nerwowych siatkówki, przepuszczająca naładowane atomy i przenosząca sygnały dotyczące słabego światła. Naukowcom jednak długo nie udawało się dokładnie ustalić, jak zbudowany jest TRPM1 i czy rzeczywiście działa jako samodzielny kanał jonowy. W tej pracy zaawansowane obrazowanie połączono z eksperymentami na komórkach, aby ujawnić niezwykłą strukturę TRPM1 i sposób, w jaki prawdopodobnie wspiera widzenie w ciemności.
Jak przemieszczają się sygnały widzenia nocnego
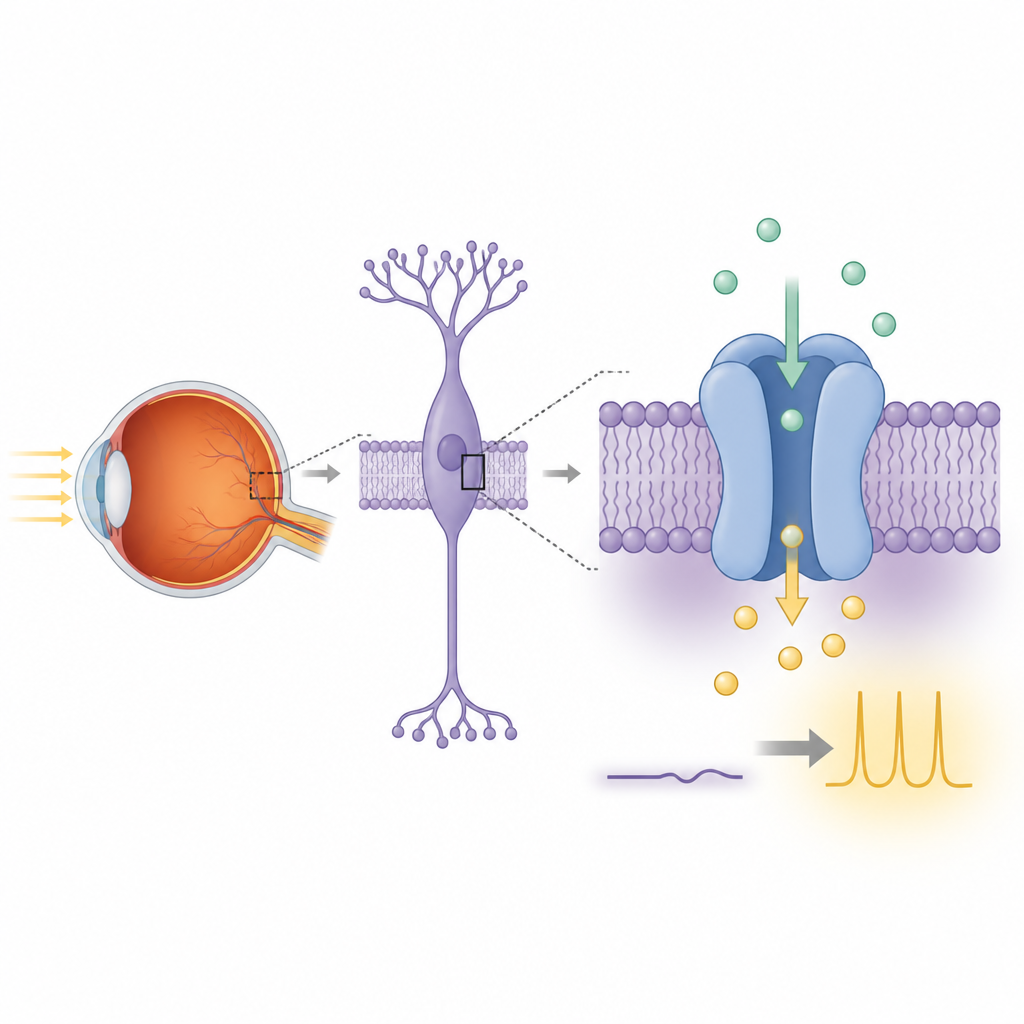
Widzenie nocne zaczyna się, gdy fotoreceptory typu pręcik w siatkówce wykrywają pojedyncze fotony i przekazują te informacje do pobliskich komórek bipolarowych. W tych komórkach łańcuch sygnałowy łączy receptor glutaminianowy o nazwie mGluR6 z TRPM1. W świetle TRPM1 wiąże się z ustalonym prądem dokomórkowym dodatnich jonów, który utrzymuje te komórki w stanie depolaryzacji. W ciemności aktywacja mGluR6 uwalnia podjednostki białka G, które wyłączają ten prąd, ponownie polaryzując komórkę i kończąc sygnał. Gdy TRPM1 lub jego partnerzy są uszkodzeni przez mutacje genetyczne, to świetlno‑napędzana komunikacja zawodzi i może rozwinąć się całkowita wrodzona stacjonarna ślepota nocna, stan, w którym widzenie przy słabym świetle jest poważnie upośledzone.
Sprawdzanie, czy TRPM1 jest prawdziwym kanałem
Mimo bliskiego podobieństwa do innych kanałów z rodziny TRPM, prawdziwa funkcja TRPM1 była przez lata dyskutowana, ponieważ jego aktywność elektryczna jest trudna do odtworzenia w standardowych liniach komórkowych. Autorzy najpierw stworzyli konstrukcję TRPM1 szczura odpowiednią do badań strukturalnych, przycinając wiotki fragment ogona, który nie jest potrzebny do fałdowania. Ekspresowali pełnometrażowy lub obcięty TRPM1 w ludzkich komórkach HEK293 zmodyfikowanych tak, by świecić po wejściu wapnia. Po dodaniu wapnia na zewnątrz komórek znacznie więcej komórek wyrażających TRPM1 zapalało się niż komórek kontrolnych, a ich fluorescencja rosła dużo silniej. Obserwacje te wskazują, że sam TRPM1 może tworzyć ścieżkę dla jonów wapnia przez błonę, wspierając ideę, że jest autentycznym kanałem jonowym.
Zaskakujący kształt kanału
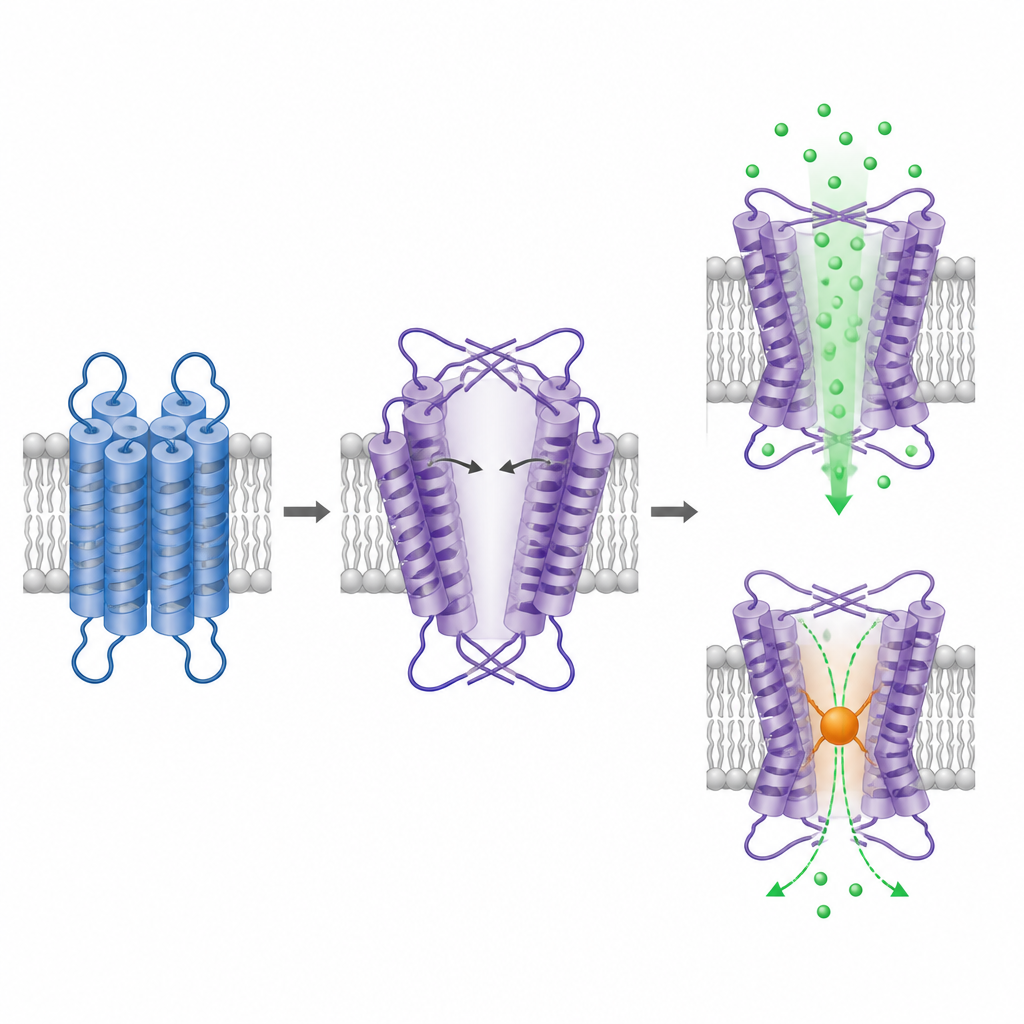
Aby zobaczyć, jak zbudowany jest TRPM1, zespół oczyścił obcięte białko i obrazował je za pomocą kriogenicznej mikroskopii elektronowej, techniki wizualizującej pojedyncze cząstki zamrożone w cienkiej warstwie lodu. Część wewnątrzkomórkowa TRPM1 tworzy znajomy, czterokrotny układ symetrii podobny do innych kanałów TRPM, co wzmacnia jego tożsamość jako kanału tetramerowego. Zaskoczenie kryje się w części przechodzącej przez błonę. Region podobny do czujnika napięcia i region poru nadal układają się w sposób wymiany domen (domain‑swapped), ale o odwrotnej „ręczności” w porównaniu ze wszystkimi dotychczas badanymi pokrewnymi kanałami jonowymi. Ta odwrócona aranżacja zmusza dwie helisy porowe do zagięcia i rozciągnięcia pod płytkimi kątami, tworząc dużą centralną jamę przypominającą szeroki, otwarty por.
Śledzenie jonów przez por
Powiększona jama w domenie błonowej TRPM1 ma, według szacunków, co najmniej około jednego nanometra szerokości w najwęższym miejscu, porównywalnie do otworów innych kanałów TRPM w ich stanie aktywnym. Wspiera to wcześniejsze sugestie, że TRPM1 ma tendencję do bycia konstytutywnie otwartym. Aby sprawdzić, czy przypuszczalny por rzeczywiście przewodzi wapń, badacze wprowadzili cysteinę w najwęższym miejscu i zastosowali reagent chemiczny, który przyłącza się do wystawionych cystein i dodaje objętości. To leczenie silnie zmniejszyło fluorescencję zależną od wapnia tylko w zmutowanym kanale, co wskazuje, że zablokowanie tej pozycji zakłóca przepływ jonów. Razem struktura i eksperyment blokujący przemawiają za tym, że zaobserwowana jama jest funkcjonalną ścieżką jonową w TRPM1.
Wskazówki dotyczące reakcji na leki i chorób
Ponieważ TRPM1 jest blisko spokrewniony z TRPM3, który był strukturalnie charakteryzowany z różnymi małocząsteczkowymi ligandami, autorzy porównali znane kieszenie wiążące między oboma kanałami. Miejsca w regionie podobnym do czujnika napięcia, które wiążą aktywatory i inhibitory w TRPM3, są dobrze zachowane w TRPM1, a inhibitor primidon rzeczywiście osłabił napływ wapnia zależny od TRPM1. W przeciwieństwie do tego steryd aktywujący TRPM3 w kieszeni między sensorem a porem nie mógł zostać pomieszczony w odwróconej architekturze TRPM1 i nie podniósł jego aktywności. Zespół również naniósł mutacje powodujące ludzką ślepotę nocną na strukturę; większość z nich znajduje się w rejonach, które wydają się stabilizować fałdowanie białka lub kontrolować jego trafienie do właściwego miejsca w komórkach siatkówki.
Co to oznacza dla widzenia nocnego
Mówiąc prosto, praca ta pokazuje, że TRPM1 rzeczywiście jest kanałem jonowym, ale z częścią przechodzącą przez błonę ułożoną w nieoczekiwany, odwrócony sposób, który nadal umożliwia istnienie szerokiego poru dla przejścia jonów. Ten niezwykły kształt może wyjaśniać, dlaczego TRPM1 zachowuje się inaczej niż jego krewni i reaguje na niektóre leki, a na inne nie. Wiążąc trójwymiarową architekturę TRPM1 z jego zdolnością do przenoszenia wapnia, badanie daje strukturalne podstawy do zrozumienia wrodzonej ślepoty nocnej oraz do badania, jak ten specjalny kanał pomaga naszym oczom widzieć przy najsłabszym świetle.
Cytowanie: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
Słowa kluczowe: TRPM1, kanał jonowy, widzenie nocne, siatkówka, kriogeniczna EM