Clear Sky Science · ru
Структура TRPM1 по данным крио-ЭМ демонстрирует нетипичную архитектуру с инвертированным трансмембранным доменом
Видеть в темноте
Каждый, кто пробирался по темной комнате, полагался на тонкий набор молекул в глазу, позволяющих видеть в сумерках. Одна из этих молекул — белок TRPM1 — давно предполагалась как мельчайший «ворота» в нервных клетках сетчатки, пропускающий заряженные частицы и передающий сигналы о слабом свете. Тем не менее ученым было трудно точно показать, как построен TRPM1 и действительно ли он функционирует как самостоятельный ионный канал. В этом исследовании объединены передовые методы визуализации и клеточные эксперименты, чтобы раскрыть необычную структуру TRPM1 и то, как он, вероятно, поддерживает ночное зрение.
Как передаются сигналы ночного зрения
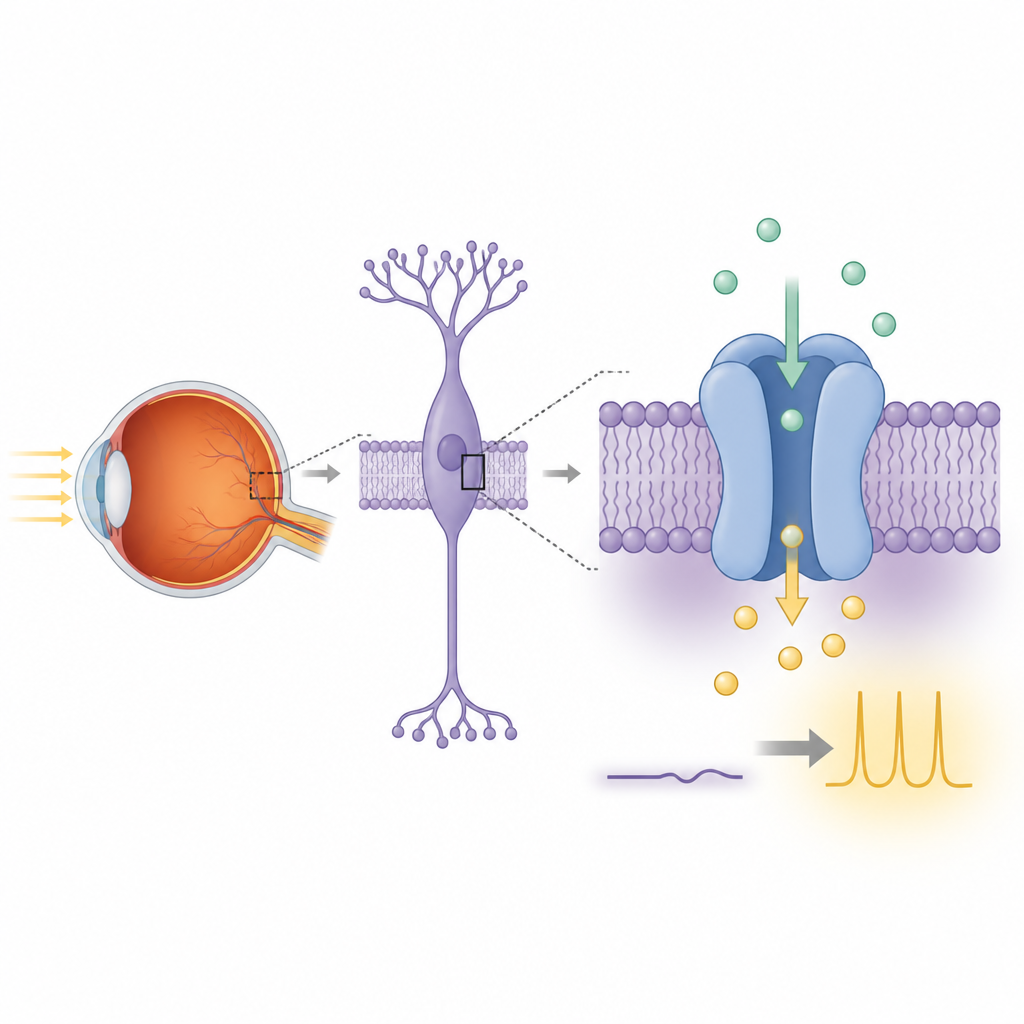
Ночное зрение начинается, когда палочковые фоторецепторы сетчатки регистрируют отдельные фотоны и передают эту информацию соседним биполярным клеткам. Внутри этих биполярных клеток цепочка сигнализации связывает глутаматный рецептор mGluR6 с TRPM1. На свету TRPM1 связан с постоянным входящим током положительно заряженных ионов, который поддерживает деполяризацию этих клеток. В темноте активация mGluR6 высвобождает субъединицы G‑белка, которые выключают этот ток, приводя клетку к реполяризации и завершая сигнал. Когда TRPM1 или его партнёры повреждены генетическими мутациями, этот световой путь нарушается и у людей развивается полная врожденная стационарная ночная слепота — состояние, при котором способность видеть при слабом освещении серьёзно нарушена.
Проверка: является ли TRPM1 настоящим каналом
Несмотря на близкое сходство с другими членами семейства TRPM, истинная функция TRPM1 годами оставалась предметом споров, потому что его электрическую активность трудно воспроизвести в стандартных лабораторных клеточных линиях. Авторы сначала создали конструкцию крысиного TRPM1, пригодную для структурных исследований, удалив гибкий хвостовой участок, несущественный для укладки. Они экспрессировали полноразмерный и укороченный TRPM1 в человеческих клетках HEK293, модифицированных так, чтобы они светились при входе кальция. При добавлении кальция снаружи значительно больше клеток, экспрессирующих TRPM1, загорелись по сравнению с контролем, и их флуоресценция возросла гораздо сильнее. Эти наблюдения свидетельствуют о том, что TRPM1 сам по себе может создавать путь для прохождения ионов кальция через мембрану, поддерживая идею о том, что это полноценный ионный канал.
Удивительная форма канала
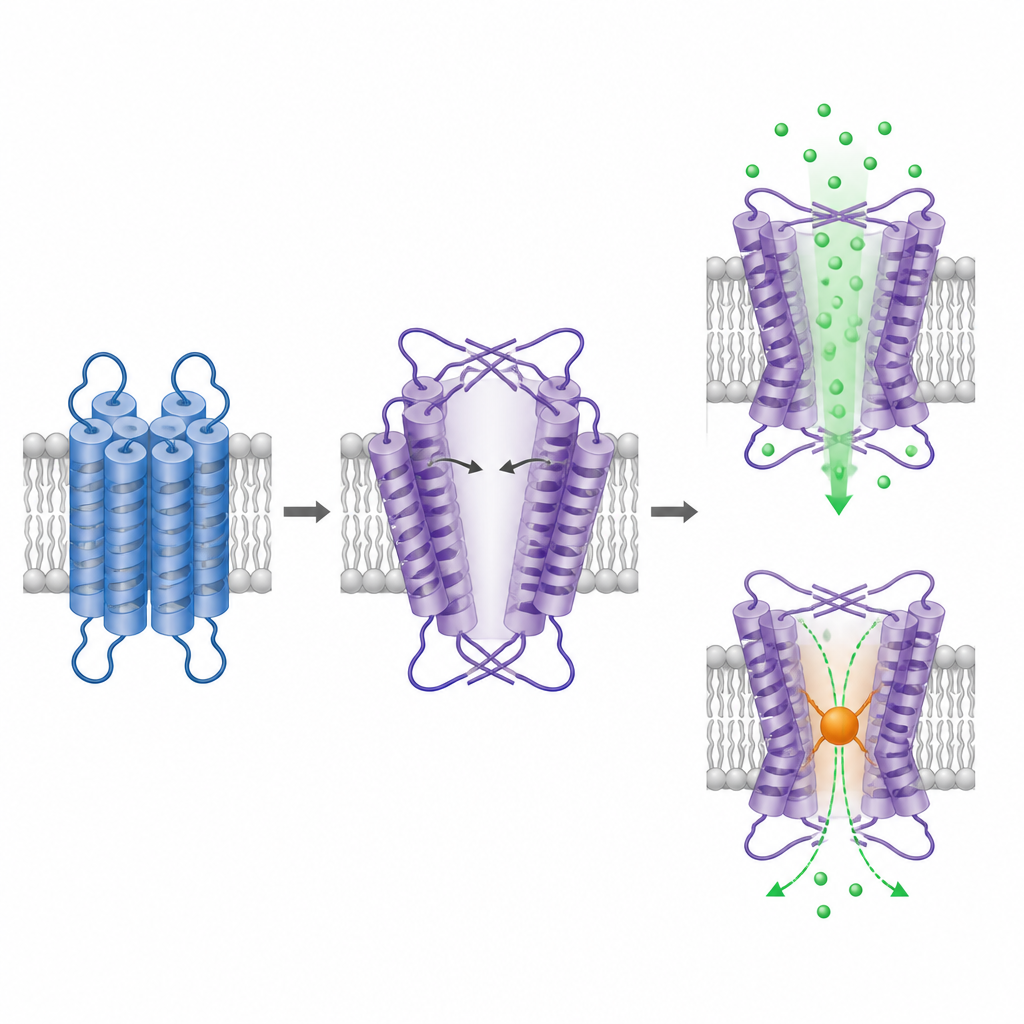
Чтобы увидеть, как устроен TRPM1, команда очистила укороченный белок и визуализировала его методом криогенной электронной микроскопии, который позволяет видеть отдельные частицы, замороженные в тонком слое льда. Внутриклеточная часть TRPM1 образует привычную четырёхчастную симметричную организацию, сходную с другими каналами TRPM, что подтверждает его тетрамерную природу. Сюрприз обнаруживается в трансмембранной части. Здесь область, похожая на датчик напряжения, и область поры по-прежнему расположены с обменом доменов, но с противоположной «правой/левой» конфигурацией по сравнению со всеми родственными ионными каналами, изученными ранее. Эта инвертированная компоновка заставляет две спирали поры сгибаться и растягиваться под малыми углами, создавая большую центральную полость, напоминающую широкую открытую пору.
Отслеживание ионов через пору
Увеличенная полость в мембранном домене TRPM1 оценивается как по крайней мере около одного нанометра в самом узком месте, что сопоставимо с отверстиями других TRPM‑каналов в их активном состоянии. Это поддерживает предыдущие предположения о том, что TRPM1 склонен к конститутивно открытому состоянию. Чтобы проверить, действительно ли предполагаемая пора проводит кальций, исследователи ввели цистеин в наиболее узкую точку и применили химический реагент, который присоединяется к доступным цистеинам и добавляет объём. Эта обработка существенно снизила зависящую от кальция флуоресценцию только у мутантного канала, что указывает на то, что блокирование этой позиции мешает прохождению ионов. В совокупности структура и эксперимент по блокированию подтверждают, что наблюдаемая полость является функциональным ионным путём в TRPM1.
Подсказки о реакции на лекарства и болезнях
Поскольку TRPM1 тесно связан с TRPM3, структура которого была охарактеризована с разными низкомолекулярными лигандами, авторы сравнили известные сайты связывания между двумя каналами. Участки в области, похожей на датчик напряжения, которые связывают активаторы и ингибиторы в TRPM3, хорошо консервативны в TRPM1, и ингибитор примидон действительно ослаблял вход кальция, зависящий от TRPM1. Напротив, стероид, активирующий TRPM3 в кармане между датчиком и порой, не смог поместиться в инвертированной архитектуре TRPM1 и не усилил его активность. Исследователи также сопоставили мутации, вызывающие ночную слепоту у человека, с картой структуры; большинство таких мутаций расположены в областях, которые, по-видимому, стабилизируют укладку белка или контролируют его транспортировку в нужное место в клетках сетчатки.
Что это значит для ночного зрения
Проще говоря, эта работа показывает, что TRPM1 действительно является ионным каналом, но с трансмембранной областью, организованной неожиданным, инвертированным образом, который при этом допускает широкую пору для прохождения ионов. Такая необычная форма может объяснять, почему TRPM1 ведёт себя иначе, чем его родственники, и реагирует на одни лекарства, но не на другие. Связав трёхмерную архитектуру TRPM1 с его способностью проводить кальций, исследование закладывает структурную основу для понимания наследственной ночной слепоты и для изучения того, как этот особый канал помогает нашим глазам видеть при едва заметном освещении.
Цитирование: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
Ключевые слова: TRPM1, ионный канал, ночное зрение, сетчатка, крио-ЭМ