Clear Sky Science · sv
Cryo-EM-struktur av TRPM1 visar en icke-kanonisk arkitektur med ett inverterat transmembrandomän
Se i mörkret
Alla som famlat sig fram i ett mörkt rum har varit beroende av ett fint samspel av molekyler i ögat som möjliggör mörkerseende. Ett av dessa, ett protein kallat TRPM1, har länge misstänkts fungera som en liten grind i nervceller i näthinnan, som släpper igenom laddade atomer och förmedlar signaler om svagt ljus. Ändå har forskare haft svårt att visa exakt hur TRPM1 är byggt och om det verkligen fungerar som en fristående jonkanal. Denna studie kombinerar avancerad avbildning och cellexperiment för att avslöja TRPM1:s ovanliga struktur och hur den sannolikt stödjer mörkerseendet.
Hur mörkerseendesignaler färdas
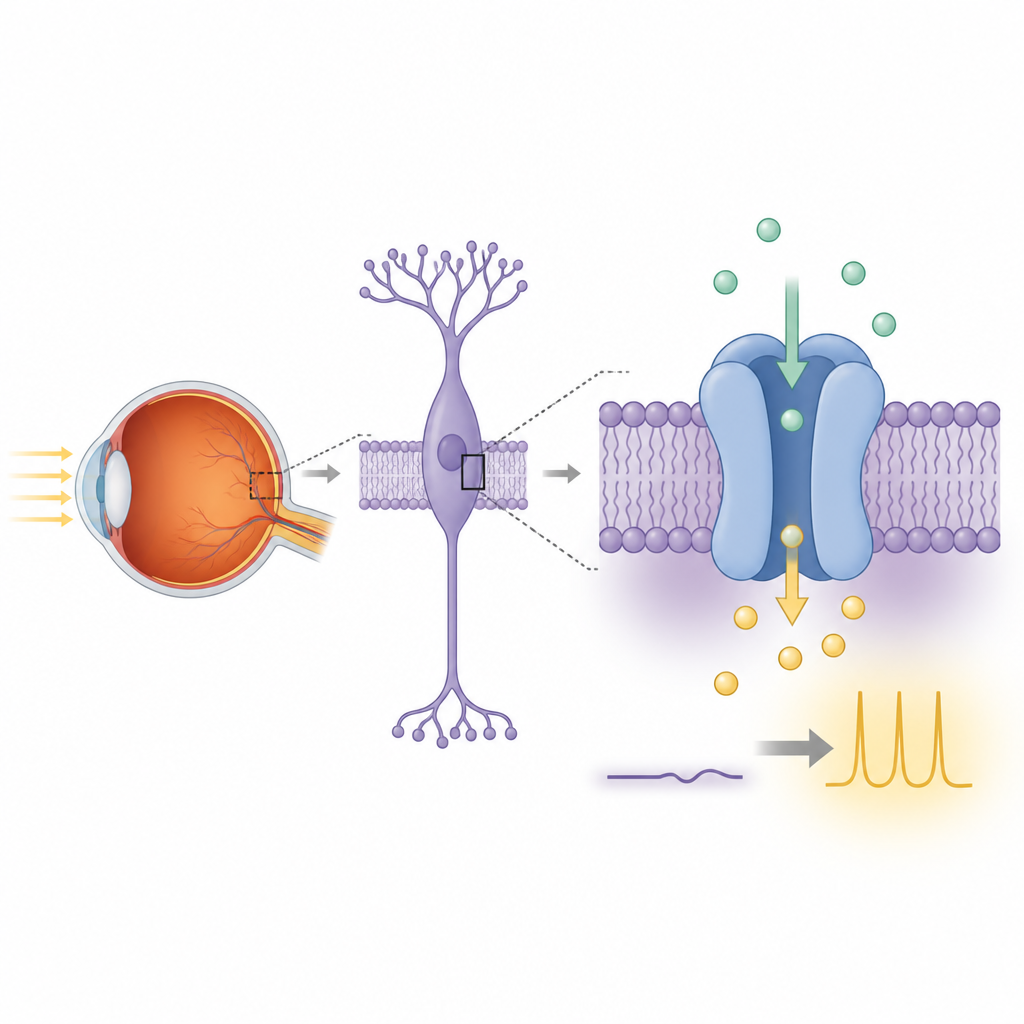
Mörkerseende börjar när stavarnas fotoreceptorer i näthinnan upptäcker enstaka fotoner och vidarebefordrar den informationen till närliggande bipolära celler. Inuti dessa bipolära celler kopplar en signalväg en glutamatreceptor kallad mGluR6 till TRPM1. I ljus är TRPM1 kopplat till en stadig inåtgående ström av positivt laddade joner som håller dessa celler depolariserade. I mörker frigör aktiveringen av mGluR6 G-proteinsubenheter som stänger av denna ström, återpolariserar cellen och avslutar signalen. När TRPM1 eller dess följeslagare skadas av genetiska mutationer fallerar denna ljusdrivna kommunikation och personer kan utveckla komplett medfödd stationär nattblindhet, ett tillstånd där förmågan att se i svagt ljus är kraftigt nedsatt.
Test av om TRPM1 är en verklig kanal
Trots sin nära likhet med andra jonkanaler i TRPM-familjen har TRPM1:s verkliga funktion debatterats i åratal eftersom dess elektriska aktivitet är svår att reproducera i vanliga cellinjer. Författarna skapade först en rått-TRPM1-konstruktion lämpad för strukturarbete och kortade bort en rörlig svansregion som inte behövs för veckning. De uttryckte antingen fullängds- eller trunkerad TRPM1 i humana HEK293-celler som konstruerats för att lysa när kalcium tar sig in. När kalcium tillfördes utanför cellerna tändes betydligt fler TRPM1-uttryckande celler än kontrollceller, och deras fluorescens ökade mycket mer. Dessa observationer tyder på att TRPM1 på egen hand kan skapa en väg för kalciumjoner att korsa membranet, vilket stöder idén att det är en äkta jonkanal.
En överraskande kanalform
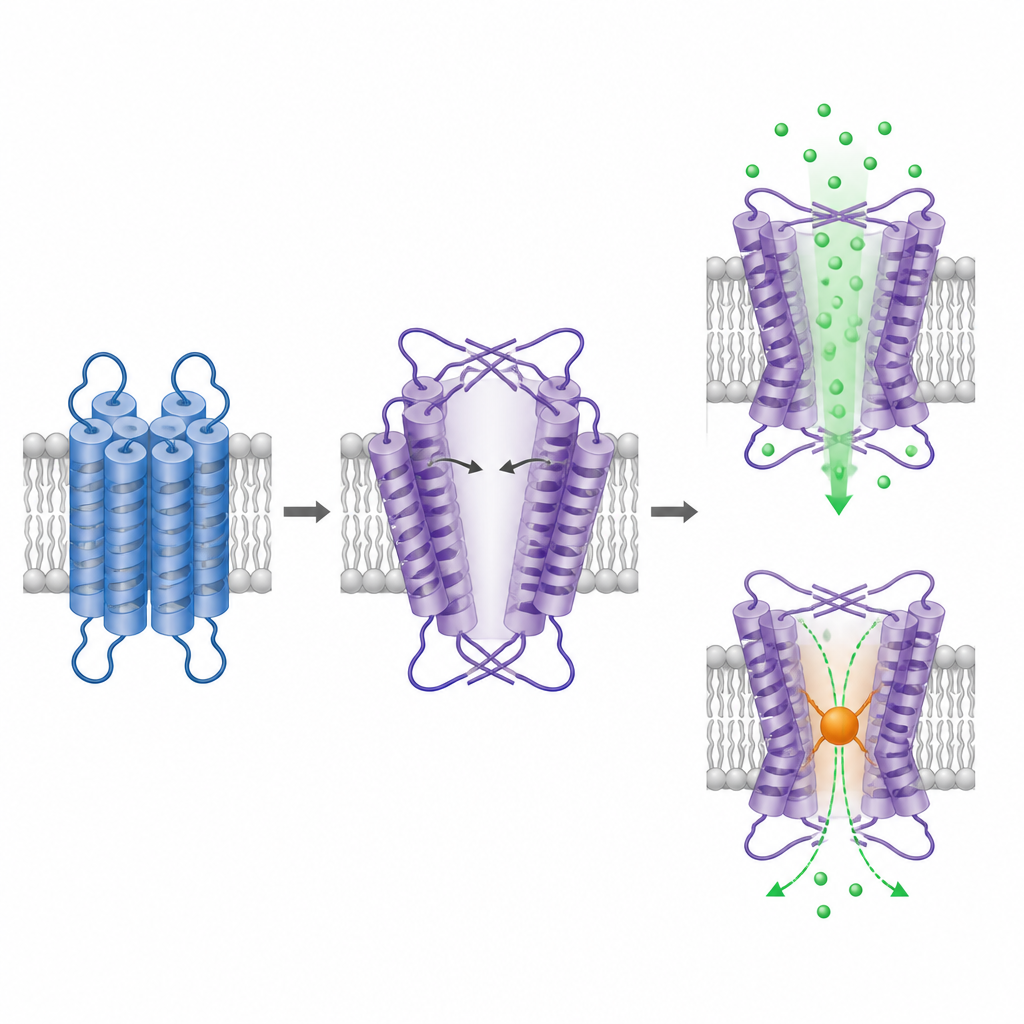
För att se hur TRPM1 är uppbyggt renade teamet det trunkerade proteinet och avbildade det med kryoelektronmikroskopi, en teknik som visualiserar enskilda partiklar frysta i ett tunt iskikt. Den intracellulära delen av TRPM1 bildar en välkänd fyrfaldig symmetrisk arrangemang likt andra TRPM-kanaler, vilket stärker dess identitet som en tetramer kanal. Överraskningen finns i den del som sträcker sig genom membranet. Här är den spänningssensorliknande regionen och porregionen fortfarande ordnade i en domän‑bytt (domain-swapped) konfiguration, men med motsatt handighet jämfört med alla närbesläktade jonkanaler som studerats hittills. Denna inverterade layout tvingar två av porhelixarna att böjas och sträckas i grunda vinklar, vilket skapar en stor central kavitetsliknande öppning som liknar en vid, öppen por.
Följa joner genom poren
Den förstorade kavitetsdelen i TRPM1:s membrandomän uppskattas vara minst omkring en nanometer över vid sitt smalaste ställe, jämförbar med öppningarna i andra TRPM-kanaler i deras aktiva tillstånd. Detta stöder tidigare förslag om att TRPM1 tenderar att vara konstitutivt öppen. För att testa om den föreslagna poren verkligen leder kalcium konstruerade forskarna in en cystein vid det smalaste stället och applicerade ett kemiskt reagens som binder till exponerade cysteiner och tillför volym. Denna behandling minskade starkt den kalciumberoende fluorescensen endast i mutantkanalen, vilket indikerar att blockering på denna position stör jonpermeation. Tillsammans talar strukturen och blockeringsexperimentet för att den observerade kaviteten är den funktionella jonvägen i TRPM1.
Ledtrådar till läkemedelssvar och sjukdom
Eftersom TRPM1 är nära besläktad med TRPM3, som har strukturellt karakteriserats med olika småmolekylära ligander, jämförde författarna kända binderfickor mellan de två kanalerna. Siter i den spänningssensorliknande regionen som binder aktivatorer och hämmare i TRPM3 är väl bevarade i TRPM1, och hämmaren primidon dämpade faktiskt TRPM1‑beroende kalciuminflöde. I kontrast kunde en steroid som aktiverar TRPM3 i en ficka mellan sensorn och poren inte rymmas i TRPM1:s inverterade arkitektur och lyckades inte öka TRPM1‑aktiviteten. Teamet kartlade också mänskliga nattblindhetsmutationer på strukturen; de flesta ligger i regioner som verkar stabilisera proteinets veckning eller kontrollera dess trafik till rätt plats i näthinnans celler.
Vad detta betyder för mörkerseendet
I klara termer visar detta arbete att TRPM1 verkligen är en jonkanal, men med en membranöverskridande region ordnad på ett oväntat, inverterat sätt som ändå tillåter en stor por för jonpassage. Denna ovanliga form kan förklara varför TRPM1 beter sig annorlunda än sina släktingar och svarar på vissa läkemedel men inte andra. Genom att knyta TRPM1:s tredimensionella arkitektur till dess förmåga att föra kalcium ger studien en strukturell grund för att förstå ärftlig nattblindhet och för att undersöka hur denna speciella kanal hjälper våra ögon att se i det svagaste ljuset.
Citering: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
Nyckelord: TRPM1, jonkanal, nattseende, näthinna, cryo-EM