Clear Sky Science · he
מבנה Cryo-EM של TRPM1 חושף ארכיטקטורה לא-קאנונית עם דומיין טרנסממברנלי הפוך
לראות בחושך
כל מי שהתהלך בחדר חשוך הסתמך על מערכת עדינה של מולקולות בעין שמאפשרת ראיית לילה. אחת מהן, חלבון הנקרא TRPM1, נתפסת מזה זמן כשער זעיר בתאי עצב של הרשתית, שמאפשר לעבור אטומים טעונים ולשאת איתותים לגבי אור חלש. עם זאת, מדענים התקשו להראות בדיוק כיצד TRPM1 בנויה והאם היא באמת פועלת כתעלת יונים עצמאית. המחקר הזה משלב הדמיה מתקדמת וניסויים בתאים כדי לחשוף את המבנה הבלתי שגרתי של TRPM1 וכיצד היא סביר שתומכת בראיית לילה.
כיצד עוברות אותות ראיית הלילה
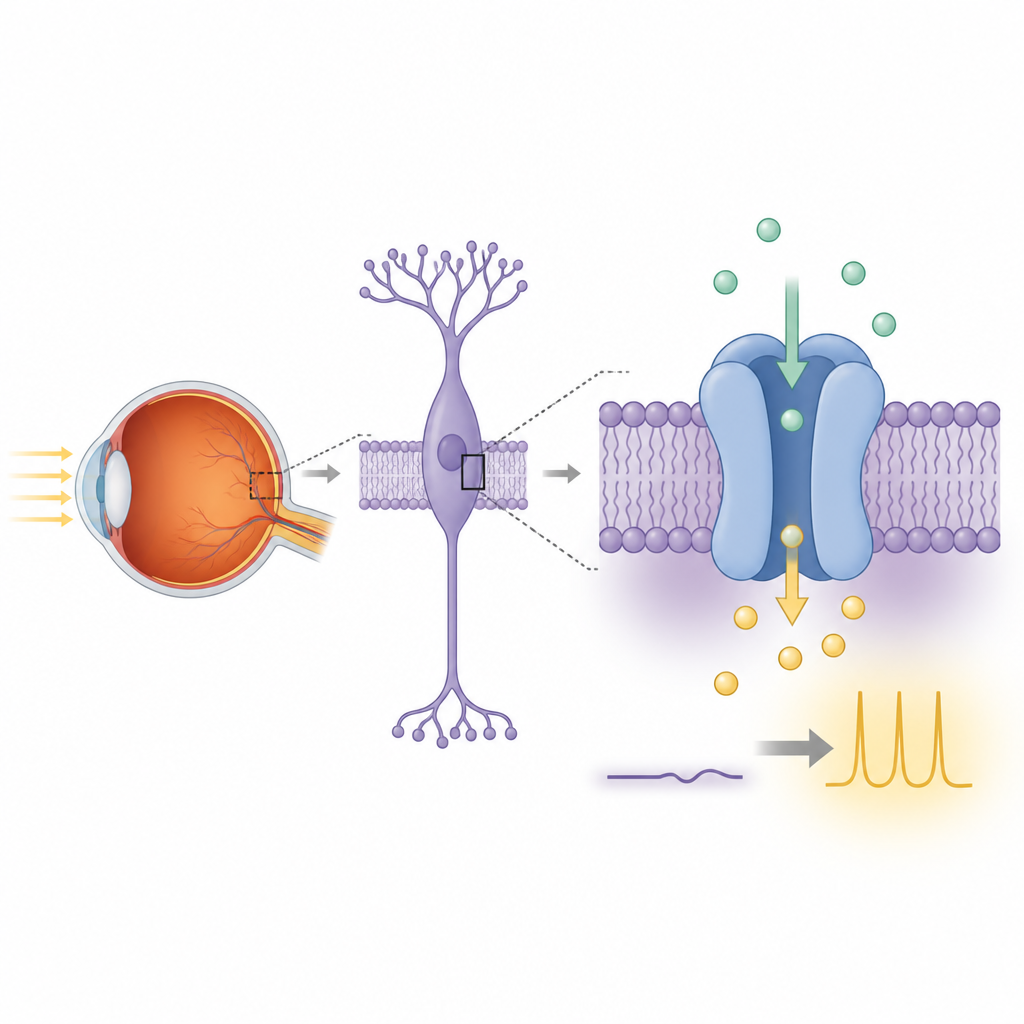
ראיית לילה מתחילה כאשר קולטני המקלונים ברשתית מזהים פוטון יחיד ומעבירים את המידע לתאי ביניים סמוכים. בתוך תאי הביניים הללו, שרשרת איתות מקשרת רצפטור לגלוטמט בשם mGluR6 ל-TRPM1. באור, TRPM1 מקושרת לזרם פנימי קבוע של יונים חיוביים ששומר על דפולריזציה של תאים אלה. בחושך, הפעלת mGluR6 משחררת תת-יחידות חלבון G שמשביתות את הזרם הזה, מחזירות את התא למצב ריפולריזציה ומסיימות את האיתות. כאשר TRPM1 או שותפיה פגועים על ידי מוטציות גנטיות, התקשורת המונחת-אור נכשלת ואנשים עלולים לפתח עוורון לילה מולד סטציונרי מלא, מצב שבו הראייה בתאורה חלשה נפגעת קשות.
בדיקת האם TRPM1 היא תעלה אמיתית
למרות הדמיון הקרוב שלה לערוצי משפחת TRPM האחרים, תפקידה האמיתי של TRPM1 היה שנוי במחלוקת במשך שנים מכיוון שהפעילות החשמלית שלה קשה לשחזור בקווי תאים מעבדה סטנדרטיים. החוקרים יצרו תחילה בניית TRPM1 של חולדה המתאימה לעבודה מבנית, וגזרו קצה זנב גמיש שאינו דרוש לקיפול. הם הביעו ב-SEK293 אנושיות מהונדסות להאיר כשסידן נכנס, אם את ה-TRPM1 המלאה ואם את הטרונקאציה. כאשר הוסיפו סידן מחוץ לתאים, הרבה יותר תאים מבטאים TRPM1 נדלקו מאשר תאי בקרה, והפלואורסצנציה שלהם עלתה בעוצמה רבה יותר. תצפיות אלה מעידות ש-TRPM1 לבדה יכולה ליצור נתיב לחדירת יוני סידן דרך הממברנה, ותומכות ברעיון שהיא אכן תעלת יונים לגיטימית.
צורת תעלה מפתיעה
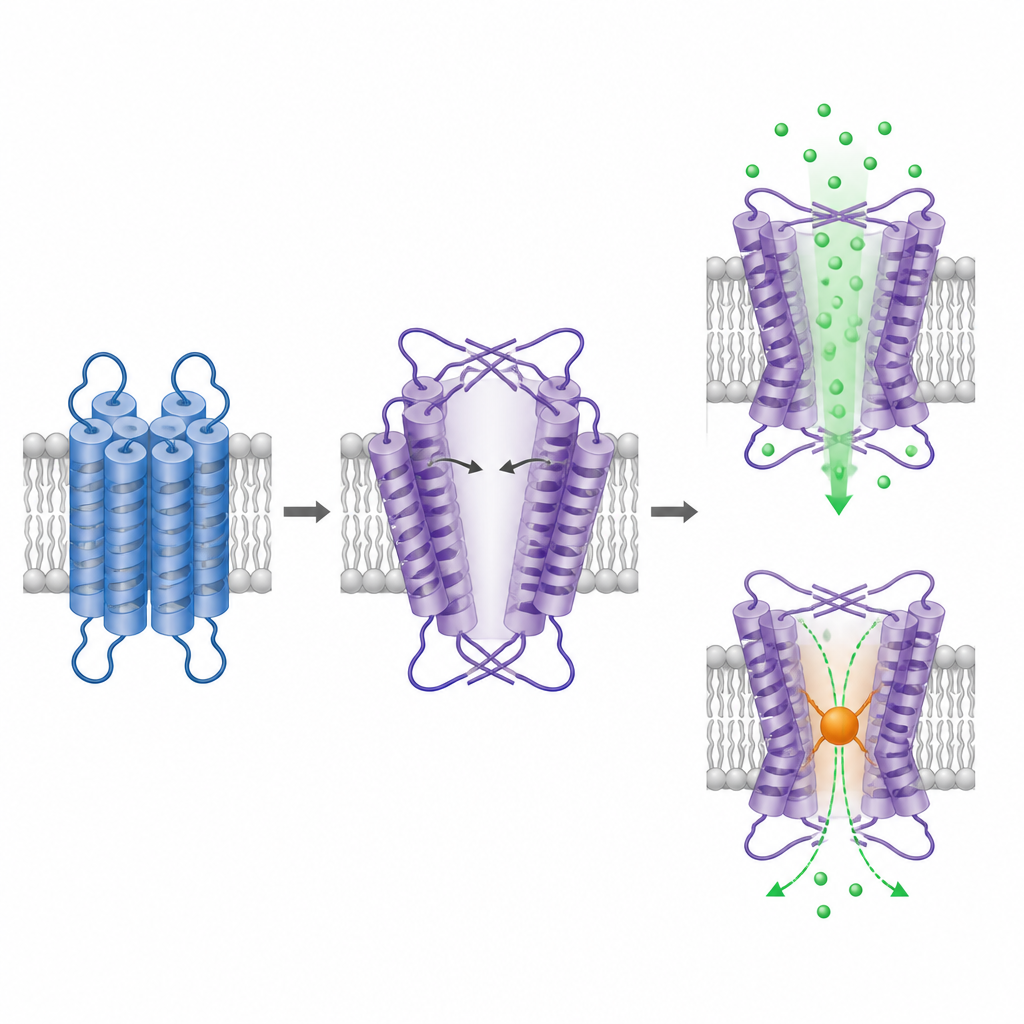
כדי לראות כיצד TRPM1 בנויה, הקבוצה טיהרה את החלבון הטרונקי והדמיתה אותו באמצעות מיקרוסקופ אלקטרונים קפוא (cryo-EM), טכניקה הממחישה חלקיקים מוקפאים בשכבת קרח דקה. החלק התוך-תאי של TRPM1 יוצר סידור סימטרי בארבע־קפל שהוא מוכר מדומיינים של ערוצי TRPM אחרים, וחיזק את זהותה כערוץ טטרמרי. ההפתעה נמצאת בחלק החוצה בממברנה. כאן, אזור דמוי חיישן מתח ותחום הנקבוב עדיין מסודרים במבנה domain-swapped, אבל עם כיווניות הפוכה בהשוואה לכל ערוצי היונים הקרובים שנחקרו עד כה. פריסת הפוכה זו מאלצת שתי הליקסות של הנקבוב להתכופף ולהתארך בזוויות שטוחות, ויוצרת חלל מרכזי גדול המזכיר נקבוב רחב ופתוח.
מעקב אחר היונים דרך הנקבוב
החלל המורחב בדומיין הממברנלי של TRPM1 מוערך ככמעט ננומטר אחד ברוחבו בנקודה הצרה ביותר, גודל השווה לפתחים של ערוצי TRPM אחרים במצב הפעיל שלהם. עובדה זו תומכת בהצעות קודמות ש-TRPM1 נוטה להיות פתוחה ברצף. כדי לבדוק האם הנקבוב המוצע אכן מעביר סידן, החוקרים מהנדסים ציסטאין בנקודה הצרה ביותר ויישמו תג כימי שמתחבר לציסטאינים חשופים ומוסיף נפח. הטיפול הזה הפחית בהדרגה את הפלואורסצנציה התלויה בסידן רק בערוץ המוטנטי, מה שמצביע על כך שחסימת המיקום הזה מפריעה לחדירות היונים. יחד, המבנה וניסוי החסימה תומכים בכך שהחלל הנצפה הוא נתיב היונים התפקודי ב-TRPM1.
רמזים לתגובות לתרופות ומחלה
מכיוון ש-TRPM1 קשורה בקשר הדוק ל-TRPM3, שאותו תיארו מבחינה מבנית עם ליגנדים קטנים שונים, המחברים השוו כיסי קשירה ידועים בין שתי התעלות. אתרים באזור דמוי החיישן למתח שקושרים ממריצים ומעכבים ב-TRPM3 שמורים היטב ב-TRPM1, והמעכב פרימידון אכן הקטין את כניסת הסידן התלויה ב-TRPM1. לעומת זאת, סטרואיד שמפעיל את TRPM3 בכיס בין החיישן לנקבוב לא יכול היה להתאים בארכיטקטורה ההפוכה של TRPM1 ונכשל בהגברה של פעילותה. הצוות גם מיפו מוטציות אנושיות של עוורון לילה על המבנה; רוב המוטציות נמצאות באזורים שנראים כמייצבים את קיפול החלבון או מבקרים את היעתו למקום הנכון בתאי הרשתית.
מה משמעות הדבר לראיית לילה
במלים פשוטות, עבודה זו מראה ש-TRPM1 אכן תעלת יונים, אך עם אזור החוצה את הממברנה המסודר באופן בלתי צפוי והפוך שמאפשר עדיין נקבוב גדול למעבר יונים. צורה יוצאת דופן זו עשויה להסביר מדוע TRPM1 מתנהגת שונה מקרוביה ומגיבה לחלק מהתרופות אך לא לאחרות. על ידי קישור הארכיטקטורה התלת־ממדית של TRPM1 ליכולתה לשאת סידן, המחקר מספק בסיס מבני להבנת עוורון הלילה התורשתי ולחקירת האופן שבו תעלה מיוחדת זו עוזרת לעינינו לראות בתאורה החלשה ביותר.
ציטוט: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
מילות מפתח: TRPM1, תעלת יונים, ראיית לילה, רשתית, cryo-EM