Clear Sky Science · nl
Cryo-EM-structuur van TRPM1 onthult een niet‑canonische architectuur met een omgekeerd transmembraandomein
Zien in het donker
Iedereen die wel eens door een donkere kamer heeft gelopen, vertrouwt op een fijn afgestemde reeks moleculen in het oog die nachtzicht mogelijk maken. Eén van deze, een eiwit genaamd TRPM1, werd lang verondersteld te fungeren als een klein poortje in zenuwcellen van het netvlies, dat geladen deeltjes doorlaat en signalen over zwak licht draagt. Toch hebben wetenschappers moeite gehad precies aan te tonen hoe TRPM1 is opgebouwd en of het daadwerkelijk zelfstandig als ionkanaal functioneert. Deze studie combineert geavanceerde beeldvorming en celexperimenten om TRPM1’s ongewone structuur te onthullen en te laten zien hoe het waarschijnlijk het nachtzicht ondersteunt.
Hoe nachtzichtsignalen reizen
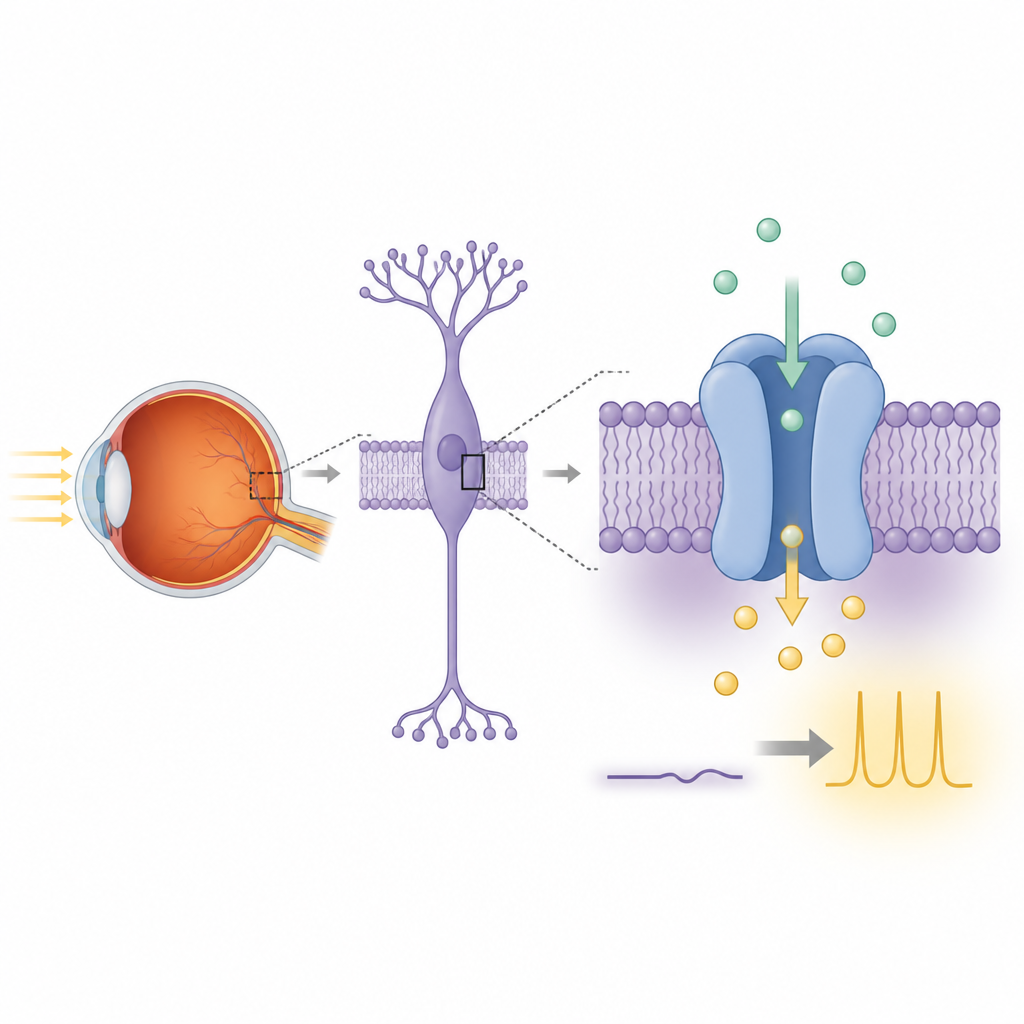
Nachtzicht begint wanneer staafjes in het netvlies individuele fotonen detecteren en die informatie doorgeven aan naburige bipolaire cellen. Binnen deze bipolaire cellen schakelt een signaalroute een glutamaatreceptor, mGluR6, aan TRPM1. Bij licht gaat TRPM1 gepaard met een constante instroming van positief geladen ionen die deze cellen gedepolariseerd houdt. In het donker leidt activering van mGluR6 tot vrijlating van G‑proteïnesubunits die deze stroom afsluiten, waardoor de cel repolariseert en het signaal eindigt. Wanneer TRPM1 of zijn partners door genetische mutaties beschadigd raken, faalt deze lichtgestuurde communicatie en kunnen mensen een volledige congenitale stationaire nachtblindheid ontwikkelen, een aandoening waarbij zien bij weinig licht ernstig is aangetast.
Testen of TRPM1 echt een kanaal is
Ondanks de nauwe gelijkenis met andere TRPM‑familie ionkanalen is de ware functie van TRPM1 jarenlang ter discussie geweest omdat zijn elektrische activiteit moeilijk reproduceerbaar is in standaard laboratoriumcelijnen. De auteurs maakten eerst een ratten‑TRPM1‑construct geschikt voor structureel onderzoek door een flexibele staartregio weg te knippen die niet nodig is voor vouwing. Ze brachten zowel de volledige als de ingekorte TRPM1 tot expressie in menselijke HEK293‑cellen die oplichten wanneer calcium binnenkomt. Wanneer calcium buiten de cellen werd toegevoegd, lichtten veel meer TRPM1‑expressie‑cellen op dan controles en nam hun fluorescentie veel sterker toe. Deze waarnemingen geven aan dat TRPM1 op zichzelf een doorgang voor calciumionen over het membraan kan creëren, wat het idee ondersteunt dat het een echt ionkanaal is.
Een verrassende kanaalvorm
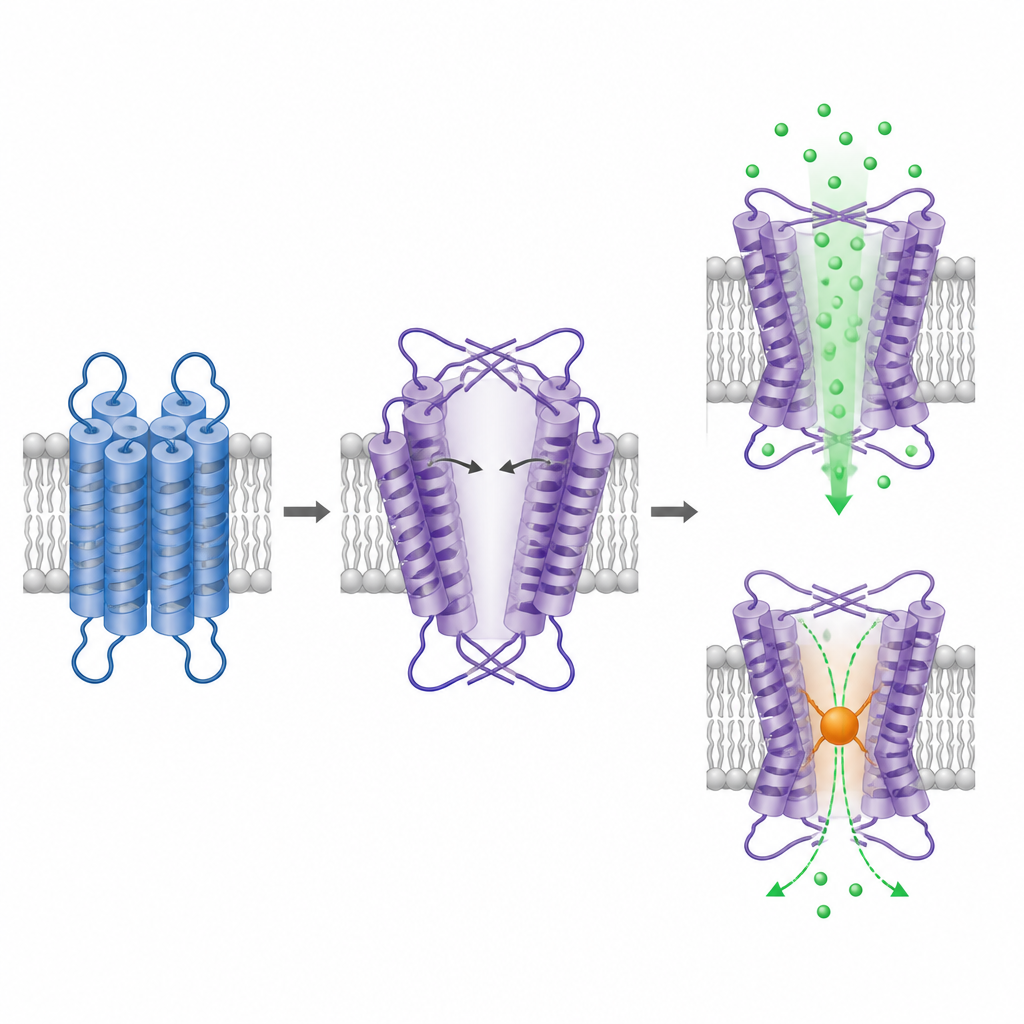
Om te zien hoe TRPM1 is opgebouwd, zuiverde het team het ingekorte eiwit en maakte er beelden van met cryogene elektronenmicroscopie, een techniek die individuele deeltjes visualiseert bevroren in een dun ijslaagje. Het intracellulaire gedeelte van TRPM1 vormt een vertrouwde viervoudig symmetrische ordening vergelijkbaar met andere TRPM‑kanalen, wat zijn identiteit als tetramere kanaal bevestigt. De verrassing zit in het membraanbruikende deel. Daar zijn het voltagesensor‑achtige gebied en het poriegebied nog steeds in een domein‑gewisselde configuratie gerangschikt, maar met de tegenovergestelde oriëntatie vergeleken met alle gerelateerde ionkanalen die tot nu toe bestudeerd zijn. Deze omgekeerde opstelling dwingt twee van de porelelices om bij ondiepe hoeken te buigen en uit te rekken, waardoor een grote centrale holte ontstaat die lijkt op een brede, open porie.
Volgen van ionen door de porie
De vergrote holte in TRPM1’s membraandomein wordt geschat ten minste ongeveer één nanometer breed te zijn op het smalste punt, vergelijkbaar met de openingen van andere TRPM‑kanalen in hun actieve toestand. Dit ondersteunt eerdere suggesties dat TRPM1 de neiging heeft constitutief open te zijn. Om te testen of de veronderstelde porie daadwerkelijk calcium leidt, introduceerden de onderzoekers een cysteïne op het smalste punt en brachten een chemisch reagens aan dat zich aan blootliggende cysteïnes hecht en extra massa toevoegt. Deze behandeling verminderde de calciummetingen sterk, maar alleen in het gemuteerde kanaal, wat aangeeft dat blokkering van deze positie de ionendoorgang belemmert. Samen pleiten de structuur en het blokkeerexperiment ervoor dat de waargenomen holte de functionele iondoorgang in TRPM1 is.
Aanwijzingen voor medicijnreacties en ziekte
Aangezien TRPM1 nauw verwant is aan TRPM3, dat structureel is gekarakteriseerd in complex met verschillende kleine molecuul‑liganden, vergeleken de auteurs bekende bindingspockets tussen de twee kanalen. Sites in het voltagesensor‑achtige gebied die in TRPM3 activatoren en remmers binden, zijn goed geconserveerd in TRPM1, en de remmer primidon dempte inderdaad TRPM1‑afhankelijke calciuminflux. In contrast kon een steroid dat TRPM3 activeert in een pocket tussen sensor en porie niet worden geaccommodeerd in TRPM1’s omgekeerde architectuur en versterkte TRPM1‑activiteit niet. Het team bracht ook menselijke nachtblindheidsmutaties in kaart op de structuur; de meeste liggen in regio’s die het eiwitvouwing stabiliseren of het transport naar de juiste plaats in netvliescellen regelen.
Wat dit betekent voor nachtzicht
Eenvoudig gezegd laat dit werk zien dat TRPM1 daadwerkelijk een ionkanaal is, maar met een transmembraan‑regio die op een onverwachte, omgekeerde manier is gerangschikt en toch een grote porie voor ionpassage toelaat. Deze ongewone vorm kan verklaren waarom TRPM1 zich anders gedraagt dan zijn verwanten en op sommige geneesmiddelen reageert maar op andere niet. Door de driedimensionale architectuur van TRPM1 te koppelen aan zijn vermogen calcium te geleiden, biedt de studie een structurele basis om erfelijke nachtblindheid te begrijpen en te onderzoeken hoe dit speciale kanaal onze ogen helpt zien bij het zwakste licht.
Bronvermelding: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
Trefwoorden: TRPM1, ionkanaal, nachtzicht, netvlies, cryo-EM