Clear Sky Science · fr
Structure Cryo-EM de TRPM1 révèle une architecture non canonique avec un domaine transmembranaire inversé
Voir dans le noir
Quiconque s’est frayé un chemin dans une pièce sombre a compté sur un ensemble délicat de molécules dans l’œil qui rendent la vision nocturne possible. L’une d’elles, une protéine appelée TRPM1, est depuis longtemps suspectée d’agir comme une petite porte dans les neurones de la rétine, laissant passer des atomes chargés et transmettant des signaux sur la faible lumière. Pourtant, les scientifiques ont eu du mal à montrer exactement comment TRPM1 est construit et si elle fonctionne réellement comme un canal ionique autonome. Cette étude combine imagerie avancée et expériences cellulaires pour révéler la structure inhabituelle de TRPM1 et la façon dont elle soutient probablement la vision nocturne.
Comment les signaux de la vision nocturne voyagent
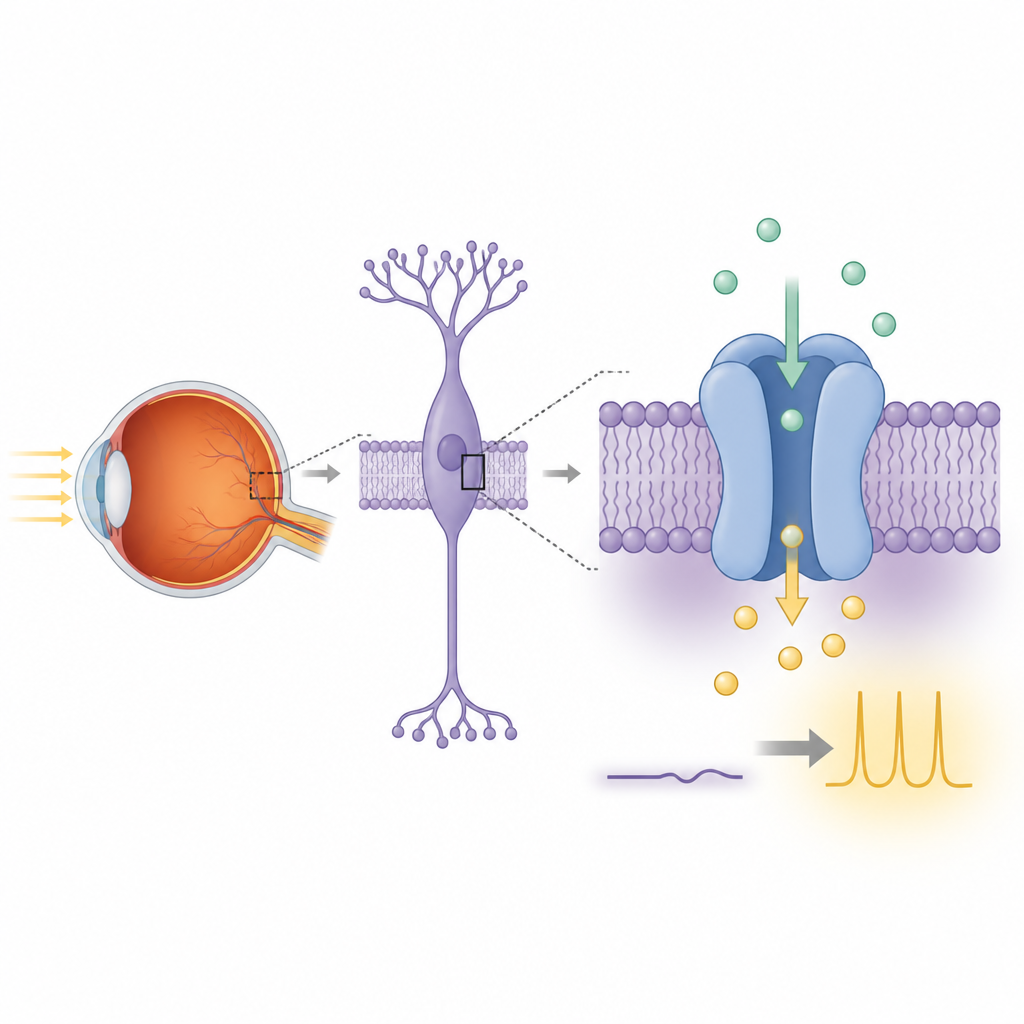
La vision nocturne commence lorsque les photorécepteurs en bâtonnets de la rétine détectent des photons isolés et transmettent cette information aux cellules bipolaires voisines. À l’intérieur de ces cellules bipolaires, une chaîne de signalisation relie un récepteur au glutamate appelé mGluR6 à TRPM1. À la lumière, TRPM1 est associé à un courant entrant soutenu d’ions positifs qui maintient ces cellules dépolarisées. Dans l’obscurité, l’activation de mGluR6 libère des sous-unités de protéine G qui coupent ce courant, repolarisant la cellule et mettant fin au signal. Lorsque TRPM1 ou ses partenaires sont endommagés par des mutations génétiques, cette communication dépendante de la lumière échoue et des personnes peuvent développer une amaurose congénitale stationnaire complète de la nuit, une condition où la vision en faible luminosité est sévèrement altérée.
Tester si TRPM1 est un vrai canal
Malgré sa forte similarité avec d’autres canaux TRPM, la fonction réelle de TRPM1 a fait débat pendant des années parce que son activité électrique est difficile à reproduire dans des lignées cellulaires de laboratoire standard. Les auteurs ont d’abord conçu un montage de TRPM1 de rat adapté au travail structural, en coupant une région terminale flexible qui n’est pas nécessaire pour le repliement. Ils ont exprimé TRPM1 en longueur complète ou tronquée dans des cellules HEK293 humaines modifiées pour s’illuminer lorsqu’il y a entrée de calcium. Lorsque du calcium a été ajouté à l’extérieur des cellules, bien plus de cellules exprimant TRPM1 se sont allumées que dans les contrôles, et leur fluorescence a augmenté beaucoup plus fortement. Ces observations indiquent que TRPM1, à elle seule, peut créer une voie pour que des ions calcium traversent la membrane, soutenant l’idée qu’il s’agit d’un canal ionique authentique.
Une forme de canal surprenante
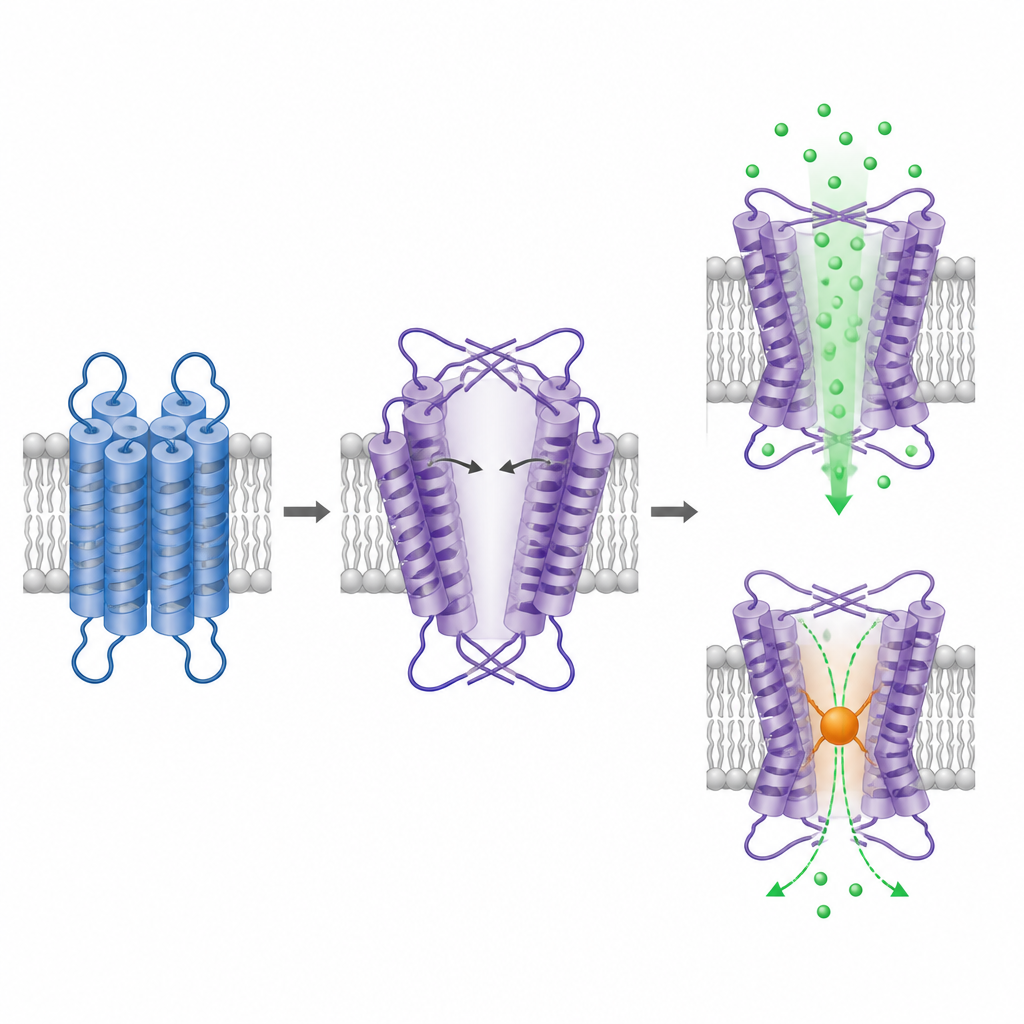
Pour voir comment TRPM1 est construite, l’équipe a purifié la protéine tronquée et l’a imagée par microscopie électronique cryogénique, une technique qui visualise des particules individuelles congelées dans une mince couche de glace. La portion intracellulaire de TRPM1 forme un agencement familier à symétrie quaternaire similaire à d’autres canaux TRPM, renforçant son identité de canal tétramérique. La surprise réside dans la partie qui traverse la membrane. Ici, la région semblable à un senseur de tension et la région de pore restent arrangées selon un échange de domaines, mais avec une chiralité opposée comparée à tous les canaux ioniques apparentés étudiés jusqu’à présent. Cette disposition inversée oblige deux des hélices du pore à se plier et à s’étirer à des angles peu prononcés, créant une grande cavité centrale qui ressemble à un pore large et ouvert.
Suivre les ions à travers le pore
La cavité agrandie dans le domaine membranaire de TRPM1 est estimée mesurer au moins environ un nanomètre à son point le plus étroit, comparable aux ouvertures d’autres canaux TRPM à l’état actif. Cela soutient les suggestions antérieures que TRPM1 tend à être constitutivement ouverte. Pour tester si le pore putatif transporte réellement le calcium, les chercheurs ont introduit une cystéine au point le plus étroit et appliqué un réactif chimique qui se fixe aux cystéines exposées et ajoute du volume. Ce traitement a fortement réduit la fluorescence dépendante du calcium uniquement dans le canal mutant, indiquant que le blocage de cette position gêne la perméation ionique. Ensemble, la structure et l’expérience de blocage soutiennent que la cavité observée est la voie ionique fonctionnelle de TRPM1.
Indices sur les réponses aux médicaments et la maladie
Parce que TRPM1 est étroitement apparenté à TRPM3, qui a été caractérisé structurellement avec divers petits ligands, les auteurs ont comparé des sites de liaison connus entre les deux canaux. Des sites dans la région semblable au senseur de tension qui lient des activateurs et des inhibiteurs dans TRPM3 sont bien conservés dans TRPM1, et l’inhibiteur primidone a en effet atténué l’entrée de calcium dépendante de TRPM1. En revanche, un stéroïde qui active TRPM3 à un site entre le senseur et le pore ne pouvait pas être accommodé dans l’architecture inversée de TRPM1 et n’a pas réussi à augmenter l’activité de TRPM1. L’équipe a également cartographié des mutations humaines responsables de la cécité nocturne sur la structure ; la plupart se situent dans des régions qui semblent stabiliser le repliement de la protéine ou contrôler son adressage au bon endroit dans les cellules rétiniennes.
Ce que cela signifie pour la vision nocturne
En termes simples, ce travail montre que TRPM1 est bien un canal ionique, mais avec une région traversant la membrane arrangée de façon inattendue et inversée qui permet néanmoins un pore large pour le passage des ions. Cette forme inhabituelle peut expliquer pourquoi TRPM1 se comporte différemment de ses homologues et répond à certains médicaments mais pas à d’autres. En reliant l’architecture tridimensionnelle de TRPM1 à sa capacité à transporter le calcium, l’étude fournit une base structurale pour comprendre la cécité nocturne héréditaire et pour explorer comment ce canal particulier aide nos yeux à voir dans la lumière la plus faible.
Citation: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
Mots-clés: TRPM1, canal ionique, vision nocturne, rétine, cryo-EM