Clear Sky Science · ar
البنية المجمدة TRPM1 تكشف عن بنية غير تقليدية مع نطاق غشائي مقلوب
الرؤية في الظلام
أي شخص تجوّل في غرفة مظلمة يعتمد على مجموعة دقيقة من الجزيئات في العين التي تجعل الرؤية الليلية ممكنة. أحد هذه المكونات، بروتين يُدعى TRPM1، كان مُشتبَهًا به طويلاً كونه يعمل كبوابة صغيرة في الخلايا العصبية للشبكية، يسمح لتدفق ذرات مشحونة ويحمل إشارات حول الضوء الخافت. ومع ذلك، كافح العلماء لإظهار بالضبط كيفية بناء TRPM1 وما إذا كان يعمل فعلاً كقناة أيونية مستقلة. يجمع هذا البحث بين التصوير المتقدم وتجارب الخلايا ليكشف عن بنية TRPM1 غير العادية وكيف يدعم على الأرجح الرؤية الليلية.
كيف تنتقل إشارات الرؤية الليلية
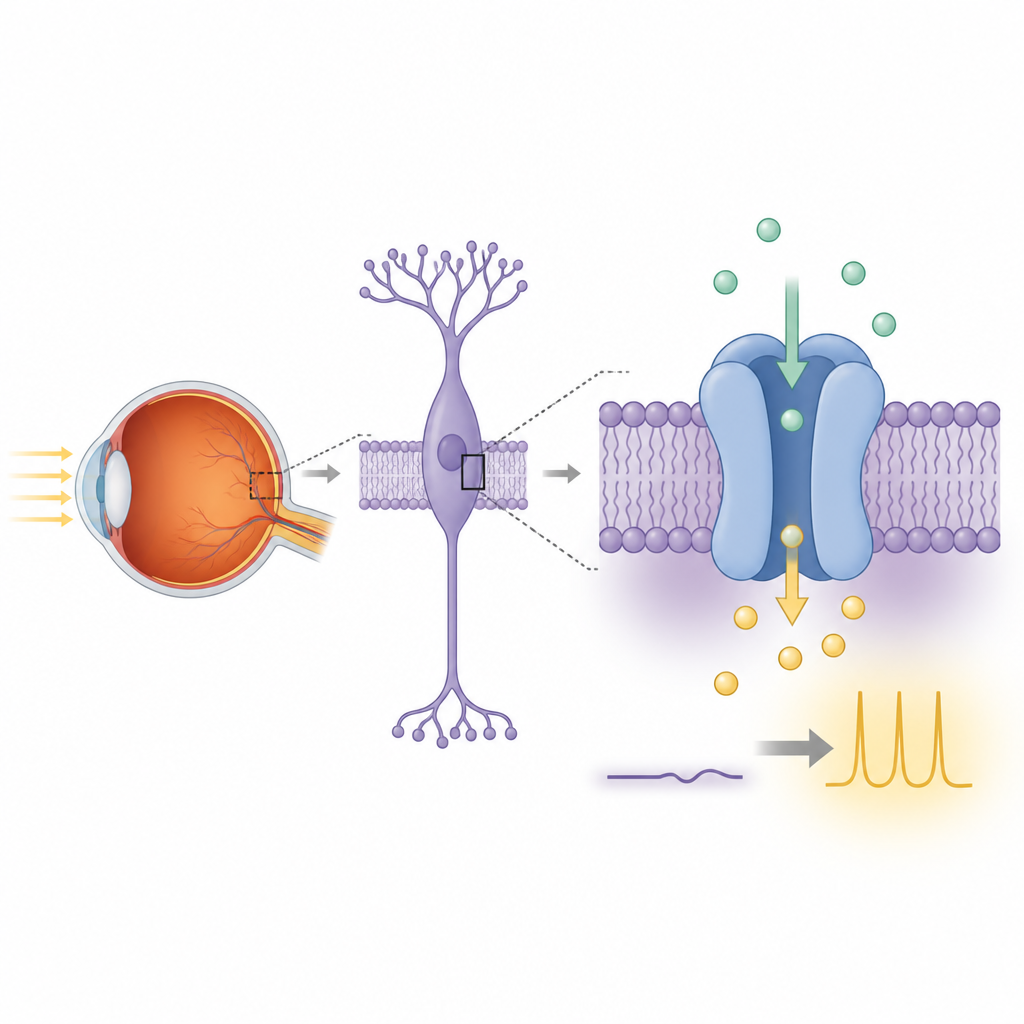
تبدأ الرؤية الليلية عندما تلتقط قضبان الخلايا الضوئية في الشبكية فوتونًا واحدًا وتنقل تلك المعلومة إلى الخلايا الثنائية القطبية المجاورة. داخل هذه الخلايا الثنائية، يربط سلسلة إشارات مستقبل الغلوتامات المسمى mGluR6 بـ TRPM1. في الضوء، يرتبط TRPM1 بتيار وارد ثابت من الأيونات موجبة الشحنة يحافظ على إزالة استقطاب هذه الخلايا. في الظلام، يؤدي تفعيل mGluR6 إلى تحرير وحدات البروتين G التي تُغلق هذا التيار، فتستعيد الخلية استقطابها وتنتهي الإشارة. عندما يتضرر TRPM1 أو شركاؤه بواسطة طفرات جينية، يفشل هذا التواصل المدفوع بالضوء وقد يصاب الناس بالعمى الليلي الخلقي الثابت الكامل، حالة تقلّ فيها القدرة على الرؤية في الإضاءة الخافتة بشدة.
اختبار ما إذا كان TRPM1 قناة حقيقية
على الرغم من تشابهه القريب مع قنوات عائلة TRPM الأخرى، ظلّ دور TRPM1 الحقيقي محور نقاش لسنوات لأن نشاطه الكهربائي صعب إعادة إنتاجه في خطوط خلايا المختبر القياسية. أنشأ المؤلفون أولاً تركيبًا لبروتين TRPM1 من الفأر مناسبًا للأعمال الهيكلية، بقص جزء ذي نهاية مرنة غير ضروري للطي. عبّروا عن TRPM1 الكامل الطول أو المقتطع في خلايا HEK293 بشرية مُهندَسة لتتوهّج عند دخول الكالسيوم. عندما أُضيف الكالسيوم خارج الخلايا، أضاءت خلايا كثيرة تعبر عن TRPM1 أكثر من خلايا الضبط، وزادت فلوريسنتها بقوة أكبر. تشير هذه الملاحظات إلى أن TRPM1 بمفرده قادر على إنشاء مسار لأيونات الكالسيوم لعبور الغشاء، مما يدعم الفكرة أنه قناة أيونية حقيقية.
شكل قناة مفاجئ
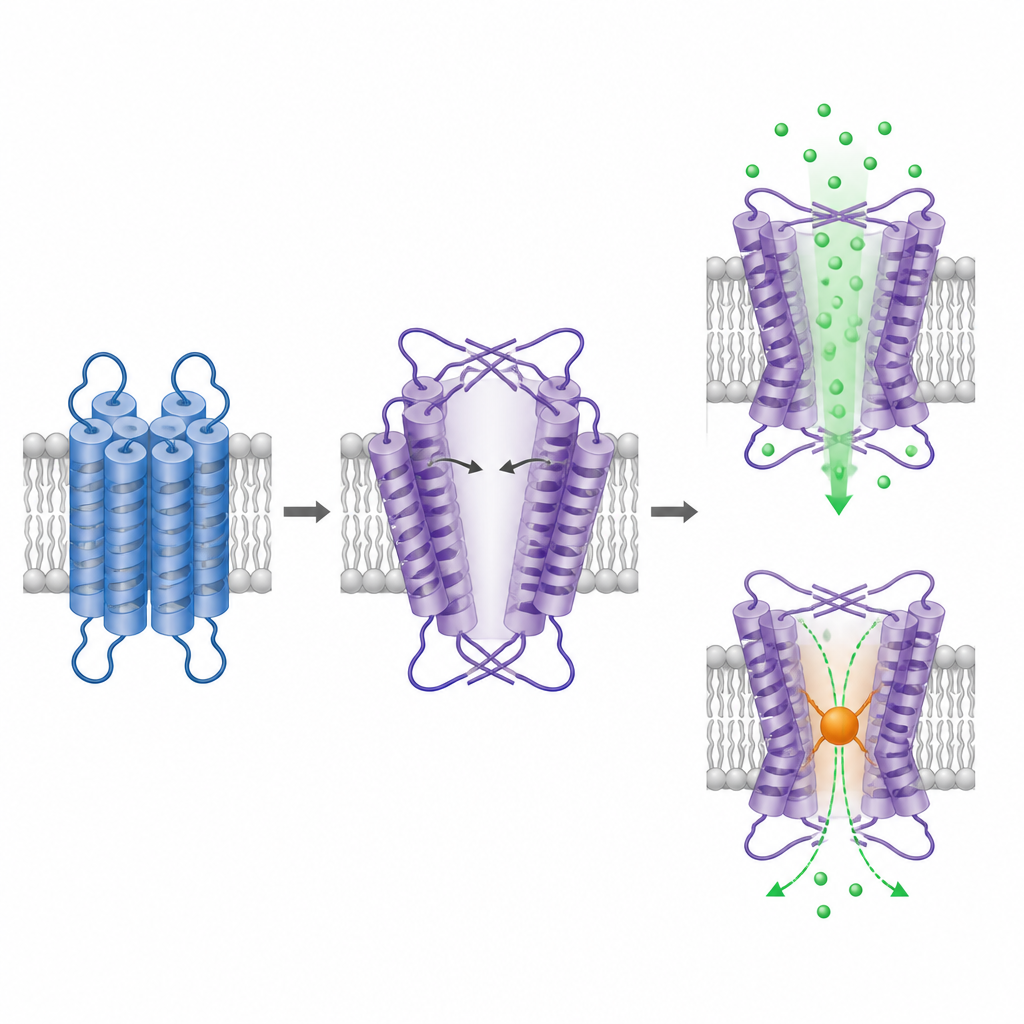
لمعرفة كيفية بناء TRPM1، نقّى الفريق البروتين المقتطع وصوّره بواسطة الميكروسكوب الإلكتروني بالتبريد، تقنية تُظهر جزيئات مفردة مجمدة في طبقة رقيقة من الجليد. يشكل الجزء داخل الخلوي من TRPM1 ترتيبًا متماثلًا رباعيًا مألوفًا مشابهًا لقنوات TRPM الأخرى، مما يعزز هويته كقناة رباعية الوحدات. المفاجأة تكمن في الجزء العابر للغشاء. هنا، تظل منطقة مشابهة لمستشعر الجهد ومنطقة المسام مرتبة بتبادل نطاقات، لكن مع يدِية معكوسة مقارنة بكل القنوات الأيونية ذات الصلة التي دُرست حتى الآن. هذا الترتيب المقلوب يجبر اثنين من حلقات المسام على الانحناء والتمدد بزوايا ضحلة، مما يخلق تجويفًا مركزيًا كبيرًا يشبه مسمارًا واسعًا ومفتوحًا.
ملاحقة الأيونات عبر المسام
يُقدَّر أن التجويف المتسع في نطاق غشاء TRPM1 لا يقل عرضه عند أضيق نقطة عن نحو نانومتر واحد، وهو مماثل لفتحات قنوات TRPM الأخرى في حالتها النشطة. يدعم هذا المقترحات السابقة بأن TRPM1 يميل لأن يكون مفتوحًا بشكل دائم. لاختبار ما إذا كان المسار المزعوم ينقل الكالسيوم فعلاً، أدخل الباحثون سيستينًا في أضيق نقطة وطبقوا مادة كيميائية تلتصق بالسيستينات المكشوفة وتضيف كتلة. خفَّض هذا المعالجة بشدة الفلورسنت المعتمد على الكالسيوم في القناة الطافرة فقط، مما يشير إلى أن حجب هذا الموضع يعيق مرور الأيونات. معًا، تشير البنية وتجربة الحجب إلى أن التجويف المرصود هو مسار الأيونات الوظيفي في TRPM1.
لمحات حول استجابات الدواء والمرض
نظرًا لقرابة TRPM1 مع TRPM3، التي وُصفت هيكليًا مع ربط جزيئات صغيرة مختلفة، قارن المؤلفون جيوب الارتباط المعروفة بين القناتين. تُحافظ مواقع في منطقة تشبه مستشعر الجهد التي تربط المنشطات والمثبطات في TRPM3 بشكل جيد في TRPM1، وبالفعل خفّض المثبط بريميدون دخول الكالسيوم المعتمد على TRPM1. في المقابل، لم يكن بإمكان ستيرويد ينشط TRPM3 عبر جيب بين المستشعر والمسَام أن يتوافق مع بنية TRPM1 المقلوبة، وفشل في تعزيز نشاط TRPM1. رسم الفريق أيضًا طفرات العمى الليلي البشري على البنية؛ يقع معظمها في مناطق تبدو أنها تُثبّت طية البروتين أو تتحكم في توجيهه للمكان المناسب داخل خلايا الشبكية.
ماذا يعني هذا للرؤية الليلية
بشكل مبسط، يُظهر هذا العمل أن TRPM1 حقًا قناة أيونية، لكنها تمتلك منطقة عابرة للغشاء مرتبة بطريقة غير متوقعة ومقلوبة تسمح مع ذلك بمسَام كبيرة لمرور الأيونات. قد تفسر هذه البنية غير العادية سبب اختلاف سلوك TRPM1 عن أقاربه واستجابته لبعض الأدوية دون غيرها. بربط الهندسة الثلاثية الأبعاد لـ TRPM1 بقدرته على نقل الكالسيوم، يوفر البحث أساسًا بنيويًا لفهم العمى الليلي الوراثي وللاستكشاف كيف تساعد هذه القناة الخاصة أعيننا على الرؤية في أخفض مستويات الضوء.
الاستشهاد: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
الكلمات المفتاحية: TRPM1, قناة أيونية, الرؤية الليلية, الشبكية, التصوير المجمد بالإلكترون