Clear Sky Science · ja
逆向きの膜横断ドメインをもつ非正統的な構造を明らかにしたTRPM1のクライオEM構造
暗闇で見ること
暗い部屋でつまずいたことのある人は誰でも、夜間視覚を可能にする眼の繊細な分子群に頼っている。その一つであるTRPM1というタンパク質は、網膜の神経細胞において微小な門として働き、電荷を帯びた原子(イオン)を通して薄明かりの情報を伝えると長く考えられてきた。しかし、TRPM1がどのように構築され、独立したイオンチャネルとして本当に機能するかを正確に示すことは科学者たちにとって困難であった。本研究は高度なイメージングと細胞実験を組み合わせ、TRPM1の異例の構造とそれが夜間視にどのように寄与するかを明らかにする。
夜間視の信号の伝わり方
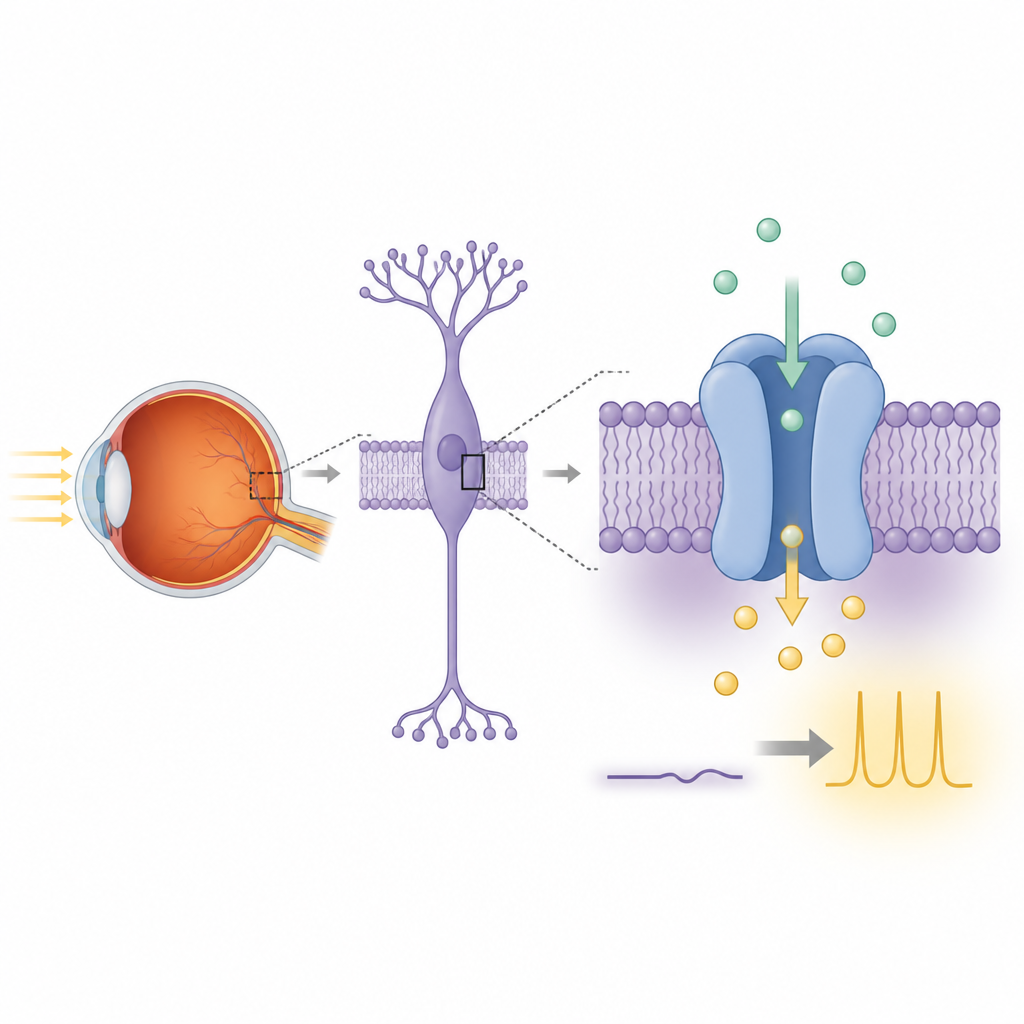
夜間視は、網膜の杆体(ロッド)光受容体が単一光子を検出し、その情報を近傍の双極細胞に伝えることから始まる。双極細胞内部では、mGluR6と呼ばれるグルタミン酸受容体がTRPM1へとつながるシグナル連鎖を形成する。明るいとき、TRPM1は内部へ向かう陽イオンの安定した流れに関与し、これによりこれらの細胞は脱分極状態を維持する。暗いときにはmGluR6の活性化によってGタンパク質サブユニットが放出され、この流れが遮断されて細胞は再分極し、信号が終了する。TRPM1やその連携因子が遺伝子変異で障害されると、この光に基づく情報伝達が失われ、先天性の定常性完全夜盲という、薄明かりでの視力が著しく低下する状態が生じる。
TRPM1が本当のチャネルかを検証する
TRPM1は他のTRPMファミリーのイオンチャネルに非常に類似しているにもかかわらず、標準的な培養細胞株では電気的活動を再現しにくいため、その真の機能は長年議論されてきた。著者らはまず構造研究に適したラットTRPM1コンストラクトを作製し、折りたたみに不要な柔らかい末端領域を切り詰めた。全長あるいはトランケートしたTRPM1を、カルシウム流入時に蛍光を発するよう改変したヒトHEK293細胞に発現させたところ、細胞外にカルシウムを加えるとTRPM1を発現した細胞の方が対照細胞よりはるかに多く発光し、蛍光増強も大きかった。これらの観察は、TRPM1単独で膜を横切るカルシウムイオンの通路を形成し得ることを示し、真のイオンチャネルであるという考えを支持する。
驚くべきチャネルの形状
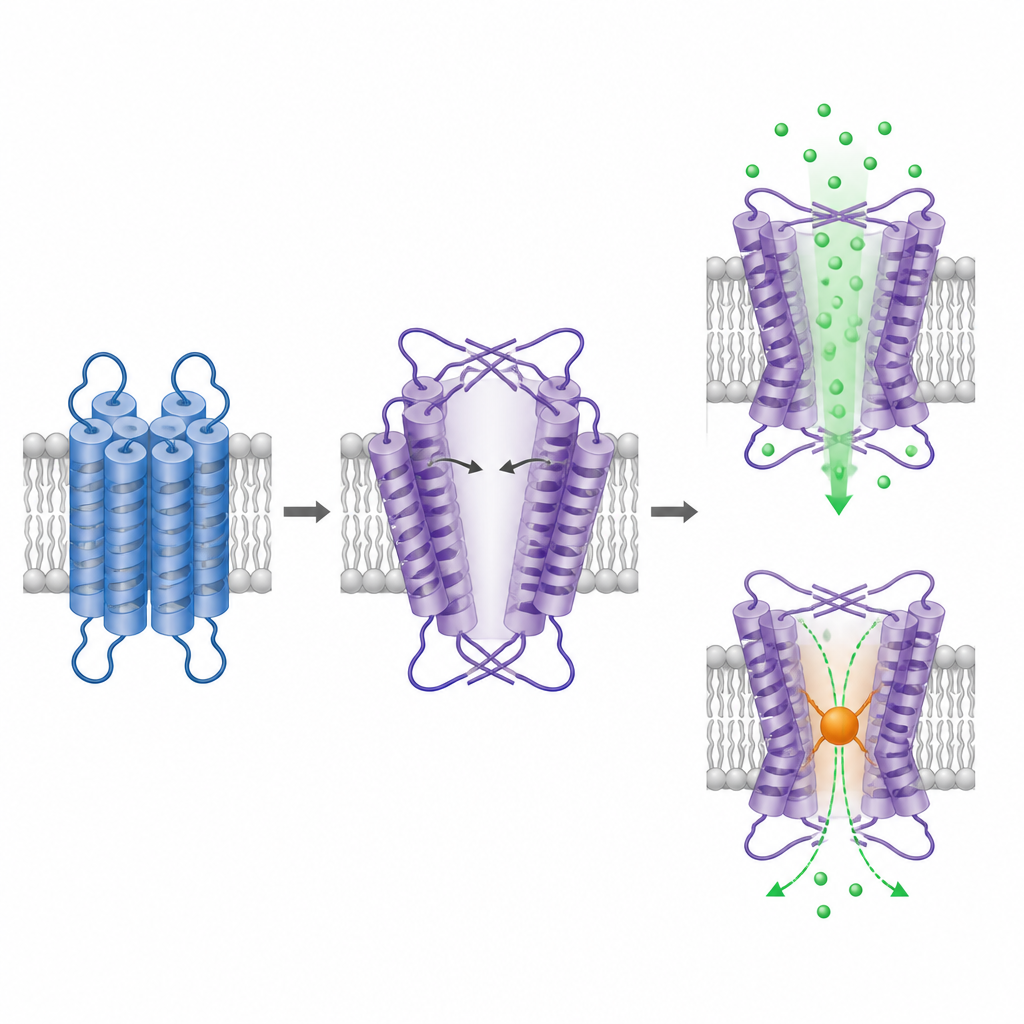
TRPM1の構造を明らかにするため、研究チームはトランケートしたタンパク質を精製し、クライオ電子顕微鏡で単一粒子を薄い氷層で凍結して観察した。細胞内側の部分は他のTRPMチャネルに似た四回対称の配置を取り、四量体チャネルであることを補強した。驚きは膜を貫く部分にあった。ここでは電位センサー様領域と孔領域がドメインスワップした配置を維持しているが、これまでに研究された関連イオンチャネルとは逆の手性を示していた。この逆向きの配置は、二つの孔ヘリックスが浅い角度で曲がり伸びることを余儀なくされ、大きな中央空洞、すなわち広く開いた孔に似た構造を生み出している。
孔を通るイオンの追跡
TRPM1の膜領域にある拡大された空洞は、最も狭い点で少なくとも約1ナノメートル程度と推定され、活性状態にある他のTRPMチャネルの開口部と同程度である。これはTRPM1が恒常的に開いている傾向があるという以前の示唆を支持する。仮想的な孔が本当にカルシウムを通すかを試すため、研究者らは狭窄点にシステインを人工導入し、露出したシステインに付着して容積を増す化学試薬を適用した。この処置は変異チャネルにおいてのみカルシウム依存性蛍光を強く抑制し、該当位置の遮断がイオン透過を妨げることを示した。構造と遮断実験を総合すると、観察された空洞がTRPM1における機能的なイオン経路であると主張できる。
薬物反応と疾患への手がかり
TRPM1はTRPM3と密接に関連しており、TRPM3は様々な低分子リガンドとともに構造解析されているため、著者らは両チャネル間の既知の結合ポケットを比較した。活性化剤や阻害剤が結合する電位センサー様領域の部位はTRPM1でもよく保存されており、阻害剤プリミドンは実際にTRPM1依存のカルシウム流入を抑えた。対照的に、センサーと孔の間のポケットでTRPM3を活性化するステロイドは、TRPM1の逆向き構造には収まらず、TRPM1活性を増強することができなかった。チームはまたヒトの夜盲変異を構造上にマッピングしたところ、ほとんどがタンパク質の折りたたみを安定化する領域や網膜細胞内で適切な局在へ輸送する制御領域に位置していた。
夜間視に対する意義
平たく言えば、本研究はTRPM1が確かにイオンチャネルであることを示しているが、その膜貫通領域は予想外の逆向き配列で配置され、それでもイオンが通る大きな孔を提供していることを示す。こうした異例の形状は、TRPM1が近縁チャネルとは異なる振る舞いを示し、一部の薬剤には応答しても他には応答しない理由を説明するかもしれない。TRPM1の三次元構造をカルシウムを通す能力に結びつけることで、この研究は遺伝性夜盲の理解と、この特殊なチャネルが極めて暗い光の中で我々の眼がどのように視るのを助けるかを探るための構造的基盤を提供する。」}
引用: Fabrizio, M., Brewer, M., Bogdanović, N. et al. Cryo-EM structure of TRPM1 reveals a non-canonical architecture with an inverted transmembrane domain. Nat Commun 17, 4260 (2026). https://doi.org/10.1038/s41467-026-70722-7
キーワード: TRPM1, イオンチャネル, 暗所視, 網膜, クライオEM