Clear Sky Science · tr
PHIP, SWI/SNF-mutant kanserlerin büyümesini sağlamak için NuRD’u baskılıyor
Bu çalışma kanser için neden önemli
Kanserler sıklıkla genleri açıp kapayan hücresel mekanizmalar bozulduğunda ortaya çıkar. Bu makale, PHIP adındaki daha az bilinen bir proteinin bazı yüksek agresif çocukluk ve over kanserlerinin hayatta kalmasına nasıl yardımcı olduğunu ve PHIP’in bloke edilmesinin şu anda az seçenek bulunan tümörleri seçici şekilde tedavi etmek için neden yeni bir yol olabileceğini inceliyor.
DNA düzeni üzerindeki çekişme
Hücrelerimizde DNA, kromatin oluşturmak için protein makaralara sarılır; büyük moleküler makineler bu yapıyı sürekli itip çekerek genleri açar veya kapatır. “Açan” ana makinelerden biri, kimyasal enerji kullanarak DNA’yı gevşeten ve gen aktivitesine izin veren SWI/SNF kompleksidir. “Kapatan” tarafta ise kromatini sıkılaştıran ve gen ekspresyonunu destekleyen kimyasal işaretleri kaldıran NuRD gibi kompleksler bulunur. Yaklaşık kanserlerin %20’sinde, nadir ama ölümcül rabdoid tümörler ve ilişkili over kanserleri de dahil olmak üzere, SWI/SNF’in çekirdek bileşenleri kaybolur ve bu dengeyi genleri aktifleştiren taraf lehine ciddi şekilde zayıflatır.
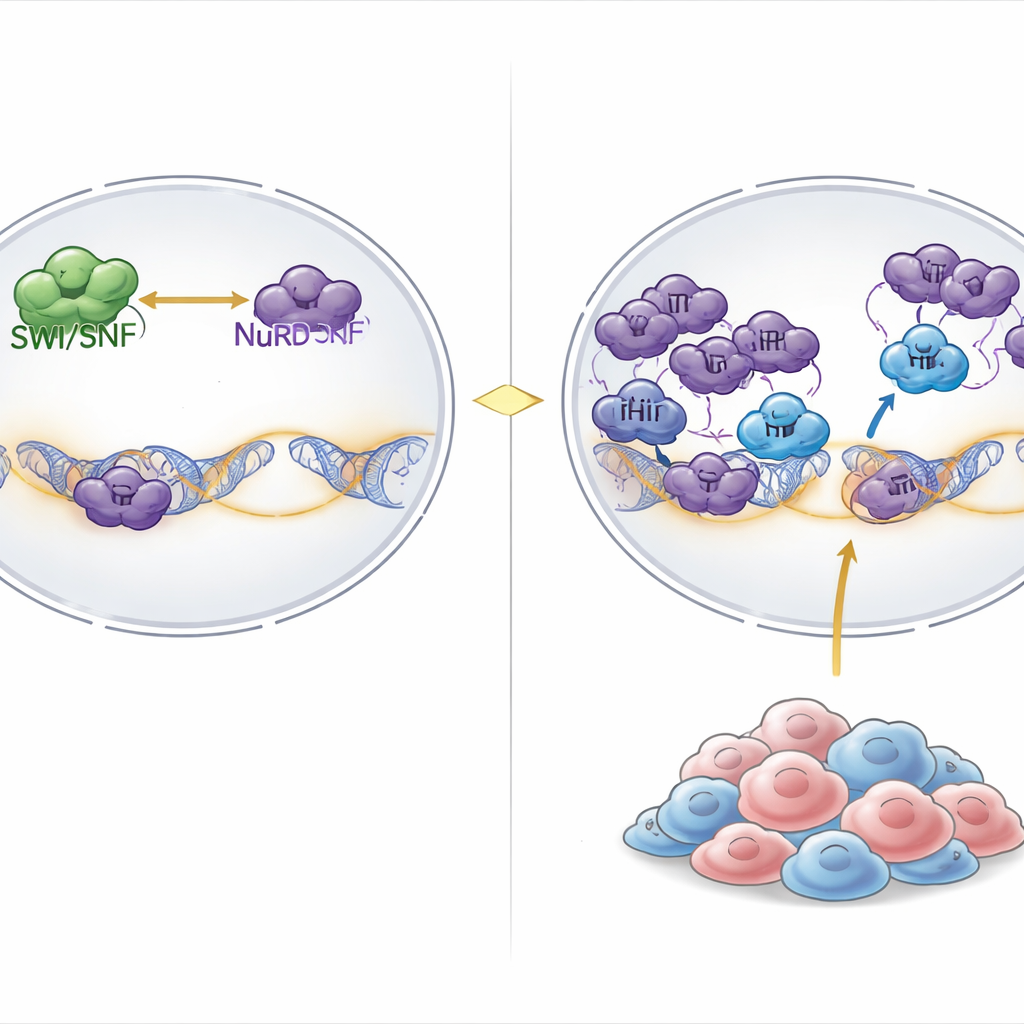
SWI/SNF-mutant tümörlerde gizli bir zayıflık bulmak
Araştırmacılar, binden fazla kanser hücre hattında yapılan genom çapında CRISPR gen yok etme taramalarının sonuçlarını taradı. Geniş SWI/SNF bozukluğuna sahip kanserlerde hangi genlerin özgün olarak vazgeçilmez olduğunu sordular. Öne çıkan unsur PHIP oldu; daha önce DNA replikasyonuyla ilişkilendirilmiş, ancak gen kontrolüne açıkça bağlanmamış bir kromatin-bağlayıcı proteindi. PHIP devre dışı bırakıldığında, SWI/SNF-mutant rabdoid ve over kanser hücrelerinin büyümesi keskin şekilde azaldı; oysa çoğu diğer kanser tipi PHIP kaybını tolere etti. Normalde dirençli hücrelere SWI/SNF kusurları eklemek, bu hücreleri PHIP kaybına karşı yeni duyarlı hale getirdi; bu da PHIP bağımlılığının doku türünden ziyade SWI/SNF işlev kaybının doğrudan bir sonucusu olduğunu gösterdi.
PHIP büyüme genlerini nasıl açık tutar
PHIP’in ne yaptığını anlamak için ekip, PHIP’in kromatinde nerede bulunduğunu ve PHIP düzeyleri değiştiğinde gen aktivitesinin nasıl etkilendiğini haritaladı. PHIP, kimyasal olarak zaten aktif işaretlenmiş gen başlangıç bölgelerinin yakınında kümelendi. PHIP azaltıldığında, özellikle hücre bölünmesini yönlendirenler olmak üzere, bu genlerin birçoğu aşağı çekildi; PHIP artırıldığında tam tersi görüldü. PHIP ayrıca bu promotörlerde histon proteinleri üzerinde belirli asetil işaretlerinin korunmasında kritik bulundu—bunlar açık, transkripsiyona uygun kromatin durumunu gösteren kimyasal bayraklardır. PHIP olmadan asetilasyon azaldı ve ilgili genler sustu; bu durum PHIP’in aktif gen bölgelerinin yerel bir koruyucusu gibi davrandığıyla uyumluydu.
PHIP, baskılayıcı bir kompleks için bir kapıcı rolünde
PHIP’in kendi enzim aktivitesi yok, bu yüzden yazarlar bunun diğer faktörleri çağırarak çalışıp çalışmadığını sordular. PHIP’in kromatine CRL4 adlı bir ubiquitin ligazı enzim topluluğunu getirdiğini buldular. Bu ligaz, hedef proteinlere küçük ubiquitin etiketleri takar; bu genellikle onların davranışını veya yerlerini değiştirir. Kütle spektrometrisi ve biyokimyasal testler, PHIP–CRL4’ün doğrudan NuRD kompleksinin kilit parçalarını, özellikle CHD4 yeniden şekillendirme altbirimini etiketlediğini ortaya koydu. Kanser hücrelerinde, CRL4’ün NuRD ile DNA üzerinde etkileşime girebilmesi PHIP’e bağlıydı; bu NuRD’un ubiquitinlenmesine ve promotörlerden uzaklaştırılmasına yol açtı. PHIP kaybolduğunda NuRD gen başlangıç bölgelerinde birikti, lokal asetil işaretleri düştü ve yakınlardaki genler sustu. Önemli olarak, CHD4’ün azaltılması, PHIP inaktivasyonunun neden olduğu asetilasyon kaybını tersine çevirebildi; bu etkiyi NuRD’un yeniden şekillendirme aktivitesine bağladı.
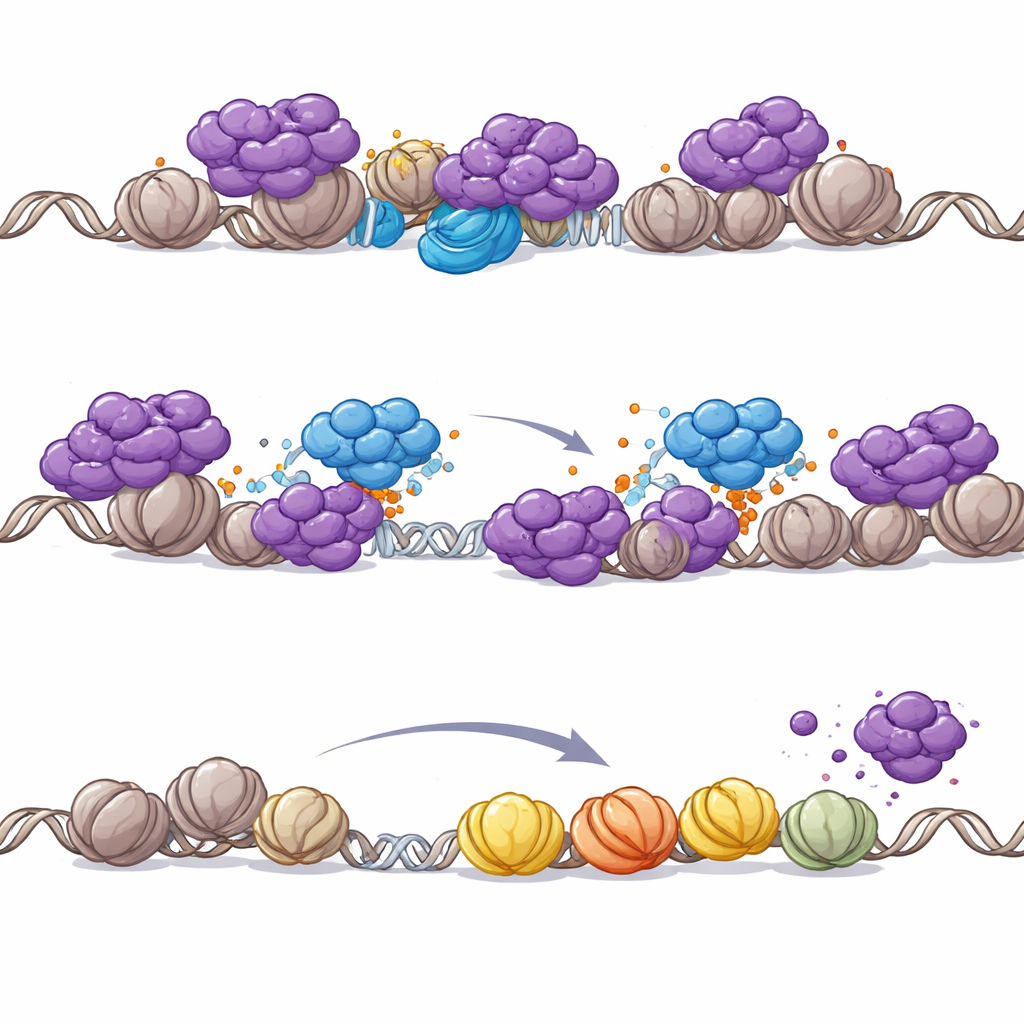
SWI/SNF bozulduğunda PHIP neden kritik hale geliyor
Ardından ekip, bu PHIP–NuRD etkileşiminin neden özellikle SWI/SNF-mutant kanserlerde bu kadar önemli olduğunu araştırdı. Rabdoid tümör hücrelerinde eksik bir SWI/SNF altbirimini geri vermek, NuRD’un genomdaki yerleşimini yeniden şekillendirdi: NuRD promotörlerden uzaklaşarak SWI/SNF tarafından yeniden etkinleştirilen enhancer bölgelerine kaydı. Ancak SWI/SNF yok olduğunda NuRD promotörlere yeniden dağıldı ve hayatta kalmak için gerekli genlerin yaygın bir şekilde kapanma tehdidiyle karşılaştı. Bu savunmasız durumda, NuRD’un PHIP aracılığıyla uzaklaştırılması promotör kaynaklı gen ekspresyonunu canlı tutmak için elzem hale geldi. Aksi takdirde normal hücrelerde bile, SWI/SNF’in çekirdek motorlarını kimyasal olarak degrade etmek, kromatinden NuRD’un PHIP’e bağımlı uzaklaştırılmasını tetiklemek için yeterliydi; bu da PHIP’in rolünün SWI/SNF kaybıyla sıkı bağlantılı olduğunu güçlendirdi.
Laboratuvar kaplarından hasta kaynaklı tümörlere
Çalışmanın hücre hatlarının ötesinde geçerliliğini test etmek için araştırmacılar hasta kaynaklı beyin tümörü organoidleri ve rabdoid tümörlerin fare modellerine yöneldi. Çocukların SWI/SNF kusurlarına sahip kanserlerinden elde edilen üç boyutlu tümör kültürlerinde PHIP’in bozulması tümör hücrelerinin dayanıklılığını belirgin şekilde azalttı; SWI/SNF mutasyonlarından yoksun ilişkili bir beyin kanserinden türetilen organoidler büyük ölçüde etkilenmedi. PHIP devre dışı bırakılmış organoidler fare beyinlerine nakledildiğinde, hayvanlar kontrol tümörlerine sahip olanlara göre çok daha uzun yaşadı. PHIP knockout grubunda sonunda nükseden tümörler kısmen geri kazanılmış PHIP düzeylerine sahipti; bu da PHIP kaybından kaçabilen kanser hücrelerinin yeniden büyüyebilenler olduğunu gösterdi.
Gelecekteki kanser tedavileri için anlamı
Bu çalışma, SWI/SNF’in alışılmış aktifleştirici gücü zayıfladığında gen aktivitesini koruyan moleküler bir “gözcü” olarak PHIP’i ortaya koyuyor. Kritik promotörlerden baskılayıcı NuRD kompleksini uzaklaştırmak için bir etiketleme enzimini işe alarak, PHIP SWI/SNF-mutant tümörlerin temel büyüme genlerini açık tutmasına olanak sağlar. Çoğu diğer kanser tipi—ve muhtemelen birçok normal hücre—PHIP’e bu kadar bağımlı olmadığından, benzersiz bağlanma cebini hedefleyen ilaçlar teoride rabdoid ve ilişkili tümörlere sağlıklı dokulardan çok daha fazla zarar verebilir. Bu tür tedaviler henüz geliştirilip klinik olarak test edilmemiş olsa da çalışma, bazı en zorlu SWI/SNF-mutant kanserlere karşı PHIP’i hedeflemenin açık bir mekanistik gerekçesini haritalandırıyor.
Atıf: Malone, H.A., Myers, J.A., Gruss, E.G. et al. PHIP suppresses NuRD to enable the growth of SWI/SNF-mutant cancers. Nat Commun 17, 2877 (2026). https://doi.org/10.1038/s41467-026-70699-3
Anahtar kelimeler: epigenetik kanser tedavisi, SWI/SNF mutasyonları, NuRD kompleksi, kromatin yeniden şekillendirme, rabdoid tümörler