Clear Sky Science · pt
PHIP suprime o NuRD para permitir o crescimento de cânceres com mutação no SWI/SNF
Por que este estudo importa para o câncer
Os cânceres frequentemente surgem quando a maquinaria celular que liga e desliga genes fica desregulada. Este artigo investiga como uma proteína pouco conhecida chamada PHIP ajuda certos cânceres infantis e ovarianos altamente agressivos a sobreviver, e por que bloquear a PHIP pode oferecer uma nova forma seletiva de tratar tumores que atualmente têm poucas opções eficazes.
A disputa pelo roteiro do DNA
No interior de nossas células, o DNA está enrolado em torno de carretéis proteicos formando a cromatina, e grandes máquinas moleculares constantemente deslocam essa estrutura para abrir genes para uso ou fechá-los. Uma das principais máquinas de “abertura” é o complexo SWI/SNF, que usa energia química para afrouxar o DNA e permitir a atividade gênica. No lado do “fechamento” estão complexos como o NuRD, que compactam a cromatina e removem marcas químicas que favorecem a expressão gênica. Em cerca de 20% dos cânceres, incluindo tumores raros mas letais chamados tumores rabdoides e cânceres ovarianos relacionados, componentes centrais do SWI/SNF são perdidos, enfraquecendo severamente o lado ativador desse equilíbrio.
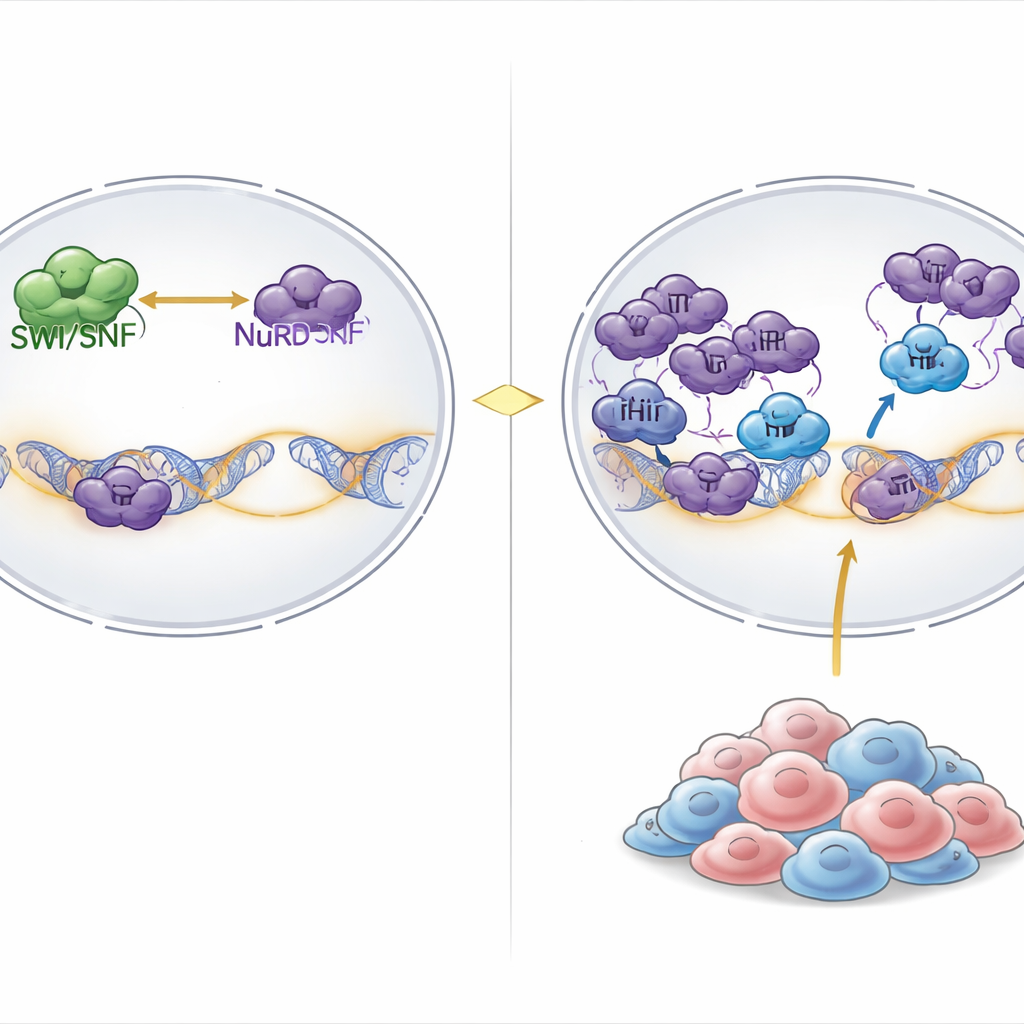
Encontrando uma fraqueza oculta em tumores com mutação no SWI/SNF
Os pesquisadores vasculharam resultados de rastreios CRISPR de perda de genes em escala genômica em mais de mil linhagens celulares de câncer. Perguntaram quais genes eram exclusivamente essenciais em cânceres com ampla disrupção do SWI/SNF. Um achado de destaque foi PHIP, uma proteína que se liga à cromatina previamente associada à replicação do DNA, mas não claramente ligada ao controle gênico. Quando a PHIP foi desativada, o crescimento de células de câncer rabdoide e ovariano com mutações no SWI/SNF caiu drasticamente, enquanto a maioria de outros tipos de câncer tolerou a perda de PHIP. Introduzir defeitos no SWI/SNF em células normalmente resistentes as tornou sensíveis à perda de PHIP, mostrando que a dependência por PHIP é uma consequência direta da falha do SWI/SNF e não do tipo de tecido.
Como a PHIP mantém genes de crescimento ativados
Para entender o que a PHIP faz, a equipe mapeou onde ela se posiciona na cromatina e como a atividade gênica muda quando os níveis de PHIP sobem ou caem. A PHIP se concentrou perto de sítios de início de genes que já tinham marcas químicas associadas à atividade. Reduzir a PHIP fez muitos desses genes serem reprimidos, especialmente aqueles que impulsionam a divisão celular, enquanto aumentar a PHIP teve o efeito oposto. A PHIP também se mostrou crucial para manter marcas específicas de acetila em histonas — sinais químicos que indicam um estado de cromatina aberto e favorável à transcrição — nesses promotores. Sem PHIP, a acetilação desapareceu e os genes correspondentes silenciaram, consistente com a PHIP atuando como um guardião local de regiões gênicas ativas.
PHIP como um segurança para um complexo repressivo
A PHIP não possui atividade enzimática própria, então os autores investigaram se ela funciona recrutando outros fatores. Descobriram que a PHIP traz um conjunto enzimático chamado ligase de ubiquitina CRL4 para a cromatina. Essa ligase anexa pequenas etiquetas de ubiquitina a proteínas-alvo, muitas vezes alterando seu comportamento ou localização. Espectrometria de massa e testes bioquímicos revelaram que o complexo PHIP–CRL4 marca diretamente partes-chave do complexo NuRD, particularmente a subunidade remodeladora CHD4. Em células cancerosas, a PHIP foi necessária para que o CRL4 interagisse com o NuRD no DNA, levando à ubiquitinação do NuRD e à sua remoção dos promotores. Quando a PHIP foi perdida, o NuRD se acumulou nos sítios de início dos genes, as marcas locais de acetilação caíram e genes próximos foram silenciados. Importante, reduzir CHD4 pôde reverter a perda de acetilação causada pela inativação da PHIP, atribuindo o efeito à atividade remodeladora do NuRD.
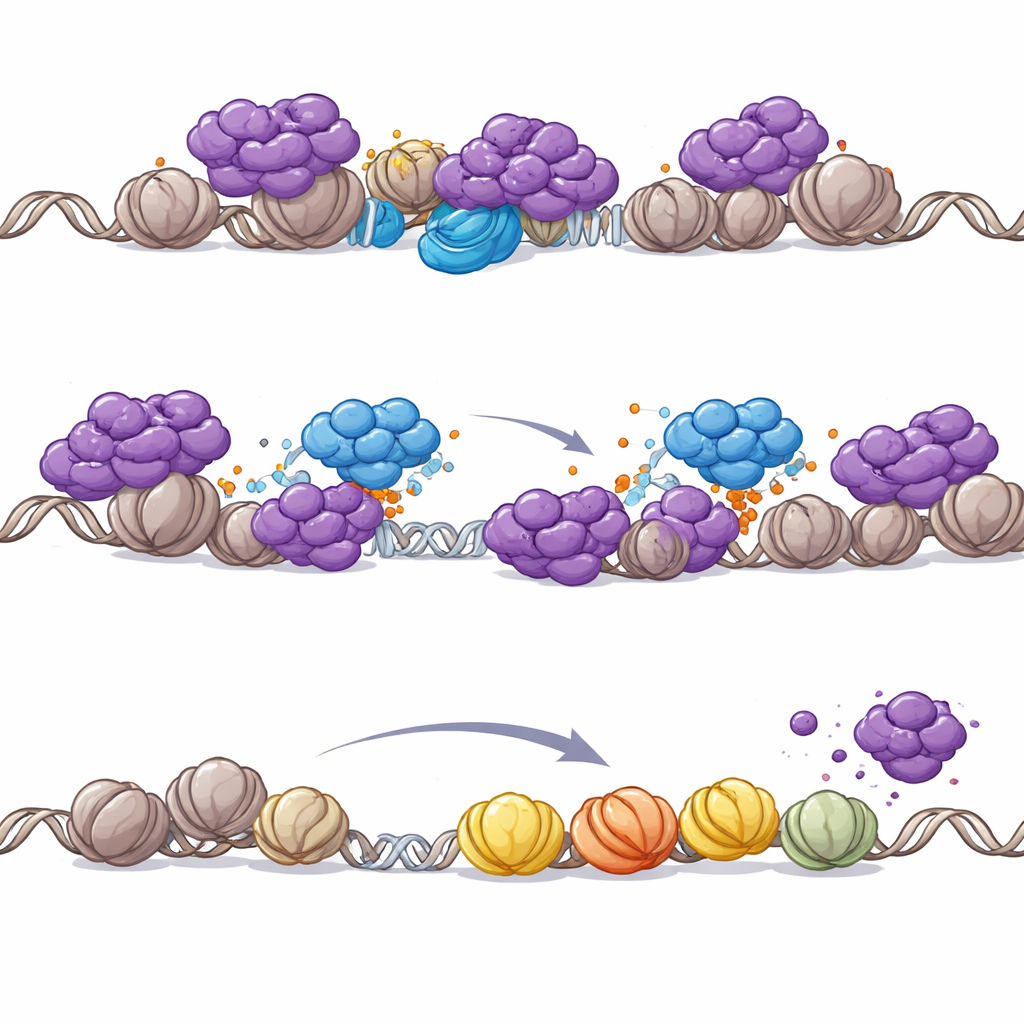
Por que a PHIP se torna crítica quando o SWI/SNF está quebrado
A equipe então explorou por que essa interação PHIP–NuRD é tão importante especificamente em cânceres com mutação no SWI/SNF. Restaurar uma subunidade ausente do SWI/SNF em células de tumor rabdoide remodelou a distribuição do NuRD no genoma: o NuRD se deslocou para longe dos promotores e em direção a regiões enhancers que foram reativadas pelo SWI/SNF. Quando o SWI/SNF está ausente, porém, o NuRD se redistribui para promotores, ameaçando um desligamento generalizado de genes necessários para a sobrevivência. Nesse cenário vulnerável, a expulsão do NuRD mediada pela PHIP torna-se essencial para manter a expressão gênica dependente de promotores. Mesmo em células normais, degradar quimicamente os motores centrais do SWI/SNF foi suficiente para desencadear a remoção de NuRD dependente de PHIP da cromatina, reforçando que o papel da PHIP está intimamente ligado à perda do SWI/SNF.
Dos pratos de laboratório a tumores derivados de pacientes
Para testar a relevância além de linhagens celulares, os pesquisadores recorreram a organoides de tumores cerebrais derivados de pacientes e modelos em camundongos de tumores rabdoides. Em culturas tumorais tridimensionais crescidas a partir de cânceres infantis com defeitos no SWI/SNF, a interrupção da PHIP reduziu marcadamente a aptidão das células tumorais, enquanto organoides de um câncer cerebral relacionado sem mutações no SWI/SNF foram amplamente indiferentes. Quando organoides com PHIP nocaute foram implantados nos cérebros de camundongos, os animais viveram muito mais do que aqueles com tumores controle. Tumores que eventualmente recidivaram no grupo com nocaute de PHIP apresentaram níveis de PHIP parcialmente restaurados, indicando que células cancerosas que escaparam da perda de PHIP foram as capazes de crescer novamente.
O que isso significa para tratamentos futuros do câncer
Este trabalho revela a PHIP como um “guarda-costas” molecular que protege a atividade gênica em cânceres onde o poder ativador habitual do SWI/SNF está comprometido. Ao recrutar uma enzima de marcação para expulsar o complexo repressivo NuRD de promotores críticos, a PHIP permite que tumores com mutação no SWI/SNF mantenham ligados genes essenciais ao crescimento. Como a maioria dos outros tipos de câncer — e presumivelmente muitas células normais — não depende tanto da PHIP, drogas que inibam seu bolso de ligação único poderiam, em princípio, atingir tumores rabdoides e relacionados de forma muito mais seletiva que o tecido saudável. Embora tais tratamentos ainda precisem ser desenvolvidos e testados clinicamente, o estudo traça uma justificativa mecanística clara para direcionar a PHIP como nova estratégia contra alguns dos cânceres com mutações no SWI/SNF mais desafiadores.
Citação: Malone, H.A., Myers, J.A., Gruss, E.G. et al. PHIP suppresses NuRD to enable the growth of SWI/SNF-mutant cancers. Nat Commun 17, 2877 (2026). https://doi.org/10.1038/s41467-026-70699-3
Palavras-chave: terapia epigenética contra o câncer, mutações no SWI/SNF, complexo NuRD, remodelamento da cromatina, tumores rabdoides