Clear Sky Science · sv
PHIP undertrycker NuRD för att möjliggöra tillväxt av SWI/SNF-mutanta cancerformer
Varför den här studien är viktig för cancer
Cancer uppstår ofta när cellens maskineri som slår av och på gener kommer i obalans. Denna artikel undersöker hur ett mindre känt protein kallat PHIP hjälper vissa mycket aggressiva barnoch äggstockscancerformer att överleva, och varför blockering av PHIP kan erbjuda ett nytt, selektivt sätt att behandla tumörer som i dag har få bra behandlingsalternativ.
Dragspelet om DNA-manuset
I våra celler är DNA lindat runt proteiner för att bilda kromatin, och stora molekylära maskiner skjuter ständigt på denna struktur för att antingen öppna gener för användning eller stänga ner dem. Ett stort ”öppnings”-maskineri är SWI/SNF-komplexet, som använder kemisk energi för att luckra upp DNA och möjliggöra genaktivitet. På ”stänga”-sidan finns komplex som NuRD, som förtätar kromatin och tar bort kemiska markörer som gynnar genuttryck. I ungefär 20 % av cancrar, inklusive sällsynta men dödliga tumörer kallade rhabdoida tumörer och närliggande äggstockscancerformer, förloras kärnkomponenter av SWI/SNF, vilket kraftigt försvagar den genaktiverande sidan av denna balans.
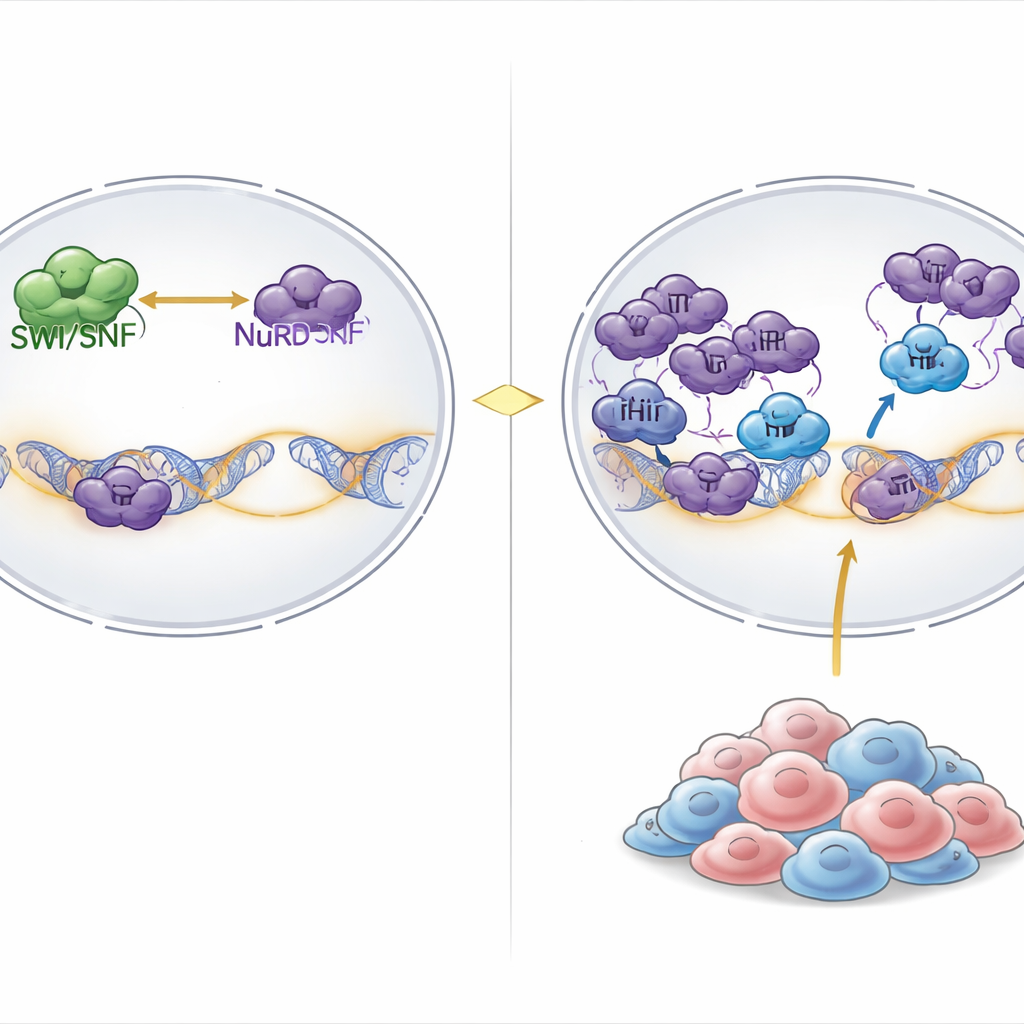
Att hitta en dold svaghet i SWI/SNF-mutanta tumörer
Forskarna gick igenom resultat från genommätande CRISPR-knockout-skärmar i mer än tusen cancercellinjer. De frågade vilka gener som var unikt nödvändiga i cancerformer med omfattande SWI/SNF-störning. Ett framstående fynd var PHIP, ett kromatinbindande protein tidigare kopplat till DNA-replikation men inte tydligt till genreglering. När PHIP stängdes av minskade tillväxten i SWI/SNF-mutanta rhabdoida och äggstockscellinjer kraftigt, medan de flesta andra cancerformer tål förlust av PHIP. Att introducera SWI/SNF-defekter i normalt motståndskraftiga celler gjorde dem nykänsliga för PHIP-förlust, vilket visar att beroendet av PHIP är en direkt följd av SWI/SNF-fel och inte av vävnadstyp.
Hur PHIP håller tillväxtgenerna påslagna
För att förstå vad PHIP gör kartlade teamet var det binder på kromatin och hur genaktiviteten förändras när PHIP-nivåer sjunker eller stiger. PHIP klustrade nära genstartplatser som redan var kemiskt märkta som aktiva. Att reducera PHIP ledde till att många av dessa gener nedreglerades, särskilt de som driver celldelning, medan ökad PHIP gav motsatt effekt. PHIP visade sig också vara avgörande för att bibehålla specifika acetylmarkörer på histonproteiner—kemiska flaggor som signalerar ett öppet, transkriptionsvänligt kromatinläge—vid dessa promotorer. Utan PHIP försvann acetyleringen och de berörda generna tystnade, vilket stämmer med att PHIP fungerar som en lokal väktare av aktiva genregioner.
PHIP som vakthund mot ett repressivt komplex
PHIP saknar egen enzymatisk aktivitet, så författarna undersökte om det verkar genom att rekrytera andra faktorer. De fann att PHIP tar med sig ett enzymkomplex kallat CRL4 ubiquitin-ligas till kromatin. Denna ligas fäster små ubiquitin-taggar på målcproteiner, vilket ofta förändrar deras funktion eller lokalisering. Masspektrometri och biokemiska tester visade att PHIP–CRL4 direkt märker nyckeldelar av NuRD-komplexet, särskilt remodeleringssubenheten CHD4. I cancerceller krävdes PHIP för att CRL4 skulle interagera med NuRD på DNA, vilket ledde till NuRD-ubikvitinering och dess borttagning från promotorer. När PHIP förlorades samlades NuRD på genstartplatser, lokala acetylmarkörer minskade och närliggande gener tystnade. Viktigt är att nedreglering av CHD4 kunde återställa acetyleringen som förlorades vid PHIP-inaktivering, vilket pekar på att effekten härleds till NuRD:s remodeleringsaktivitet.
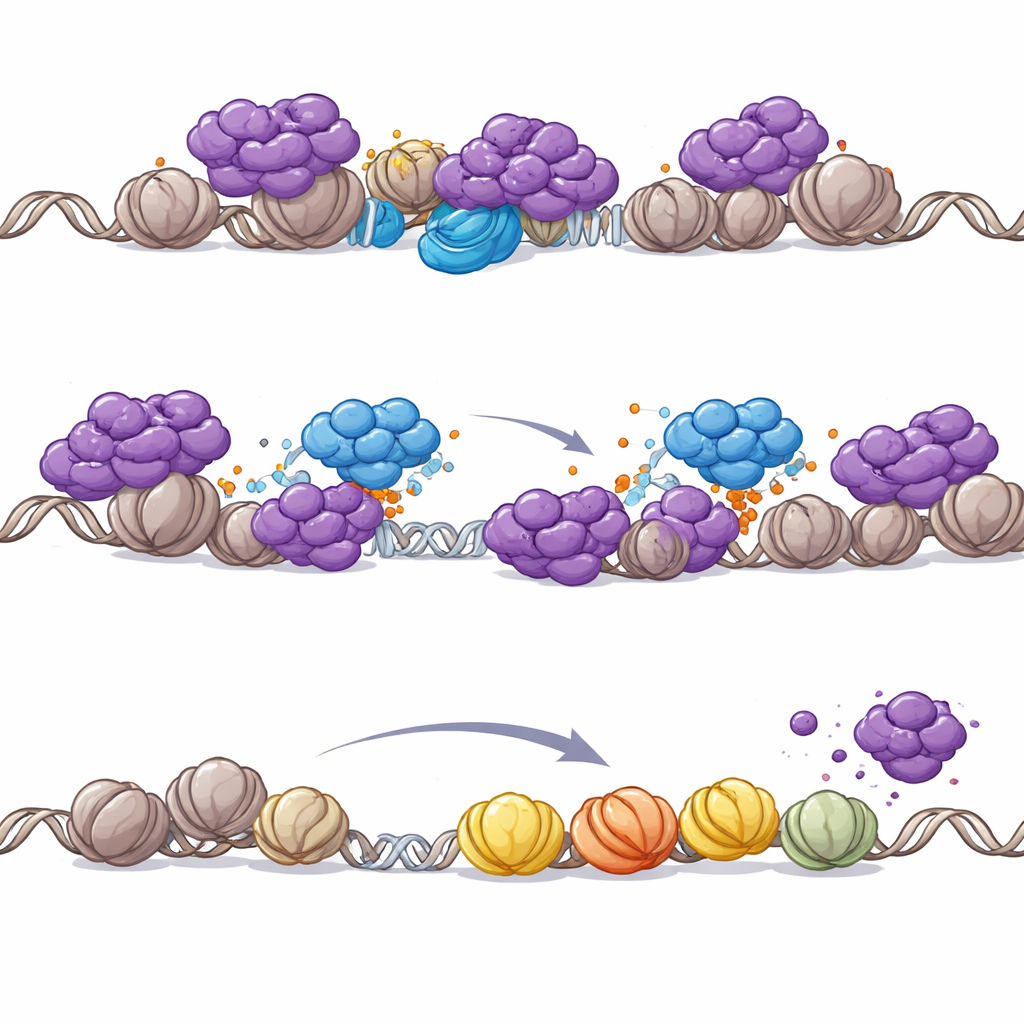
Varför PHIP blir kritiskt när SWI/SNF är skadat
Teamet undersökte sedan varför PHIP–NuRD-interaktionen är så viktig särskilt i SWI/SNF-mutanta cancerformer. Återställande av en saknad SWI/SNF-subenhet i rhabdoida tumörceller omformade var NuRD sitter i genomet: NuRD förflyttade sig bort från promotorer och mot förstärkarregioner som återaktiverades av SWI/SNF. När SWI/SNF saknas omdistribueras dock NuRD till promotorer och hotar att stänga ner gener som behövs för överlevnad. I detta sårbara läge blir PHIP-medierad utkastning av NuRD nödvändig för att hålla promotorstyrt genuttryck vid liv. Även i i övrigt normala celler var kemisk degradering av SWI/SNF:s kärnkomponenter tillräcklig för att utlösa PHIP-beroende borttagning av NuRD från kromatin, vilket stärker att PHIP:s roll är tätt kopplad till SWI/SNF-förlust.
Från odlingsskålar till patienthärledda tumörer
För att testa relevansen bortom cellinjer vände forskarna sig till patienthärledda hjärntumörorganoider och musmodeller av rhabdoida tumörer. I tredimensionella tumörkulturer odlade från barncancer med SWI/SNF-defekter minskade störning av PHIP tydligt tumörcellernas fitness, medan organoider från en närliggande hjärncancer utan SWI/SNF-mutationer i stort sett var opåverkade. När organoider med PHIP-utsläckning implanterades i musers hjärnor överlevde djuren mycket längre än de med kontrolltumörer. Tumörer som slutligen återkom i PHIP-knockoutgruppen hade delvis återställda PHIP-nivåer, vilket indikerar att de celler som undkom PHIP-förlust var de som kunde växa igen.
Vad detta betyder för framtida cancerbehandlingar
Denna studie visar PHIP som en molekylär ”livvakt” som skyddar genaktivitet i cancerformer där SWI/SNF:s vanliga aktiverande kraft är försvagad. Genom att rekrytera ett märkande enzym för att kasta det repressiva NuRD-komplexet från viktiga promotorer möjliggör PHIP att SWI/SNF-mutanta tumörer håller viktiga tillväxtgener påslagna. Eftersom de flesta andra cancerformer—och sannolikt många normala celler—inte är lika beroende av PHIP, kan läkemedel som hämmar dess unika bindingsficka i princip slå hårdare mot sårbara rhabdoida och besläktade tumörer än mot frisk vävnad. Även om sådana behandlingar återstår att utveckla och kliniskt pröva, kartlägger studien en tydlig mekanistisk motivering för att rikta in sig på PHIP som en ny strategi mot några av de mest utmanande SWI/SNF-mutanta cancerformerna.
Citering: Malone, H.A., Myers, J.A., Gruss, E.G. et al. PHIP suppresses NuRD to enable the growth of SWI/SNF-mutant cancers. Nat Commun 17, 2877 (2026). https://doi.org/10.1038/s41467-026-70699-3
Nyckelord: epigenetisk cancervård, SWI/SNF-mutationer, NuRD-komplexet, kromatinombyggnad, rhabdoida tumörer