Clear Sky Science · it
PHIP sopprime NuRD per permettere la crescita dei tumori con mutazioni SWI/SNF
Perché questo studio è importante per il cancro
I tumori insorgono spesso quando la macchina cellulare che accende e spegne i geni va in tilt. Questo articolo esplora come una proteina poco nota chiamata PHIP aiuti la sopravvivenza di alcuni tumori pediatrici e ovarici altamente aggressivi, e perché bloccare PHIP potrebbe offrire un modo nuovo e selettivo per trattare neoplasie che attualmente hanno poche opzioni efficaci.
Lo scontro per il copione del DNA
All’interno delle nostre cellule il DNA è avvolto attorno a proteine avvolgenti per formare la cromatina, e grandi macchine molecolari ne modulano continuamente la struttura per aprire i geni all’attività o chiuderli. Una principale macchina “apritrice” è il complesso SWI/SNF, che usa energia chimica per allentare il DNA e consentire l’espressione genica. Sul fronte “chiudente” agiscono complessi come NuRD, che compattano la cromatina e rimuovono marche chimiche favorevoli all’espressione genica. In circa il 20% dei tumori, inclusi tumori rari ma letali chiamati rabdoidi e tumori ovarici correlati, componenti fondamentali di SWI/SNF vengono persi, indebolendo gravemente il lato attivatore di questo equilibrio.
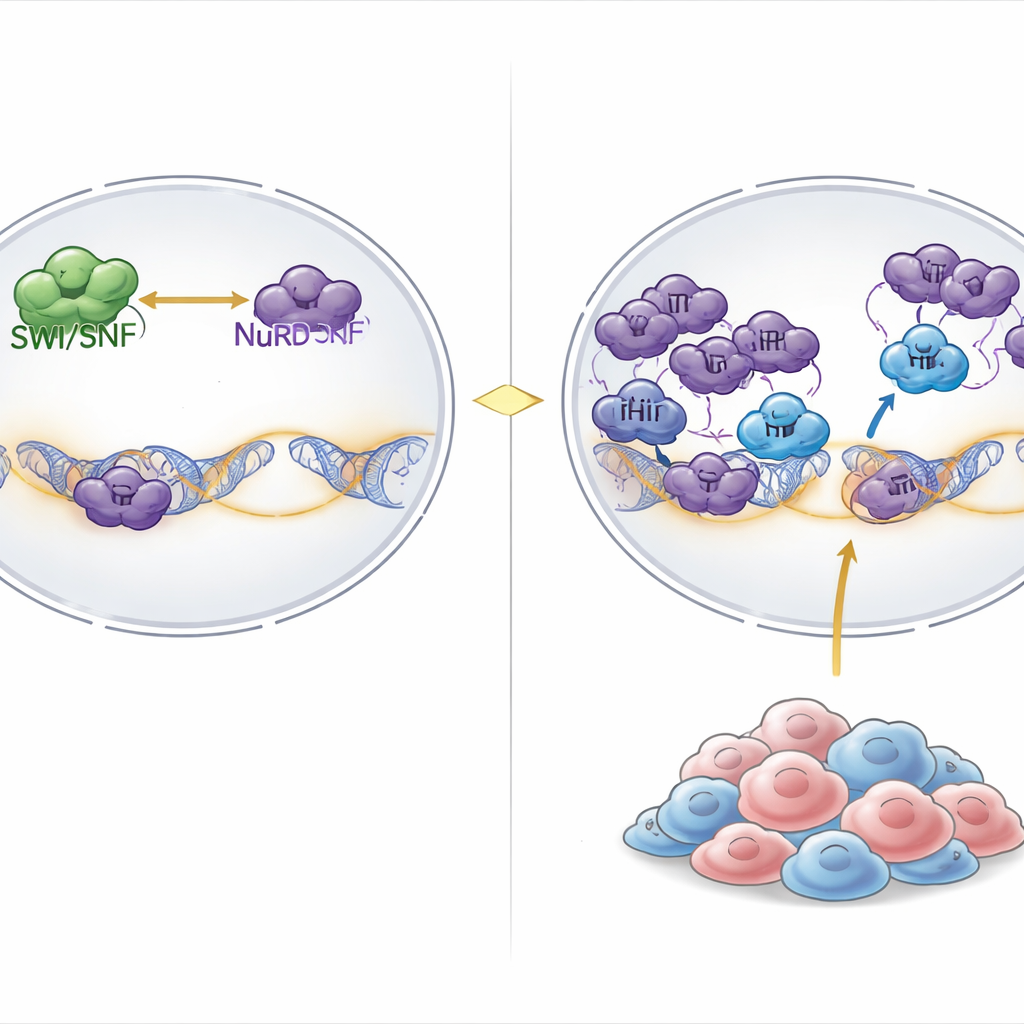
Scoprire una debolezza nascosta nei tumori con mutazioni SWI/SNF
I ricercatori hanno analizzato i risultati di screening CRISPR a livello genomico su più di mille linee cellulari tumorali. Hanno indagato quali geni fossero essenziali in modo unico nei tumori con ampia disfunzione di SWI/SNF. Un gene emerso con evidenza è stato PHIP, una proteina legante la cromatina precedentemente associata alla replicazione del DNA ma non chiaramente implicata nel controllo genico. Quando PHIP veniva disattivato, la crescita di cellule di tumori rabdoidi e ovarici con mutazioni SWI/SNF diminuiva drasticamente, mentre la maggior parte degli altri tipi di cancro tollerava la perdita di PHIP. L’introduzione di difetti SWI/SNF in cellule normalmente resistenti le rese sensibili alla perdita di PHIP, dimostrando che la dipendenza da PHIP è una conseguenza diretta del malfunzionamento di SWI/SNF e non del tipo di tessuto.
Come PHIP mantiene attivi i geni della crescita
Per capire cosa fa PHIP, il gruppo ha mappato dove si localizza sulla cromatina e come cambia l’attività genica al variare dei livelli di PHIP. PHIP si raggruppava vicino ai siti di inizio dei geni già marcati chimicamente come attivi. La riduzione di PHIP portava all’abbassamento di molti di questi geni, in particolare quelli che guidano la divisione cellulare, mentre l’aumento di PHIP aveva l’effetto opposto. PHIP si è rivelato anche cruciale per mantenere specifiche marche di acetilazione sulle istonine—indicatori chimici di uno stato di cromatina aperto favorevole alla trascrizione—su questi promotori. Senza PHIP l’acetilazione diminuiva e i geni corrispondenti si spegnevano, coerente con il ruolo di PHIP come guardiano locale delle regioni geniche attive.
PHIP come buttafuori per un complesso repressivo
PHIP non possiede attività enzimatica propria, perciò gli autori hanno chiesto se agisca reclutando altri fattori. Hanno scoperto che PHIP porta sulla cromatina un assemblaggio enzimatico chiamato ligasi ubiquitina CRL4. Questa ligasi attacca piccole etichette di ubiquitina a proteine bersaglio, modificandone spesso il comportamento o la localizzazione. Spettrometria di massa e test biochimici hanno rivelato che il complesso PHIP–CRL4 targhetta direttamente parti chiave del complesso NuRD, in particolare la subunità rimodellante CHD4. Nelle cellule tumorali PHIP era richiesto perché CRL4 interagisse con NuRD sul DNA, provocandone l’ubiquitinizzazione e la rimozione dai promotori. In assenza di PHIP, NuRD si accumulava ai siti di inizio genico, le marche locali di acetilazione calavano e i geni vicini venivano silenziati. È importante che ridurre i livelli di CHD4 potesse invertire la perdita di acetilazione causata dall’inattivazione di PHIP, attribuendo l’effetto all’attività rimodellante di NuRD.
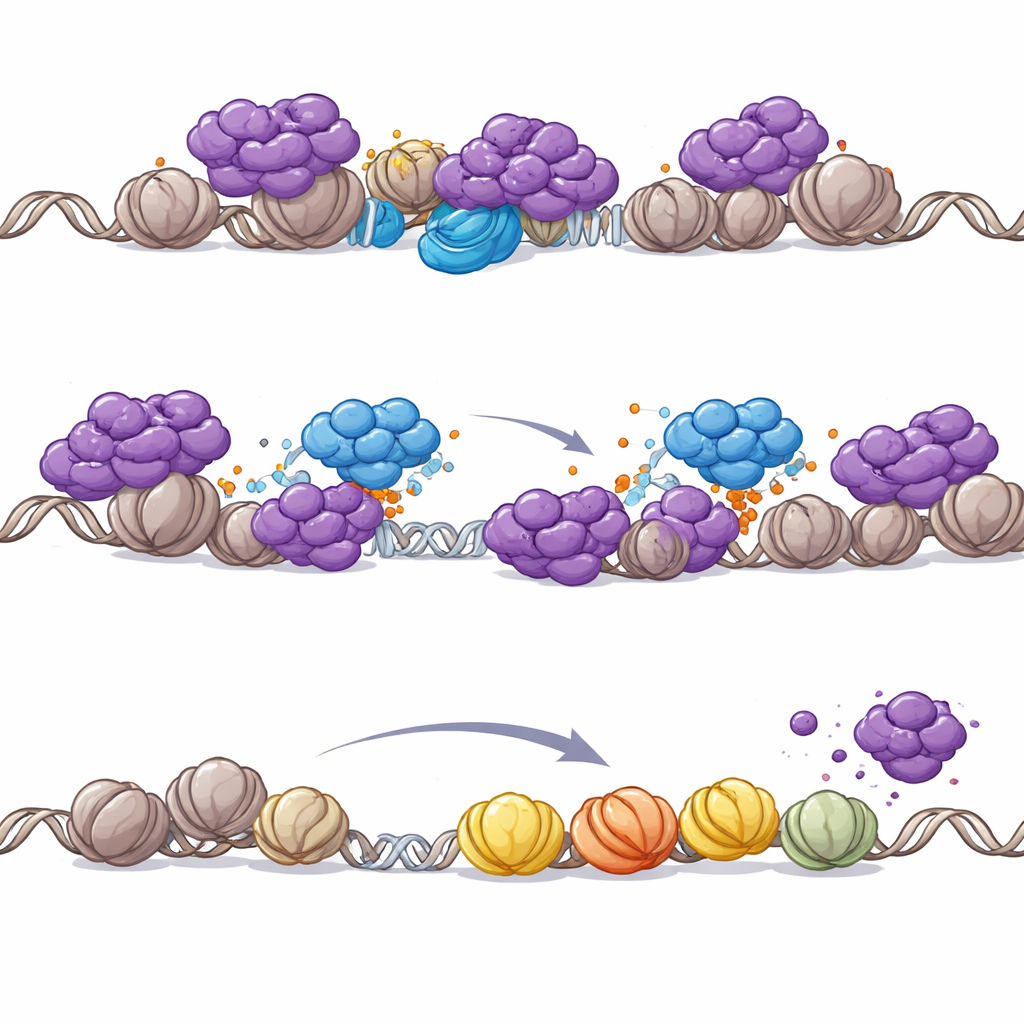
Perché PHIP diventa critico quando SWI/SNF è compromesso
Il gruppo ha poi indagato perché l’interazione PHIP–NuRD sia così importante specificamente nei tumori con mutazioni SWI/SNF. Ripristinare una subunità mancante di SWI/SNF nelle cellule di tumore rabdoide ha rimodellato la posizione di NuRD nel genoma: NuRD si è spostato lontano dai promotori verso regioni potenziatrici riattivate da SWI/SNF. Quando SWI/SNF è assente, tuttavia, NuRD si ridistribuisce sui promotori, minacciando lo spegnimento diffuso dei geni necessari alla sopravvivenza. In questo contesto vulnerabile, l’allontanamento mediato da PHIP di NuRD diventa essenziale per mantenere viva l’espressione genica guidata dai promotori. Anche in cellule altrimenti normali, degradare chimicamente i motori centrali di SWI/SNF era sufficiente a scatenare la rimozione di NuRD dipendente da PHIP dalla cromatina, rafforzando l’idea che il ruolo di PHIP sia strettamente legato alla perdita di SWI/SNF.
Dalle piastre di laboratorio ai tumori derivati dai pazienti
Per testare la rilevanza oltre le linee cellulari, i ricercatori hanno utilizzato organoidi tumorali cerebrali derivati da pazienti e modelli murini di tumori rabdoidi. In colture tridimensionali di tumori cresciute da neoplasie pediatriche con difetti di SWI/SNF, la perturbazione di PHIP riduceva marcatamente la fitness delle cellule tumorali, mentre gli organoidi di un tumore cerebrale correlato privo di mutazioni SWI/SNF risultavano in gran parte indifferenti. Quando organoidi con PHIP eliminato sono stati impiantati nel cervello di topi, gli animali sono sopravvissuti molto più a lungo rispetto a quelli con tumori di controllo. I tumori che alla fine recidivavano nel gruppo con knockout di PHIP presentavano livelli di PHIP parzialmente ripristinati, indicando che le cellule tumorali che sfuggivano alla perdita di PHIP erano quelle capaci di ricrescere.
Cosa significa per i trattamenti futuri contro il cancro
Questo lavoro identifica PHIP come una sorta di “guardaspalle” molecolare che protegge l’attività genica nei tumori in cui il potere attivatore di SWI/SNF è compromesso. Reclutando una ligasi che etichetta per scacciare il complesso repressivo NuRD dai promotori critici, PHIP permette ai tumori con mutazioni SWI/SNF di mantenere accesi geni chiave per la crescita. Poiché la maggior parte degli altri tipi di cancro—e presumibilmente molte cellule normali—non dipendono altrettanto da PHIP, farmaci che inibiscano la sua tasca di legame unica potrebbero, in linea di principio, colpire più duramente i tumori rabdoidi e correlati rispetto ai tessuti sani. Sebbene tali terapie restino da sviluppare e testare clinicamente, lo studio fornisce un chiaro razionale meccanicistico per mirare a PHIP come nuova strategia contro alcuni dei tumori con mutazioni SWI/SNF più difficili da trattare.
Citazione: Malone, H.A., Myers, J.A., Gruss, E.G. et al. PHIP suppresses NuRD to enable the growth of SWI/SNF-mutant cancers. Nat Commun 17, 2877 (2026). https://doi.org/10.1038/s41467-026-70699-3
Parole chiave: terapia oncologica epigenetica, mutazioni SWI/SNF, complesso NuRD, rimodellamento della cromatina, tumori rabdoidi