Clear Sky Science · nl
PHIP onderdrukt NuRD om de groei van SWI/SNF-gemuteerde kankers mogelijk te maken
Waarom deze studie belangrijk is voor kanker
Kankers ontstaan vaak wanneer het cellulaire machinerie dat genen aan- en uitzet verstoord raakt. Dit artikel onderzoekt hoe een minder bekend eiwit, PHIP, bepaalde zeer agressieve kinder- en ovariumkankers helpt overleven, en waarom het remmen van PHIP een nieuwe, selectieve manier zou kunnen bieden om tumoren te behandelen waarvoor nu weinig goede opties bestaan.
Het touwtrekken om het DNA-script
Binnen onze cellen is DNA opgerold rond eiwitspoelen tot chromatine, en grote moleculaire machines duwen voortdurend aan deze structuur om genen te openen of te sluiten. Een belangrijke “openende” machine is het SWI/SNF-complex, dat chemische energie gebruikt om DNA losser te maken en genactiviteit mogelijk te maken. Aan de “sluitende” kant werken complexen zoals NuRD, die chromatine aanspannen en chemische merktekens verwijderen die genexpressie bevorderen. In ongeveer 20% van de kankers — waaronder zeldzame maar dodelijke rhabdoïde tumoren en verwante ovariumkankers — gaan kernonderdelen van SWI/SNF verloren, waardoor de genactiverende kant van dit evenwicht ernstig verzwakt raakt.
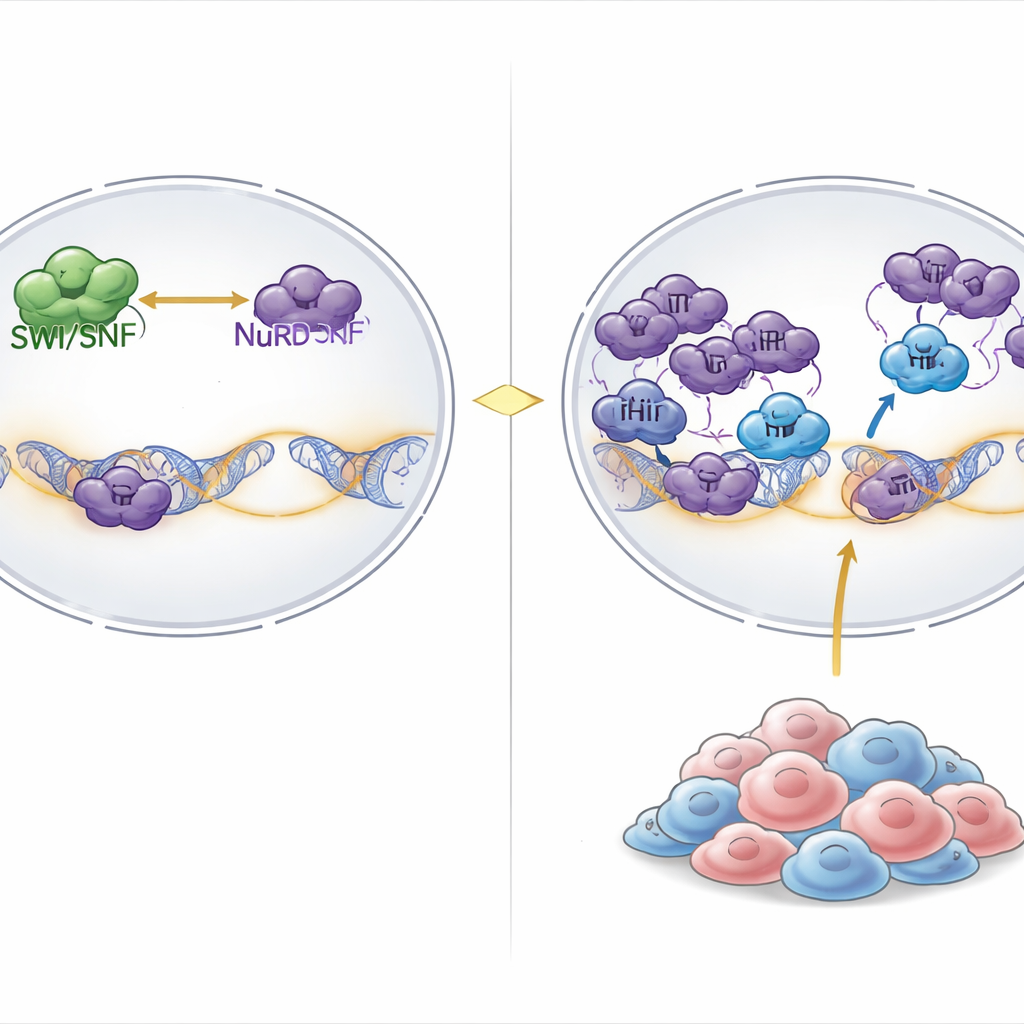
Een verborgen zwakte vinden in SWI/SNF-gemuteerde tumoren
De onderzoekers doorzochten resultaten van genoomwijde CRISPR-knockoutschermen in meer dan duizend kankercellijnen. Ze vroegen welke genen uniek essentieel waren in kankers met brede SWI/SNF-schade. Een opvallende hit was PHIP, een chromatine-bindend eiwit dat eerder aan DNA-replicatie werd gekoppeld maar niet duidelijk aan genregulatie. Wanneer PHIP werd uitgeschakeld, daalde de groei van SWI/SNF-gemuteerde rhabdoïde en ovariumkankercellen sterk, terwijl de meeste andere kankertypes verlies van PHIP tolereerden. Het inbrengen van SWI/SNF-defecten in normaal resistente cellen maakte deze cellen gevoelig voor verlies van PHIP, wat aantoont dat PHIP-afhankelijkheid een direct gevolg is van SWI/SNF-falen en niet van het weefseltype.
Hoe PHIP groeigenen aangezet houdt
Om te begrijpen wat PHIP doet, bracht het team in kaart waar het op chromatine zit en hoe genactiviteit verandert als PHIP-niveaus stijgen of dalen. PHIP clustert nabij de startplaatsen van genen die al chemisch gemarkeerd zijn als actief. Het verminderen van PHIP zorgde ervoor dat veel van deze genen minder actief werden, vooral diegenen die de celdeling aansturen, terwijl het verhogen van PHIP het omgekeerde effect had. PHIP bleek ook cruciaal voor het in stand houden van specifieke acetyl-merken op histonen—chemische vlaggen die een open, transcriptie-vriendelijke chromatine-toestand signaleren—op deze promotoren. Zonder PHIP vervaagde de acetylatie en werden de corresponderende genen stiller, wat consistent is met PHIP als een lokale beschermer van actieve genregio’s.
PHIP als uitsmijter voor een repressief complex
PHIP heeft geen eigen enzymatische activiteit, dus vroegen de auteurs of het werkt door andere factoren te rekruteren. Ze vonden dat PHIP een enzymcomplex, de CRL4 ubiquitine-ligase, naar chromatine brengt. Deze ligase hecht kleine ubiquitinemerkjes aan doelwitten, wat vaak hun gedrag of locatie verandert. Massaspectrometrie en biochemische testen toonden aan dat PHIP–CRL4 rechtstreeks sleutelonderdelen van het NuRD-complex markeert, in het bijzonder de CHD4-remodelleringssubeenheid. In kankercellen was PHIP nodig zodat CRL4 NuRD op het DNA kon aanspreken, wat leidde tot ubiquitinatie van NuRD en het verwijderen ervan van promotoren. Wanneer PHIP verloren ging, stapelde NuRD zich op bij genstartplaatsen, daalden lokale acetylmerktekens en werden nabijgelegen genen gedoofd. Belangrijk is dat het terugdraaien van CHD4 de acetylatie-verliezen veroorzaakt door PHIP-inactivatie kon herstellen, waarmee het effect aan NuRD’s remodellerende activiteit werd toegeschreven.
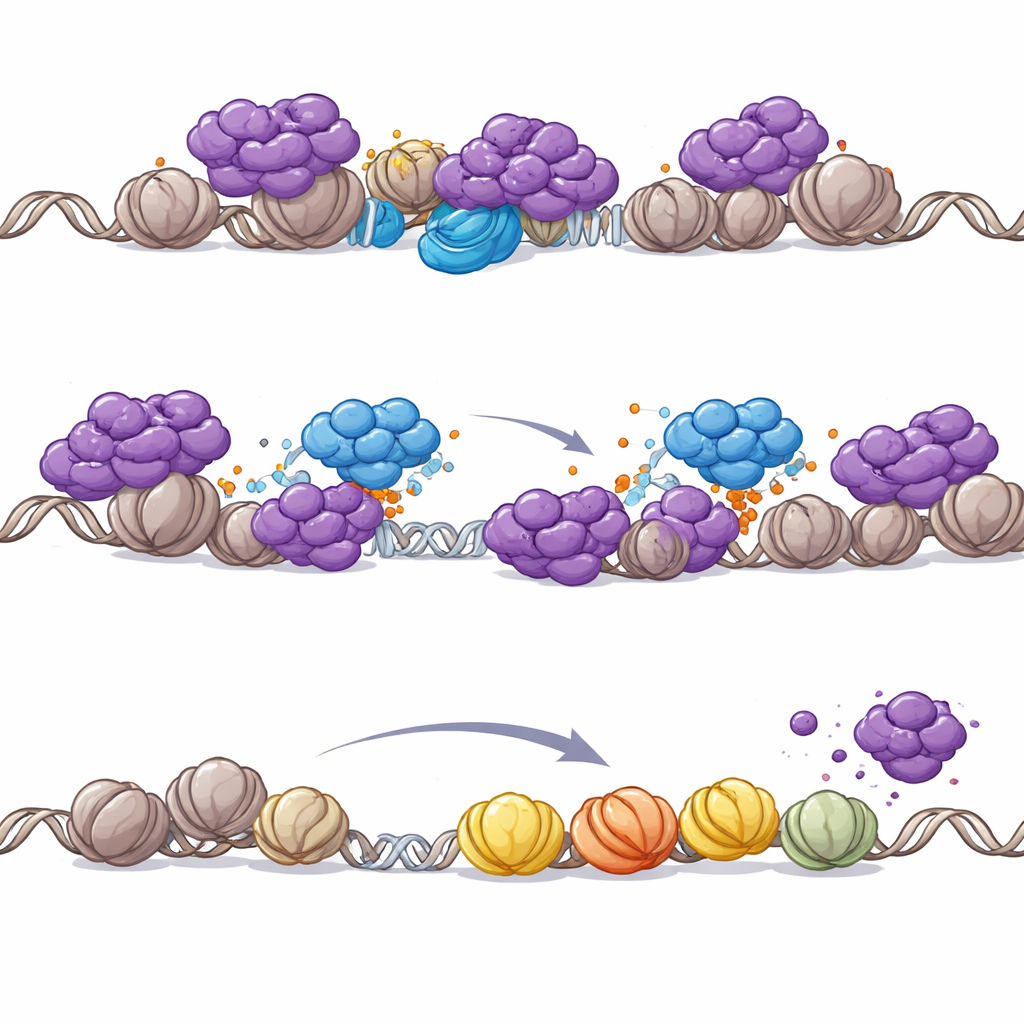
Waarom PHIP cruciaal wordt als SWI/SNF kapot is
Het team onderzocht vervolgens waarom deze PHIP–NuRD-interactie juist in SWI/SNF-gemuteerde kankers zo belangrijk is. Het herstellen van een ontbrekende SWI/SNF-subeenheid in rhabdoïde tumorcellen veranderde waar NuRD zich over het genoom verspreidt: NuRD schoof weg van promotoren en richting enhancergebieden die door SWI/SNF werden geheractiveerd. Wanneer SWI/SNF afwezig is, herverdeelt NuRD zich echter naar promotoren, waardoor een wijdverspreide uitschakeling van genen die essentieel zijn voor overleving dreigt. In deze kwetsbare situatie wordt PHIP-gemedieerde verdrijving van NuRD essentieel om promotor-gedreven genexpressie gaande te houden. Zelfs in verder normale cellen was chemische afbraak van SWI/SNF’s kernmotoren voldoende om PHIP-afhankelijke verwijdering van NuRD van chromatine te triggeren, wat benadrukt dat PHIP’s rol nauw verbonden is met verlies van SWI/SNF.
Van laboratoriumschalen naar patiënt-afgeleide tumoren
Om de relevantie buiten cellijnen te testen, gebruikten de onderzoekers patiënt-afgeleide hersentumororganoïden en muismodellen van rhabdoïde tumoren. In driedimensionale tumorculturen gekweekt uit kinderen met SWI/SNF-defecten verminderde het verstoren van PHIP de fitheid van tumorcellen aanzienlijk, terwijl organoïden van een verwante hersenkanker zonder SWI/SNF-mutaties grotendeels onaangedaan bleven. Wanneer organoïden met PHIP-knockout in de hersenen van muizen werden geïmplanteerd, leefden de dieren veel langer dan die met controletumoren. Tumoren die uiteindelijk terugkeerden in de PHIP-knockoutgroep hadden deels herstelde PHIP-niveaus, wat aangeeft dat kankercellen die ontsnapten aan PHIP-verlies degenen waren die konden teruggroeien.
Wat dit betekent voor toekomstige kankerbehandelingen
Dit werk onthult PHIP als een moleculaire “bodyguard” die genactiviteit beschermt in kankers waar SWI/SNF’s gebruikelijke activerende kracht is verlamd. Door een merkenzym te rekruteren om het repressieve NuRD-complex van cruciale promotoren te verdrijven, stelt PHIP SWI/SNF-gemuteerde tumoren in staat om belangrijke groeigenen aan te houden. Omdat de meeste andere kankertypes — en naar verwachting veel normale cellen — niet zo sterk op PHIP leunen, zouden medicijnen die zijn unieke bindingspocket remmen in principe kwetsbare rhabdoïde en verwante tumoren veel harder kunnen raken dan gezond weefsel. Hoewel dergelijke behandelingen nog ontwikkeld en klinisch getest moeten worden, schetst de studie een duidelijke mechanistische rechtvaardiging om PHIP te richten als een nieuwe strategie tegen enkele van de meest uitdagende SWI/SNF-gemuteerde kankers.
Bronvermelding: Malone, H.A., Myers, J.A., Gruss, E.G. et al. PHIP suppresses NuRD to enable the growth of SWI/SNF-mutant cancers. Nat Commun 17, 2877 (2026). https://doi.org/10.1038/s41467-026-70699-3
Trefwoorden: epigenetische kankertherapie, SWI/SNF-mutaties, NuRD-complex, chromatinehermodellering, rhabdoïde tumoren