Clear Sky Science · ja
PHIPはNuRDを抑えてSWI/SNF変異があるがんの増殖を可能にする
なぜこの研究ががんにとって重要か
がんはしばしば遺伝子のオン・オフを制御する細胞機構が乱れることで発生します。本論文は、PHIPと呼ばれる比較的知られていないタンパク質が、特定の高度に攻撃的な小児がんや卵巣がんの生存をどのように助けているか、そしてPHIPを阻害することが、現在治療選択肢が限られるこれらの腫瘍に対する新しい選択的治療法を提供し得る理由を探ります。
DNAの脚本をめぐる綱引き
細胞内ではDNAはタンパク質のスプールに巻かれてクロマチンを形成しており、大型の分子マシンがこの構造を常に押し広げたり閉じたりして、遺伝子を利用可能にしたり不活化したりします。遺伝子を“開く”主要な装置の一つがSWI/SNF複合体で、化学エネルギーを利用してDNAを緩め、遺伝子の活性化を促します。一方で“閉じる”側にはNuRDのような複合体があり、クロマチンを引き締め、遺伝子発現を促す化学的標識を除去します。約20%のがん、希少で致命的なラブドイド腫瘍や関連する卵巣がんを含め、多くでSWI/SNFの中核成分が失われ、このバランスの遺伝子活性化側が著しく弱まっています。
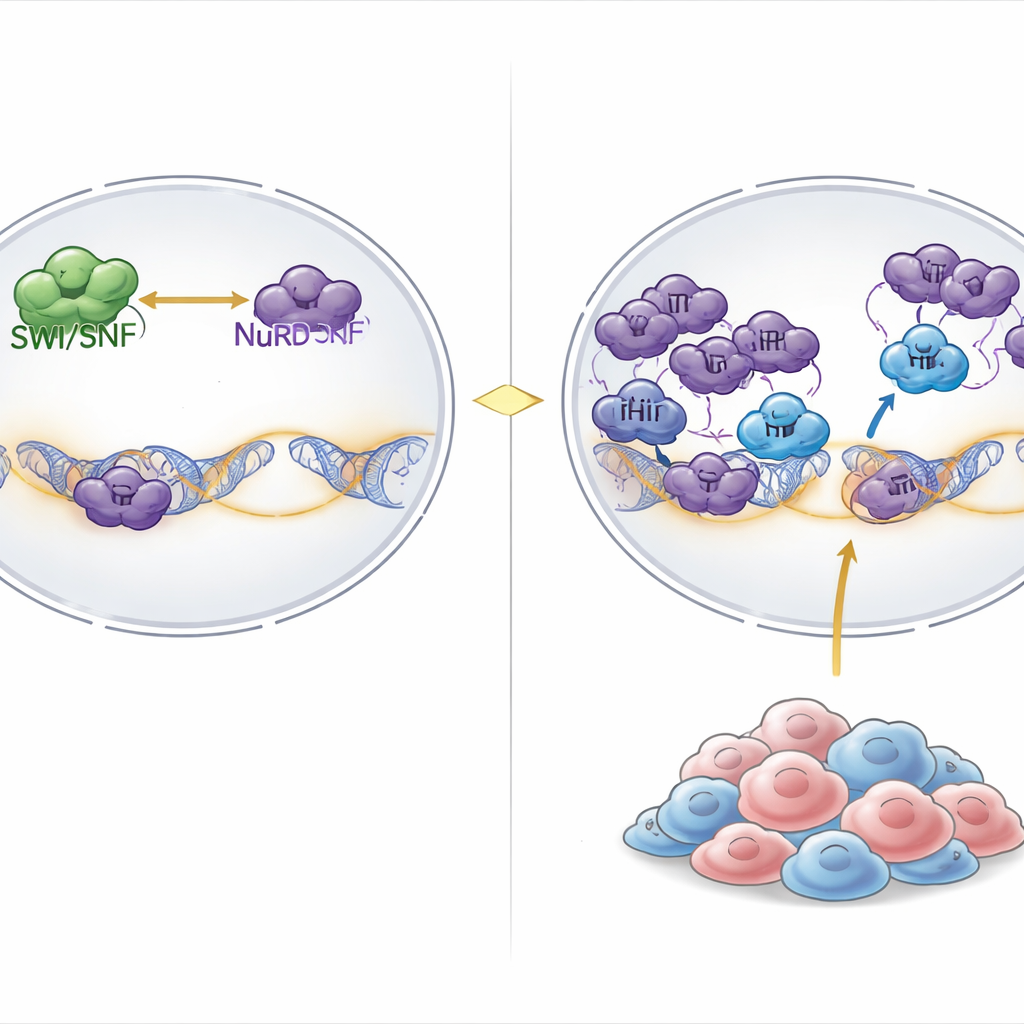
SWI/SNF変異腫瘍における潜在的弱点の発見
研究者らは1000以上のがん細胞株を対象としたゲノムワイドCRISPR遺伝子ノックアウトスクリーニングの結果を精査しました。SWI/SNFが広範に破壊されているがんで特に必須となる遺伝子はどれかを問い、際立ったヒットとしてPHIPが浮かび上がりました。PHIPはこれまでDNA複製に関連づけられていたクロマチン結合タンパク質ですが、遺伝子制御との明確な結びつきは示されていませんでした。PHIPを無効化すると、SWI/SNF変異を持つラブドイドおよび卵巣がん細胞の増殖が急激に低下したのに対し、多くの他のがん種はPHIP喪失に耐性を示しました。通常は耐性のある細胞にSWI/SNF欠損を導入するとPHIP喪失に敏感になり、PHIP依存が組織型ではなくSWI/SNF機能不全の直接的な結果であることが示されました。
PHIPが増殖遺伝子を維持する仕組み
PHIPの機能を解明するため、研究班はPHIPがクロマチンのどこに存在するか、PHIP量の増減が遺伝子活性にどう影響するかをマッピングしました。PHIPはすでに活性化を示す化学マークを持つ遺伝子の開始領域近傍に集まっていました。PHIPを減らすと、特に細胞分裂を促す遺伝子群が多く抑制され、PHIPを増やすと逆の効果が見られました。PHIPはまた、これらのプロモーターにおけるヒストンタンパク質の特定のアセチル化マークを維持する上で重要であり、これらの化学的旗はクロマチンが開いて転写に適した状態であることを示します。PHIPがないとアセチル化は失われ、対応する遺伝子は沈静化し、PHIPが局所的な活性遺伝子領域の守護者として働くことと整合します。
抑制複合体の“バウンサー”としてのPHIP
PHIP自体に酵素活性はないため、著者らは他因子をリクルートして機能するのかを検討しました。その結果、PHIPはCRL4と呼ばれるユビキチンライゲースの酵素複合体をクロマチンに導くことが分かりました。このライゲースは標的タンパク質に小さなユビキチンタグを付け、多くの場合それらの挙動や局在を変えます。質量分析や生化学的検査により、PHIP–CRL4はNuRD複合体の主要部分、特にCHD4リモデリングサブユニットに直接タグを付けることが明らかになりました。がん細胞では、PHIPはCRL4がDNA上でNuRDと関わるために必要で、NuRDのユビキチン化とプロモーターからの除去が起きます。PHIPが失われるとNuRDは遺伝子開始部位に蓄積し、局所のアセチルマークが低下して近傍の遺伝子がサイレンシングされました。重要なことに、CHD4を抑えるとPHIP不活化によるアセチル化喪失を逆転でき、この影響がNuRDのリモデリング活性に依存することを示しました。
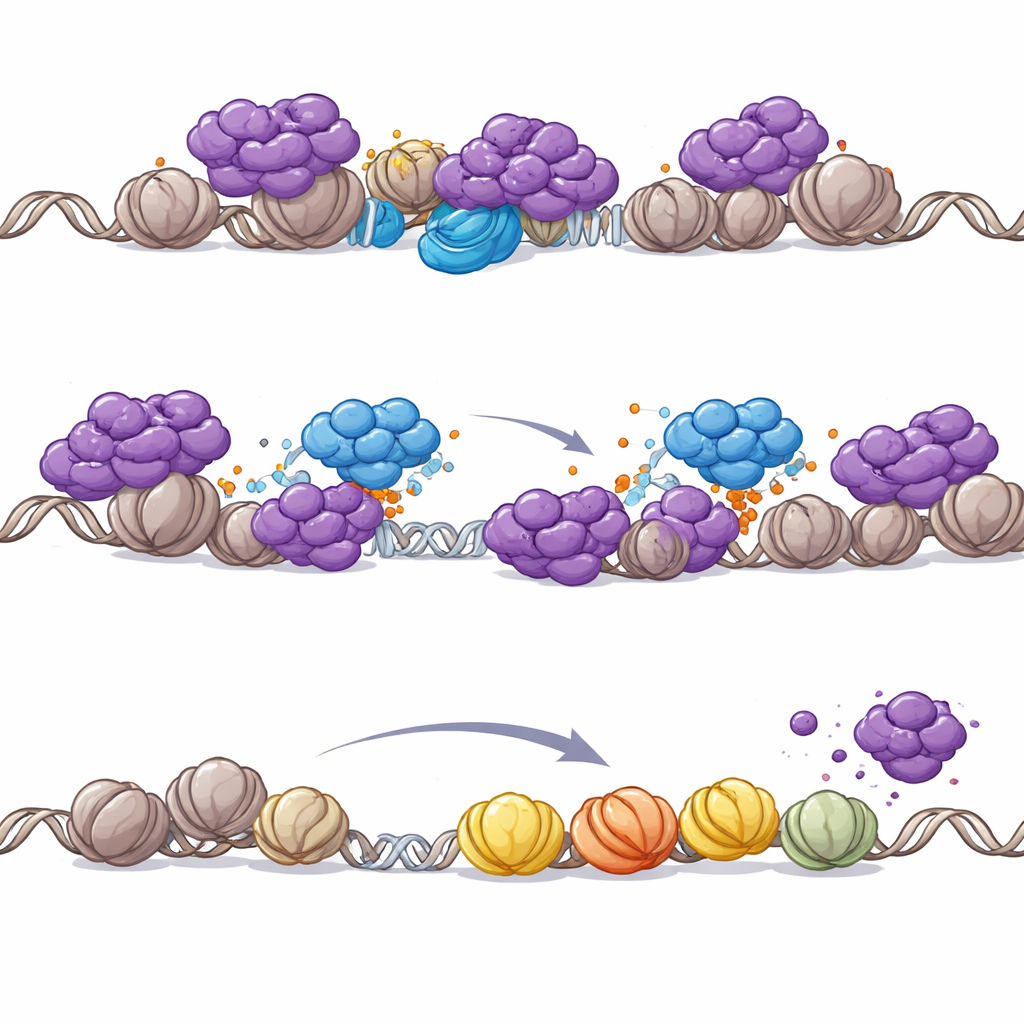
なぜSWI/SNFが壊れるとPHIPが重要になるのか
次に研究班は、なぜこのPHIP–NuRD相互作用が特にSWI/SNF変異があるがんで重要なのかを探りました。ラブドイド腫瘍細胞に欠損していたSWI/SNFサブユニットを回復させると、NuRDのゲノム上での位置が変わりました。NuRDはプロモーターから離れて、SWI/SNFによって再活性化されたエンハンサー領域へ移動したのです。しかしSWI/SNFが欠損しているとNuRDはプロモーターに再配分され、生存に必要な遺伝子の大規模なシャットダウンを招く恐れがあります。この脆弱な状況では、NuRDをプロモーターから追い出すPHIPによる仕組みがプロモーター駆動の遺伝子発現を維持するために不可欠になります。正常な細胞でも化学的にSWI/SNFの中核機能を分解すると、PHIP依存的なNuRDのクロマチンからの除去が誘導され、PHIPの役割がSWI/SNF喪失と密接に結びついていることが補強されました。
培養皿から患者由来腫瘍へ
細胞株を越えた関連性を確認するため、研究者らは患者由来の脳腫瘍オルガノイドやラブドイド腫瘍のマウスモデルを用いました。SWI/SNF欠損を持つ小児がんから育てた三次元腫瘍培養では、PHIPを破壊すると腫瘍細胞の適合性が著しく低下した一方、SWI/SNF変異を欠く関連する脳がん由来のオルガノイドは大きな影響を受けませんでした。PHIPをノックアウトしたオルガノイドをマウスの脳に移植すると、対照腫瘍を有する群よりも動物の生存が大幅に延びました。PHIPノックアウト群で最終的に再発した腫瘍は部分的にPHIPレベルを回復しており、PHIP喪失を回避したがん細胞だけが再増殖できたことを示しています。
今後のがん治療にとっての意義
本研究は、SWI/SNFの通常の活性化能力が損なわれたがんで遺伝子活性を守る分子的“ボディーガード”としてPHIPを明らかにしました。PHIPはタグ付け酵素を呼び寄せて抑制的なNuRD複合体を重要なプロモーターから追い出すことで、SWI/SNF変異腫瘍が主要な増殖遺伝子をオンに保つことを可能にします。ほとんどの他のがん種や多くの正常細胞はPHIPにそれほど依存していないと考えられるため、その特有の結合ポケットを阻害する薬剤は理論的にはラブドイドや関連腫瘍を健常組織より強く攻撃できる可能性があります。そのような治療法はまだ開発と臨床検証が必要ですが、本研究は一部の困難なSWI/SNF変異がんに対するPHIP標的化の明確な機序的根拠を示しています。
引用: Malone, H.A., Myers, J.A., Gruss, E.G. et al. PHIP suppresses NuRD to enable the growth of SWI/SNF-mutant cancers. Nat Commun 17, 2877 (2026). https://doi.org/10.1038/s41467-026-70699-3
キーワード: エピジェネティックながん治療, SWI/SNF変異, NuRD複合体, クロマチンリモデリング, ラブドイド腫瘍