Clear Sky Science · he
PHIP מדכא את NuRD כדי לאפשר את צמיחתן של סרטן עם מוטציות ב-SWI/SNF
מדוע המחקר הזה חשוב לסרטן
סרטן נגרם לעתים קרובות כאשר המכונה התאית שמדליקה וכובלת גנים משתבשת. המאמר חוקר כיצד חלבון פחות מוכר בשם PHIP מסייע להישרדות סוגי סרטן ילדותיים ואובראיים אגרסיביים במיוחד, ולמה חסימת PHIP עשויה להציע דרך בררנית חדשה לטיפול בגידולים שיש להם כיום מעט אפשרויות טובות.
משיכת חבל על תסריט ה-DNA
בתאים שלנו ה-DNA מופרש סביב ספולות חלבוניות ויוצר כרומטין, ומכונות מולקולאריות גדולות דוחקות ומכווננות את המבנה הזה כדי לפתוח גנים לשימוש או לסגור אותם. אחת המכונות העיקריות שמאפילות לפתיחה היא קומפלקס SWI/SNF, שפועל באנרגיה כימית כדי לרכך את ה-DNA ולאפשר פעילות גנים. בצד הסגירה פועלים קומפלקסים כמו NuRD, שמעבים את כרומטין ומסירים סימנים כימיים התורמים לביטוי גנים. בכ-20% מהמקרים של סרטן, כולל גידולים נדירים אך קטלניים שמכונים רבדואידיים וסרטן שחלות קשור, חתיכות ליבתיות של SWI/SNF אובדות, מה שמחליש בצורה ניכרת את הצד המפעיל של האיזון הזה.
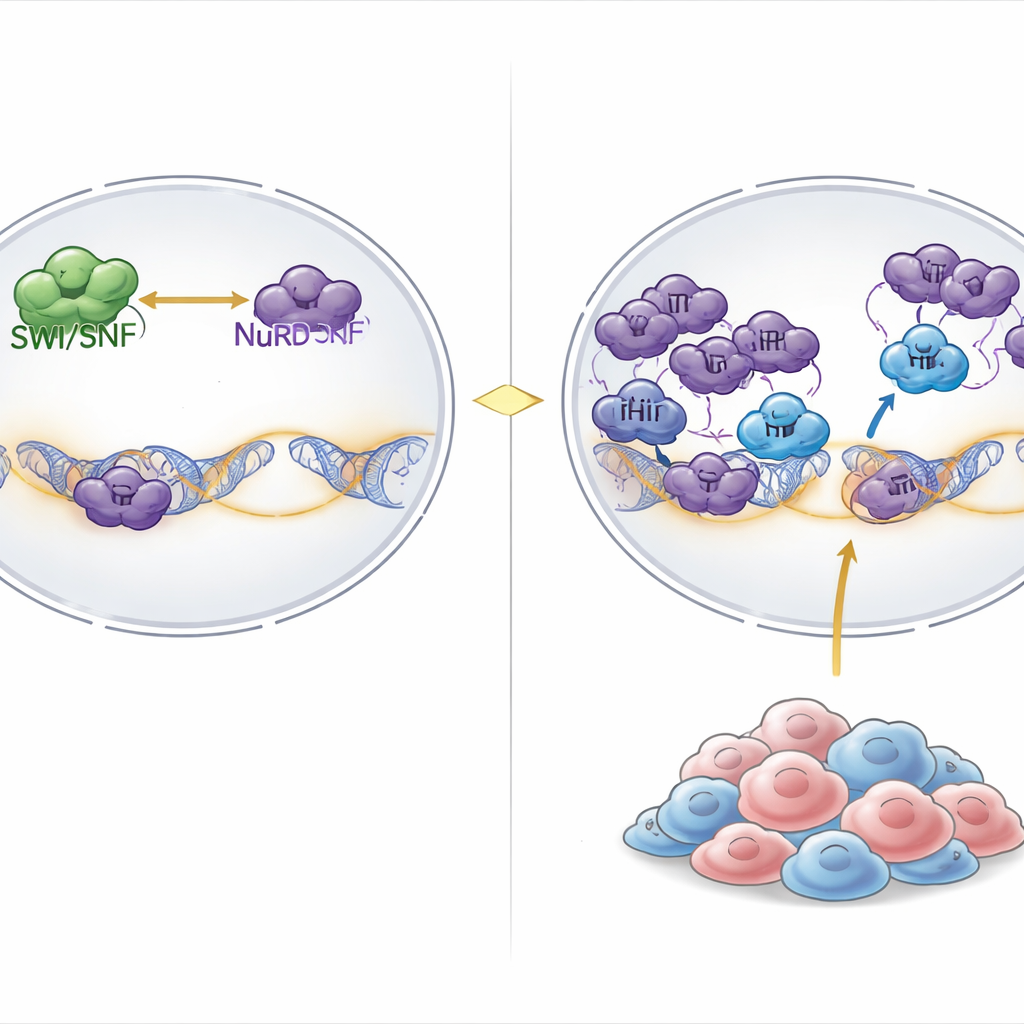
גילוי חולשה חבויה בגידולים עם מוטציות ב-SWI/SNF
החוקרים סרקו תוצאות של מסכי נוקאאוט גנים CRISPR ברמת הגנום ביותר מאלף שורות תאים סרטניות. הם חיפשו אילו גנים חיוניים באופן ייחודי בסרטנים עם פגיעה רחבה ב-SWI/SNF. ממצא בולט היה PHIP, חלבון הקשור לקשירת כרומטין שהיה ידוע קודם לכן בקשר לשכפול DNA אך לא נקשר באופן ברור לשליטה בגנים. כאשר PHIP נכבל, גידול של תאי סרטן רבדואידיים ושחלות עם מוטציות ב-SWI/SNF ירד באופן חמור, בעוד שרוב סוגי הסרטן האחרים העמידו את עצמם לאובדן PHIP. הכנסת פגמים ב-SWI/SNF לתאים שבדרך כלל עמידים הפכה אותם לרגישים לאובדן PHIP, והראתה שתלות ב-PHIP היא תוצאה ישירה של חוסר תפקוד ב-SWI/SNF ולא של סוג הרקמה.
כיצד PHIP שומרת על גנים מעוררי גדילה פתוחים
כדי להבין מה עושה PHIP, הצוות מיפוי את המיקומים שבהם היא יושבת על הכרומטין ואת השינויים בפעילות הגנים כאשר רמות PHIP עולות או יורדות. PHIP התרכזה בסביבת אתרי התחלת גנים שכבר נשאו סימנים כימיים של פעילות. הקטנת PHIP גרמה להורדת ביטוי של רבים מהגנים הללו, במיוחד כאלו המזרזים חלוקה תאית, בעוד שהגברת PHIP הובילה להשפעה הפוכה. PHIP הייתה גם קריטית לשימור סימני אצטילציה ספציפיים על היסטונים — דגלים כימיים שמסמנים מצבי כרומטין פתוחים הנוחים לשעתוק — בפרומוטרים אלה. ללא PHIP, האצטילציה נחלשה והגנים המתאימים שתקו, תואם לרעיון ש-PHIP פועלת כשומרת מקומית של אזורי גנים פעילים.
PHIP כשוער לכניסה של קומפלקס מדכא
PHIP אינה בעלת פעילות אנזימטית משלה, לכן המחברים שאלו האם היא פועלת על ידי גיוס גורמים אחרים. הם מצאו ש-PHIP מביאה להרכבה אנזימטית הנקראת CRL4 ubiquitin ligase אל הכרומטין. ליגאז זה מצמיד תגי ubiquitin קטנים לחלבונים יעד, פעמים רבות משנים את התנהגותם או מיקומם. ספקטרומטריה של מסה ובדיקות ביוכימיות הראו ש-PHIP–CRL4 תייגו ישירות חלקים מרכזיים של קומפלקס NuRD, ובפרט את תת-היחידה המחוללת CHD4. בתאי סרטן, PHIP הייתה נדרשת כדי ש-CRL4 יפנה אל NuRD על ה-DNA, מה שהוביל לאובייקטציה של NuRD והסרתו מהפרומוטרים. כאשר PHIP נפלה, NuRD הצטבר באתרי תחילת גנים, סימני האצטיל המקומיים ירדו והגנים הקרובים דוכאו. חשוב לציין, הורדה של CHD4 יכלה להפוך את אובדן האצטילציה שנגרם מאי-פעילות PHIP, מה שמקשר את ההשפעה לפעילות העיצוב של NuRD.
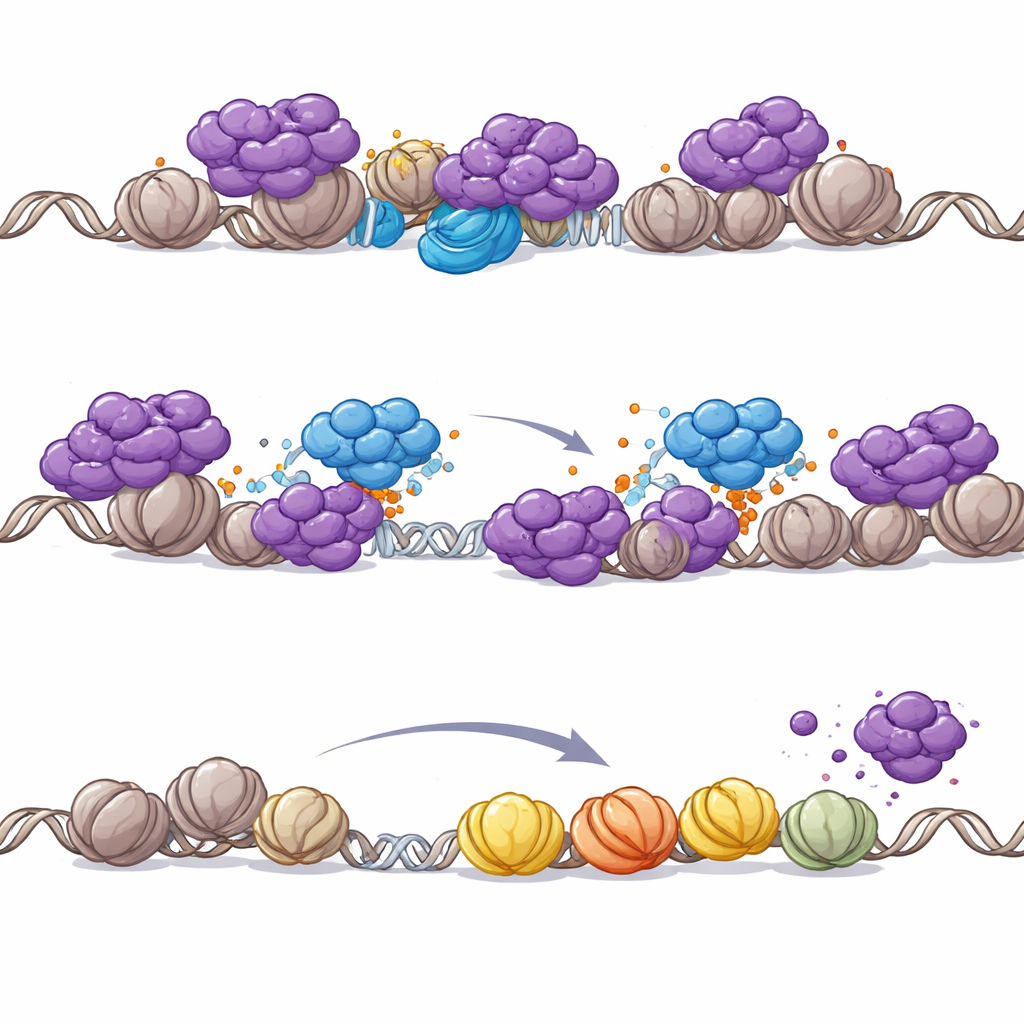
מדוע PHIP הופכת חיונית כאשר SWI/SNF שבור
הצוות בחן לאחר מכן מדוע אינטראקציית PHIP–NuRD כה משמעותית במיוחד בסרטנים עם מוטציות ב-SWI/SNF. שיחזור תת-יחידה חסרה של SWI/SNF בתאי גידול רבדואידיים שינה את התפוצה של NuRD על הגנום: NuRD זז הרחק מהפרומוטרים ואל אזורי מאיצים שהופעלו מחדש על ידי SWI/SNF. כאשר SWI/SNF נעדרת, לעומת זאת, NuRD מתעדף להתמקם בפרומוטרים, מה שמאיים על השתקה נרחבת של גנים הדרושים להישרדות. בהקשר הפגיע הזה, פינוי NuRD בתיווך PHIP נעשה חיוני כדי לשמור על ביטוי גנים מונחה פרומוטרים. גם בתאים שנראים נורמליים, פירוק כימי של מנועי הליבה של SWI/SNF הספיק לעורר פינוי NuRD התלוי ב-PHIP מהכרומטין, מה שמחזק שהתפקיד של PHIP קשור קשר הדוק לאובדן SWI/SNF.
מצלחות מעבדה אל גידולים שמקורם בחולים
כדי לבדוק רלוונטיות מעבר לשורות תאים, החוקרים פנו לאורגנואידים של גידולי מוח שמקורם בחולים ולמודלים בעכברים של גידולים רבדואידיים. בתרביות תלת־ממדיות של גידולים שגודלו ממחלת ילדים עם פגמים ב-SWI/SNF, הפרעה ב-PHIP הפחיתה במידה ניכרת את הכשירות של תאי הגידול, בעוד שאורגנואידים ממחלה מוחית קרובה שנטולת מוטציות ב-SWI/SNF לא הושפעו ברובם. כאשר אורגנואידים עם נוקאאוט של PHIP הושתלו במוחות עכברים, החיות חיו זמן רב יותר במידה משמעותית לעומת אלו שנשאו גידולים ביקורתיים. הגידולים שחזרו בסופו של דבר בקבוצת נוקאאוט PHIP החזירו חלקית את רמות PHIP, מה שמעיד שהתאים הסרטניים שברחו מאובדן PHIP הם אלו שיכלו להתרבות מחדש.
מה זה אומר לטיפולי סרטן בעתיד
המחקר חושף את PHIP כ"בלש מגן" מולקולרי שמגן על פעילות גנים בסרטנים שבהם הכוח המפעיל הטבעי של SWI/SNF נחלש. על ידי גיוס אנזים מצמיד תגים כדי לגרש את קומפלקס NuRD המדכא מפרומוטרים קריטיים, PHIP מאפשרת לסרטנים עם מוטציות ב-SWI/SNF לשמור על הדלקת גנים מרכזיים לצמיחה. מכיוון שרוב סוגי הסרטן האחרים — וככל הנראה גם תאים נורמליים רבים — אינם תלויים כל כך ב-PHIP, תרופות שימנעו את הכיס הקשירה הייחודי שלה יכולות, מבחינה עקרונית, לפגוע בגידולים הרבדואידיים ובגידולים הקשורים בהם הרבה יותר מאשר ברקמה בריאה. אמנם טיפולים כאלה עדיין דורשים פיתוח ובדיקות קליניות, המחקר ממפה הסבר מכניסטי ברור למיקוד ב-PHIP כאסטרטגיה חדשה נגד חלק מהסרטן המאתגר ביותר עם מוטציות ב-SWI/SNF.
ציטוט: Malone, H.A., Myers, J.A., Gruss, E.G. et al. PHIP suppresses NuRD to enable the growth of SWI/SNF-mutant cancers. Nat Commun 17, 2877 (2026). https://doi.org/10.1038/s41467-026-70699-3
מילות מפתח: טיפול אפיגנטי בסרטן, מוטציות ב-SWI/SNF, קומפלקס NuRD, עיצוב כרומטין, גידולים רבדואידיים