Clear Sky Science · es
PHIP suprime a NuRD para permitir el crecimiento de los cánceres con mutaciones en SWI/SNF
Por qué este estudio importa para el cáncer
Los cánceres suelen surgir cuando la maquinaria celular que enciende y apaga los genes falla. Este artículo explora cómo una proteína poco conocida llamada PHIP ayuda a que ciertos cánceres pediátricos y de ovario, altamente agresivos, sobrevivan, y por qué bloquear PHIP podría ofrecer una forma nueva y selectiva de tratar tumores que hoy tienen pocas opciones eficaces.
La lucha por el guion del ADN
Dentro de nuestras células, el ADN está enrollado alrededor de carretes proteicos para formar la cromatina, y grandes máquinas moleculares ajustan constantemente esta estructura para abrir genes y permitir su uso o cerrarlos. Una máquina clave de “apertura” es el complejo SWI/SNF, que emplea energía química para aflojar el ADN y permitir la actividad génica. En el lado de “cierre” están complejos como NuRD, que compactan la cromatina y eliminan marcas químicas que favorecen la expresión génica. En aproximadamente el 20% de los cánceres, incluidos tumores raros pero letales llamados rabdoides y cánceres ováricos relacionados, piezas centrales de SWI/SNF se pierden, debilitando gravemente el lado activador de este equilibrio.
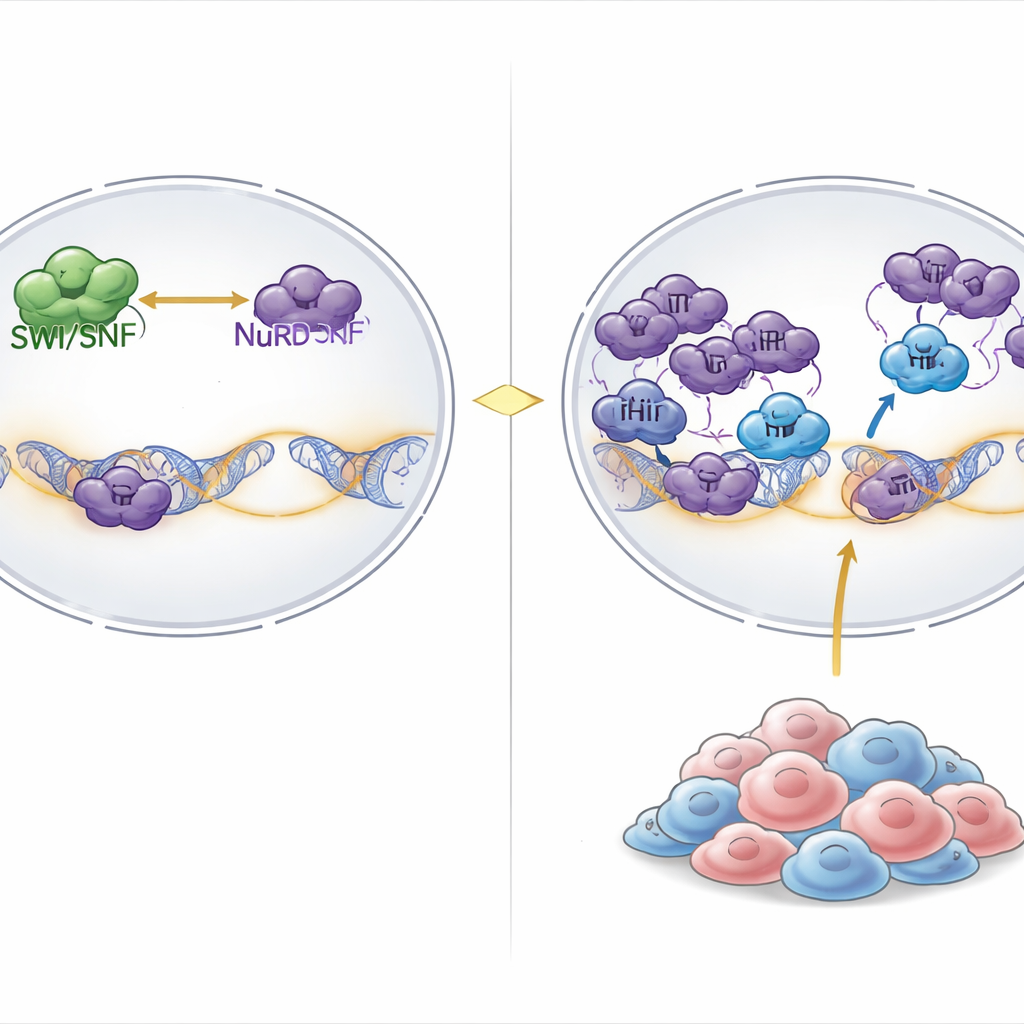
Encontrar una debilidad oculta en tumores con mutaciones en SWI/SNF
Los investigadores rastrearon resultados de cribados génicos CRISPR a escala genómica en más de mil líneas celulares cancerosas. Preguntaron qué genes eran singularmente esenciales en cánceres con una amplia disrupción de SWI/SNF. Un hallazgo destacado fue PHIP, una proteína que se une a la cromatina previamente vinculada a la replicación del ADN pero no claramente asociada al control génico. Cuando PHIP se desactivó, el crecimiento de células de tumores rabdoides y ováricos con mutaciones en SWI/SNF disminuyó drásticamente, mientras que la mayoría de otros tipos de cáncer toleraron la pérdida de PHIP. Introducir defectos de SWI/SNF en células normalmente resistentes las hizo sensibles a la pérdida de PHIP, mostrando que la dependencia de PHIP es una consecuencia directa del mal funcionamiento de SWI/SNF más que del tipo de tejido.
Cómo PHIP mantiene activados los genes de crecimiento
Para entender qué hace PHIP, el equipo cartografió dónde se localiza en la cromatina y cómo cambia la actividad génica cuando los niveles de PHIP aumentan o disminuyen. PHIP se agrupó cerca de los sitios de inicio de genes que ya presentan marcas químicas de actividad. Reducir PHIP provocó la caída de la expresión de muchos de estos genes, especialmente los que impulsan la división celular, mientras que aumentar PHIP produjo el efecto contrario. PHIP también resultó crucial para mantener marcas específicas de acetilación en las histonas—señales químicas que indican un estado de cromatina abierto y favorable a la transcripción—en estos promotores. Sin PHIP, la acetilación se desvaneció y los genes correspondientes se apagaron, consistente con el papel de PHIP como guardián local de regiones génicas activas.
PHIP como portero frente a un complejo represor
PHIP carece de actividad enzimática propia, por lo que los autores indagaron si actúa reclutando otros factores. Descubrieron que PHIP trae a la cromatina un ensamblaje enzimático llamado ligasa de ubiquitina CRL4. Esta ligasa añade pequeñas etiquetas de ubiquitina a proteínas diana, cambiando a menudo su comportamiento o localización. La espectrometría de masas y pruebas bioquímicas revelaron que PHIP–CRL4 etiqueta directamente partes clave del complejo NuRD, particularmente la subunidad remodeladora CHD4. En células cancerosas, PHIP fue necesario para que CRL4 interaccionara con NuRD en el ADN, conduciendo a la ubiquitinación de NuRD y su eliminación de los promotores. Cuando PHIP se perdió, NuRD se acumuló en los sitios de inicio génico, las marcas locales de acetilación descendieron y los genes cercanos se silenciaron. Es importante que reducir CHD4 pudo revertir la pérdida de acetilación causada por la inactivación de PHIP, atribuyendo el efecto a la actividad remodeladora de NuRD.
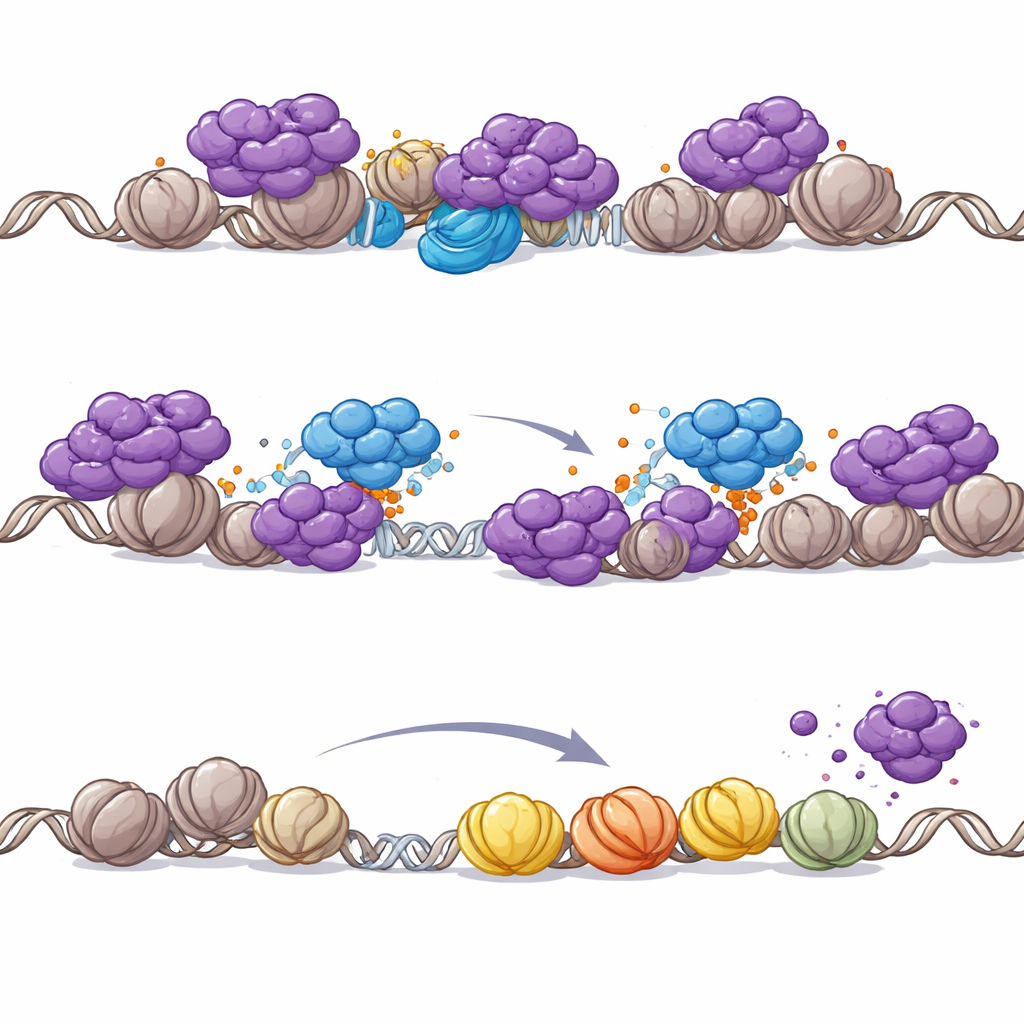
Por qué PHIP se vuelve crítico cuando SWI/SNF está roto
El equipo exploró por qué la interacción PHIP–NuRD importa tanto específicamente en cánceres con mutaciones en SWI/SNF. Restaurar una subunidad faltante de SWI/SNF en células de tumores rabdoides redistribuyó a NuRD en el genoma: NuRD se desplazó desde los promotores hacia regiones potenciadoras (enhancers) que SWI/SNF reactivó. Sin embargo, cuando SWI/SNF está ausente, NuRD se redistribuye a los promotores, amenazando con un apagado generalizado de genes necesarios para la supervivencia. En este escenario vulnerable, la expulsión mediada por PHIP de NuRD se vuelve esencial para mantener viva la expresión génica impulsada por promotores. Incluso en células por lo demás normales, degradar químicamente los motores centrales de SWI/SNF fue suficiente para desencadenar la remoción dependiente de PHIP de NuRD de la cromatina, lo que refuerza que el papel de PHIP está estrechamente ligado a la pérdida de SWI/SNF.
De placas de laboratorio a tumores derivados de pacientes
Para evaluar la relevancia más allá de las líneas celulares, los investigadores recurrieron a organoides de tumores cerebrales derivados de pacientes y a modelos de ratón de tumores rabdoides. En cultivos tumorales tridimensionales obtenidos de cánceres infantiles con defectos en SWI/SNF, la interrupción de PHIP redujo notablemente la competitividad de las células tumorales, mientras que los organoides de un cáncer cerebral relacionado sin mutaciones en SWI/SNF resultaron en gran medida no afectados. Cuando los organoides con PHIP eliminado se implantaron en cerebros de ratones, los animales vivieron mucho más que los que portaban tumores de control. Los tumores que finalmente regresaron en el grupo con PHIP eliminado mostraron niveles de PHIP parcialmente restaurados, lo que indica que las células cancerosas que escaparon a la pérdida de PHIP fueron las capaces de volver a crecer.
Qué significa esto para futuros tratamientos contra el cáncer
Este trabajo revela a PHIP como un “guardaespaldas” molecular que protege la actividad génica en cánceres donde el poder activador habitual de SWI/SNF está mermado. Al reclutar una enzima etiquetadora para expulsar al complejo represor NuRD de promotores críticos, PHIP permite que los tumores con mutaciones en SWI/SNF mantengan encendidos genes clave de crecimiento. Dado que la mayoría de otros tipos de cáncer—y presumiblemente muchas células normales—no dependen de forma tan intensa de PHIP, fármacos que inhiban su bolsillo de unión único podrían, en principio, golpear con más fuerza a los tumores rabdoides y relacionados que a los tejidos sanos. Aunque tales tratamientos aún deben desarrollarse y probarse clínicamente, el estudio traza una justificación mecanicista clara para dirigir PHIP como una nueva estrategia contra algunos de los cánceres con mutaciones en SWI/SNF más desafiantes.
Cita: Malone, H.A., Myers, J.A., Gruss, E.G. et al. PHIP suppresses NuRD to enable the growth of SWI/SNF-mutant cancers. Nat Commun 17, 2877 (2026). https://doi.org/10.1038/s41467-026-70699-3
Palabras clave: terapia epigenética contra el cáncer, mutaciones en SWI/SNF, complejo NuRD, remodelación de la cromatina, tumores rabdoides