Clear Sky Science · ar
يمنع PHIP مركب NuRD لتمكين نمو السرطانات ذات طفرات SWI/SNF
لماذا تُعَد هذه الدراسة مهمة للسرطان
تنشأ السرطانات غالباً عندما يتعطل جهاز الخلايا المسؤول عن تشغيل وإيقاف الجينات. تستكشف هذه الورقة كيف يساعد بروتين أقل شهرة يُدعى PHIP بعض السرطانات الطفولية المفرطة العدوانية وسرطانات المبيض على البقاء، ولماذا قد يوفر حجب PHIP وسيلة جديدة ومحددة لعلاج أورام تفتقر حالياً إلى خيارات فعّالة.
الصراع حول نص الحمض النووي
داخل خلايانا، يُلف الحمض النووي حول بكرات بروتينية مكوّناً الكروماتين، وتدفع آلات جزيئية كبيرة هذا الهيكل باستمرار لكي تفتح الجينات للاستعمال أو تُغلقها. أحد الآلات الرئيسية التي «تفتح» هو مركب SWI/SNF، الذي يستخدم طاقة كيميائية لتخفيف ارتباط الحمض النووي بالبروتينات والسماح بنشاط الجينات. وعلى جانب «الإغلاق» توجد مركبات مثل NuRD، التي تشد الكروماتين وتزيل العلامات الكيميائية التي تفضّل التعبير الجيني. في نحو 20% من السرطانات، بما في ذلك أورام نادرة لكنها قاتلة تُسمى أورام رابدوايت وبعض سرطانات المبيض ذات الصلة، تُفقد أجزاء أساسية من SWI/SNF، مما يضعف بشدة جانب تنشيط الجينات من هذا التوازن.
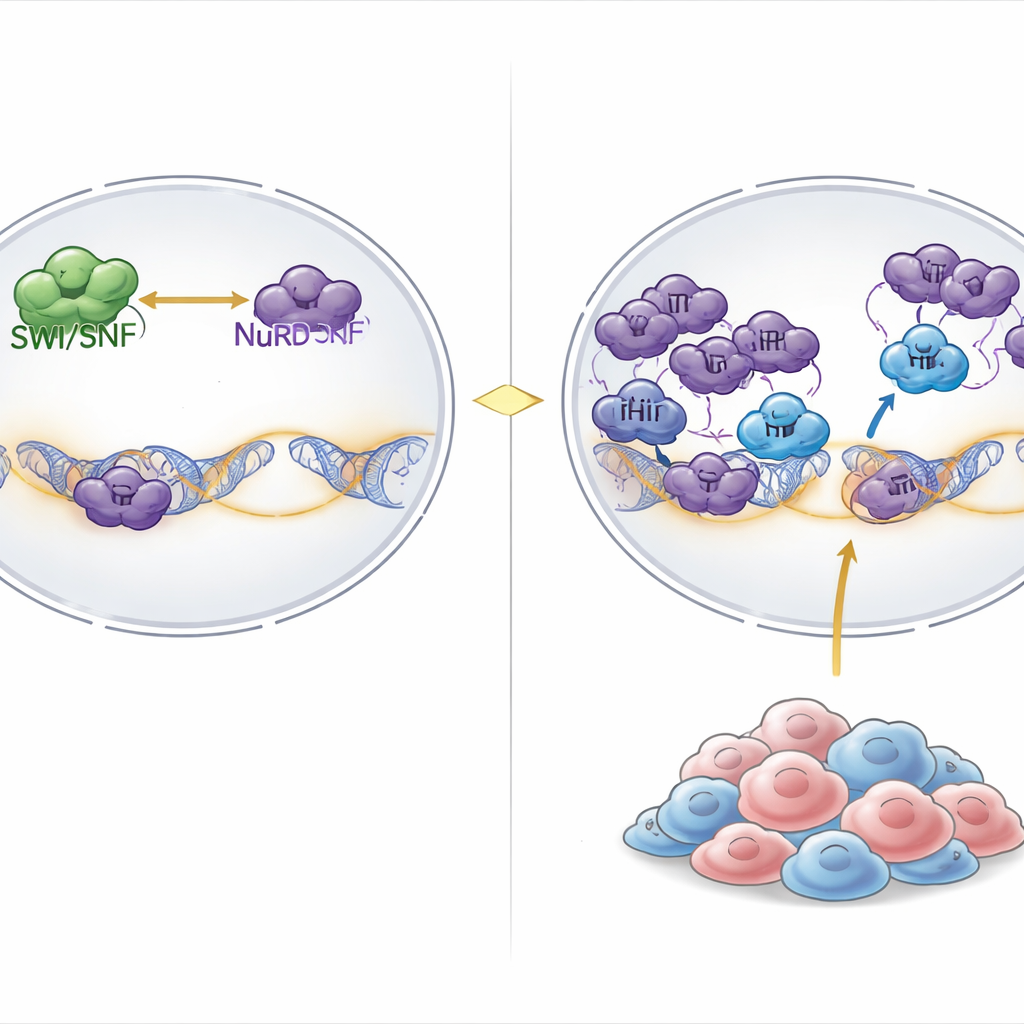
اكتشاف نقطة ضعف مخفية في الأورام ذات طفرات SWI/SNF
بحث الباحثون في نتائج شاشات تعطيل الجينات باستخدام CRISPR على مستوى الجينوم في أكثر من ألف سطر خلوي سرطاني. طرحوا سؤالاً عن أي الجينات ضرورية بشكل فريد في السرطانات التي تعاني اضطراباً واسعاً في SWI/SNF. كان أحد الاكتشافات البارزة هو PHIP، وهو بروتين مرتبط بالكروماتين سبق ربطه بتكرار الحمض النووي لكن لم يُصبح مرتبطاً بوضوح بالتحكم الجيني. عند تعطيل PHIP، تراجع نمو خلايا أورام الرابدوايت وسرطانات المبيض ذات طفرات SWI/SNF بشكل حاد، بينما تحملت معظم أنواع السرطان الأخرى فقدان PHIP. وإدخال عيوب SWI/SNF في خلايا كانت مقاومة سابقاً جعلها حساسة لفقدان PHIP، مما يبين أن الاعتماد على PHIP هو نتيجة مباشرة لخلل SWI/SNF وليس لنسج نسيج محدد.
كيف يحافظ PHIP على تشغيل جينات النمو
لفهم وظيفة PHIP، رصد الفريق مواقع وجوده على الكروماتين وكيف يتغير نشاط الجينات عند ارتفاع أو انخفاض مستوياته. تراكم PHIP بالقرب من مواقع بدء الجينات المعلمة كيميائياً كنشطة. تسبب تقليل PHIP في خفض العديد من هذه الجينات، لا سيما تلك التي تحفز انقسام الخلايا، بينما كان لتعزيز PHIP تأثير معاكس. كما ثبت أن PHIP ضروري للحفاظ على علامات أستلة محددة على الهستونات — وهي إشارات كيميائية تدل على حالة كروماتين مفتوحة ومهيأة للنقل الجيني — عند هذه المحفزات. بدون PHIP، تضاءلت الأستلة وصمتت الجينات المقابلة، متوافقاً مع دور PHIP كحارس محلي لمناطق الجينات النشطة.
PHIP كبواب لطرد مركب قمعي
يفتقر PHIP إلى نشاط إنزيمي خاص به، فساءل المؤلفون إن كان يعمل بجذب عوامل أخرى. وجدوا أن PHIP يجلب تجمّعاً إنزيمياً يُدعى ليغاز اليوبكويتين CRL4 إلى الكروماتين. يعلق هذا الليغاز علامات يوبكويتين صغيرة على بروتينات الهدف، غالباً ما يغير سلوكها أو موقعها. كشفت طيفية الكتلة والاختبارات البيوكيميائية أن مركب PHIP–CRL4 يعلِّم مباشرة أجزاءً أساسية من مركب NuRD، وبخاصّة وحدة التشكيل CHD4 المسؤولة عن إعادة التشكيل. في خلايا السرطان، كان PHIP ضرورياً لتمكين CRL4 من الارتباط بـ NuRD على الحمض النووي، مما يؤدي إلى يوبكويتنة NuRD وإزالتها من المحفزات. عند فقدان PHIP، تراكم NuRD عند مواقع بدء الجينات، انخفضت العلامات الأستيلية المحلية، وصمتت الجينات القريبة. والأهم من ذلك، أن خفض نشاط CHD4 عكس فقدان الأستلة الناجم عن تعطيل PHIP، مما يربط التأثير بنشاط إعادة تشكيل NuRD.
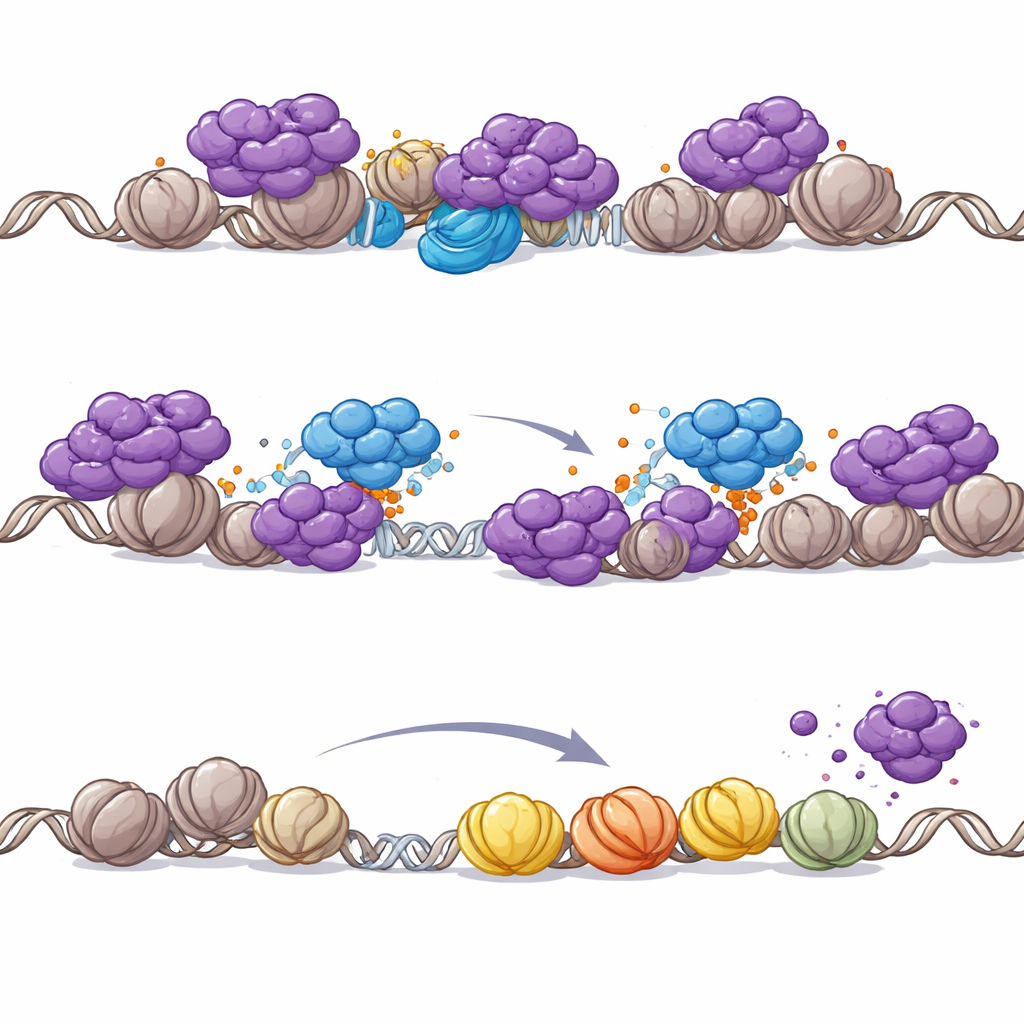
لماذا يصبح PHIP حاسماً عندما يتعطل SWI/SNF
استكشف الفريق بعد ذلك لماذا تكتسب تداخلات PHIP–NuRD أهمية خاصة في السرطانات ذات طفرات SWI/SNF. أعاد إدخال قطعة ناقصة من SWI/SNF في خلايا أورام رابدوايت تشكيل مواضع تواجد NuRD على الجينوم: انتقل NuRD بعيداً عن المحفزات ونحو مناطق المعزّزات التي أعاد SWI/SNF تنشيطها. أما عندما يغيب SWI/SNF، فيعاد توزيع NuRD إلى المحفزات، مهدداً بإغلاق واسع للجينات اللازمة للبقاء. في هذا السياق الضعيف، يصبح طرد NuRD بوساطة PHIP أمراً ضرورياً للحفاظ على التعبير الجيني المعتمد على المحفزات. وحتى في خلايا طبيعية إلى حد كبير، كانت إزالة المحركات الأساسية لـ SWI/SNF كيميائياً كافية لتحفيز إزالة NuRD المعتمدة على PHIP من الكروماتين، مما يؤكد أن دور PHIP مرتبط ارتباطاً وثيقاً بفقدان SWI/SNF.
من أطباق المختبر إلى أورام مأخوذة من المرضى
لاختبار الأهمية خارج خطوط الخلايا، لجأ الباحثون إلى أعضاء ورم دماغية مستمدة من مرضى ونماذج فأرية لأورام رابدوايت. في زرعات ثلاثية الأبعاد للنسیج الورمي مزروعة من سرطانات أطفال تحمل عيوب SWI/SNF، أدى تعطيل PHIP إلى تقليل لياقة الخلايا الورمية بشكل ملحوظ، بينما كانت الزرعات المأخوذة من سرطان دماغ ذي صلة ولا يحمل طفرات SWI/SNF غير متأثرة إلى حد كبير. عندما زُرعت الزرعات التي عُطّل فيها PHIP في أدمغة الفئران، عاشت الحيوانات لفترة أطول بكثير مقارنةً بتلك التي حوی أورام الضبط. الأورام التي انتكست لاحقاً في مجموعة تعطيل PHIP أعادت جزئياً مستويات PHIP، مما يشير إلى أن الخلايا السرطانية التي نجت من فقدان PHIP كانت هي القادرة على النمو من جديد.
ماذا يعني هذا لعلاجات السرطان المستقبلية
تكشف هذه الدراسة عن PHIP كـ«حارس شخصي» جزيئي يحمي نشاط الجينات في السرطانات حيث تتعرّض قوة التنشيط المعتادة لـ SWI/SNF للتقهقر. من خلال استقدام إنزيم الوسم لطرد المركب القمعي NuRD من المحفزات الحرجة، يمكّن PHIP الأورام ذات طفرات SWI/SNF من إبقاء جينات النمو الرئيسية مُشغّلة. ونظراً لأن معظم أنواع السرطان الأخرى — وعلى الأرجح العديد من الخلايا السليمة — لا تعتمد بقدر كبير على PHIP، فقد تُصمم أدوية تستهدف الجيب الارتباطي الفريد له لتصيب هذه الأورام الضعيفة بشكل أقوى من الأنسجة الصحية. وبينما تظل مثل هذه العلاجات بحاجة إلى التطوير والاختبار السريري، ترسم الدراسة أساساً آلياً واضحاً لتوجيه استهداف PHIP كاستراتيجية جديدة ضد بعض أكثر السرطانات ذات طفرات SWI/SNF تحدياً.
الاستشهاد: Malone, H.A., Myers, J.A., Gruss, E.G. et al. PHIP suppresses NuRD to enable the growth of SWI/SNF-mutant cancers. Nat Commun 17, 2877 (2026). https://doi.org/10.1038/s41467-026-70699-3
الكلمات المفتاحية: علاج سرطاني إبجينيتيكي, طفرات SWI/SNF, مركب NuRD, إعادة تشكيل الكروماتين, أورام رابدوايت