Clear Sky Science · pl
PHIP tłumi kompleks NuRD, umożliwiając wzrost nowotworów z mutacjami SWI/SNF
Dlaczego to badanie ma znaczenie dla onkologii
Nowotwory często powstają, gdy mechanizmy komórkowe sterujące włączaniem i wyłączaniem genów zawodzą. Artykuł bada, w jaki sposób mniej znane białko o nazwie PHIP pomaga przetrwać niektórym wysoce agresywnym nowotworom dziecięcym i jajnika oraz dlaczego blokowanie PHIP może dać nowy, selektywny sposób leczenia guzów, dla których obecnie jest niewiele dobrych opcji.
Szarpanina o DNA
W komórkach DNA owija się wokół białkowych „szpulek”, tworząc chromatynę, a duże maszyny molekularne nieustannie przesuwają ten układ, by otwierać geny do aktywności lub je zamykać. Jednym z głównych „otwierających” układów jest kompleks SWI/SNF, który zużywa energię chemiczną, aby poluzować DNA i umożliwić aktywność genów. Po stronie „zamykającej” działają komplexy takie jak NuRD, które uszczelniają chromatynę i usuwają chemiczne znaczniki sprzyjające ekspresji genów. W około 20% nowotworów, w tym w rzadkich, ale śmiertelnych guzach zwanych guzami rabdoidalnymi i w powiązanych nowotworach jajnika, utrata kluczowych elementów SWI/SNF osłabia znacząco stronę aktywującą w tym równoważeniu.
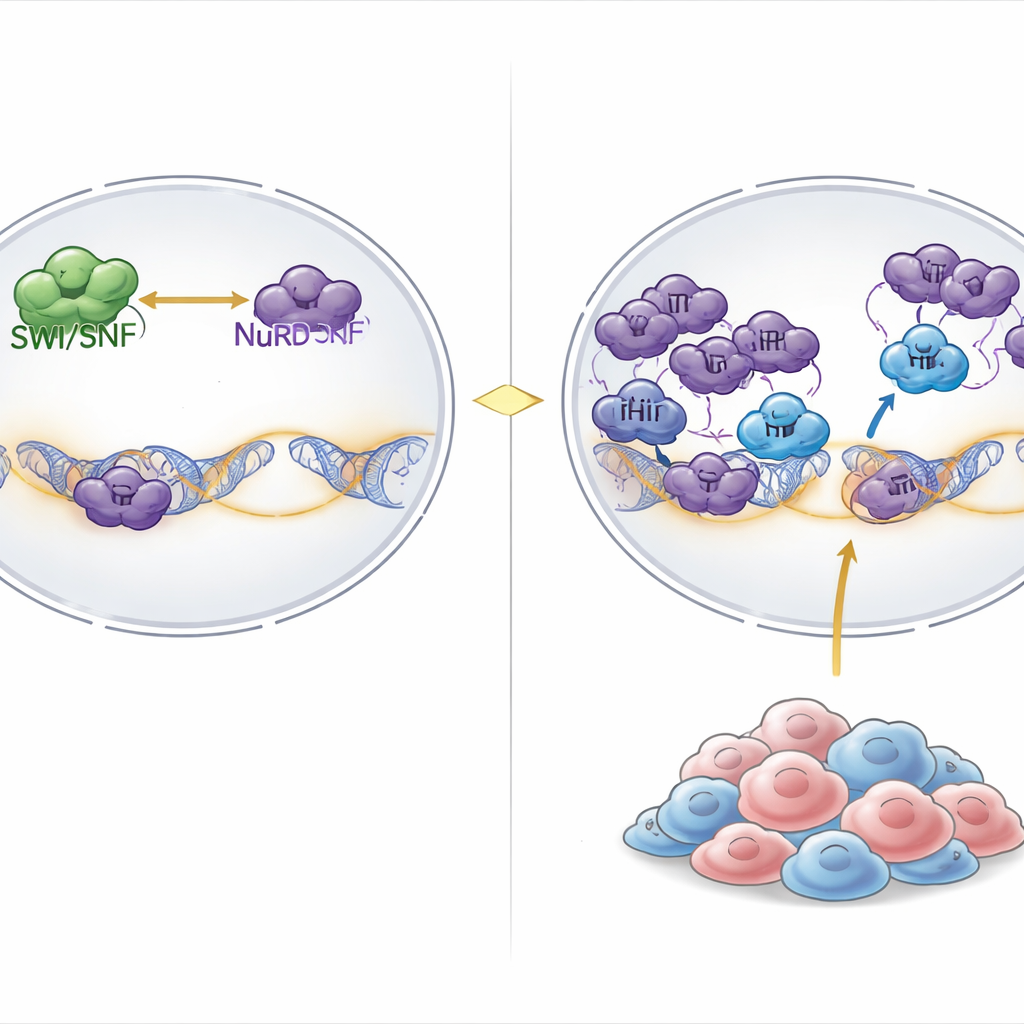
Odnalezienie ukrytej słabości w guzach z mutacjami SWI/SNF
Naukowcy przeanalizowali wyniki szeroko zakrojonych badań CRISPR z użyciem wyciszania genów w ponad tysiącu linii komórkowych nowotworowych. Zbadali, które geny są unikalnie niezbędne w nowotworach z rozległym zaburzeniem SWI/SNF. Jednym z wyróżniających się trafień był PHIP, białko wiążące chromatynę, wcześniej powiązane z replikacją DNA, ale niejasno związane z kontrolą genów. Gdy PHIP został unieszkodliwiony, wzrost komórek guzów rabdoidalnych i jajnika z mutacjami SWI/SNF gwałtownie spadł, podczas gdy większość innych typów nowotworów tolerowała utratę PHIP. Wprowadzenie defektów SWI/SNF do komórek normalnie odpornej linii uczyniło je wrażliwymi na utratę PHIP, co pokazuje, że zależność od PHIP jest bezpośrednią konsekwencją dysfunkcji SWI/SNF, a nie cechą tkanki.
Jak PHIP utrzymuje włączone geny wzrostu
Aby zrozumieć funkcję PHIP, zespół zmapował jego lokalizację na chromatynie i zmiany aktywności genów przy zwiększeniu lub zmniejszeniu poziomów PHIP. PHIP gromadził się w pobliżu startów genów, które były już chemicznie oznaczone jako aktywne. Redukcja PHIP prowadziła do wyciszenia wielu z tych genów, zwłaszcza regulatorów podziału komórkowego, podczas gdy zwiększenie PHIP miało odwrotny efekt. PHIP okazał się także kluczowy dla utrzymania określonych znaków acetylacji histonów — chemicznych flag sygnalizujących otwarty, sprzyjający transkrypcji stan chromatyny — na tych promotorach. Bez PHIP acetylacja zanikała, a związane geny cichły, co jest zgodne z rolą PHIP jako lokalnego strażnika aktywnych regionów genowych.
PHIP jako „bramkarz” dla represyjnego kompleksu
PHIP nie posiada własnej aktywności enzymatycznej, więc autorzy sprawdzili, czy działa przez rekrutację innych czynników. Odkryli, że PHIP przyprowadza na chromatynę zespół enzymatyczny CRL4 — ligazę ubikwitynową. Ta ligaza przyłącza małe znaczniki ubikwityny do białek docelowych, często zmieniając ich funkcję lub lokalizację. Spektrometria mas i testy biochemiczne ujawniły, że kompleks PHIP–CRL4 bezpośrednio znakował kluczowe części kompleksu NuRD, szczególnie podjednostkę remodelującą CHD4. W komórkach nowotworowych PHIP był niezbędny, aby CRL4 mógł zaangażować NuRD na DNA, co prowadziło do ubikwitynacji NuRD i jego usunięcia z promotorów. Gdy PHIP zniknął, NuRD nagromadził się przy startach genów, lokalne markery acetylacji spadły, a pobliskie geny zostały wyciszone. Co istotne, osłabienie CHD4 mogło odwrócić utratę acetylacji spowodowaną inaktywacją PHIP, co przypisuje efekt aktywności remodelującej NuRD.
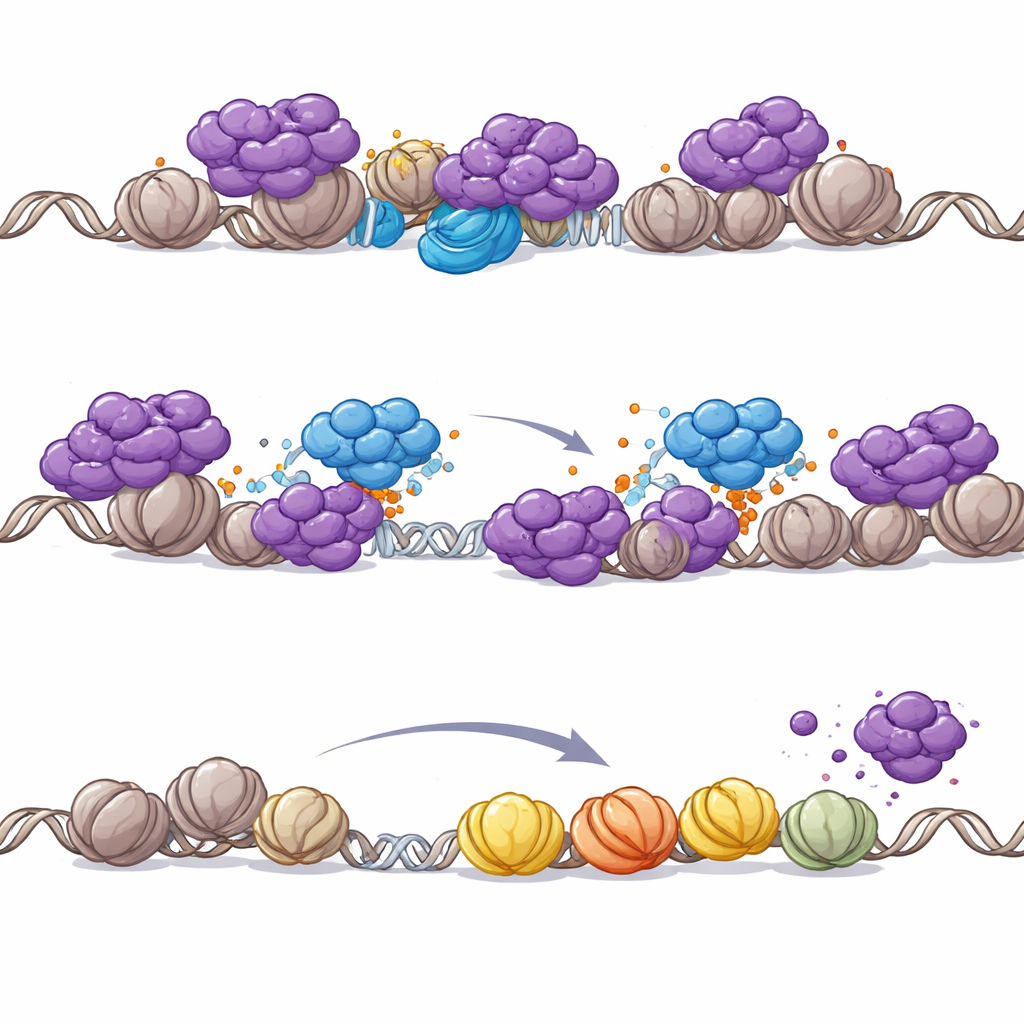
Dlaczego PHIP staje się krytyczny, gdy SWI/SNF jest uszkodzony
Zespół następnie zbadał, dlaczego interakcja PHIP–NuRD ma tak duże znaczenie szczególnie w nowotworach z mutacjami SWI/SNF. Przywrócenie brakującej podjednostki SWI/SNF w komórkach guza rabdoidalnego przekształciło rozmieszczenie NuRD w genomie: NuRD przeniósł się z promotorów w kierunku regionów enhancerowych, które zostały reaktywowane przez SWI/SNF. Jednak gdy SWI/SNF jest nieobecny, NuRD redystrybuuje się na promotory, zagrażając masowym wyłączeniem genów niezbędnych do przeżycia. W tym podatnym kontekście ewakuacja NuRD zależna od PHIP staje się niezbędna, aby utrzymać ekspresję genów inicjowaną z promotorów. Nawet w komórkach pozornie normalnych chemiczne zniszczenie podstawowych silników SWI/SNF wystarczyło, by wywołać usuwanie NuRD z chromatyny zależne od PHIP, co potwierdza ścisłe powiązanie roli PHIP z utratą SWI/SNF.
Od hodowli komórek do guzów pochodzących od pacjentów
Aby sprawdzić znaczenie poza liniami komórkowymi, badacze użyli organoidów mózgowych pochodzących od pacjentów oraz modeli mysich guzów rabdoidalnych. W trójwymiarowych hodowlach nowotworowych pochodzących z nowotworów dziecięcych z defektami SWI/SNF zakłócenie PHIP znacznie obniżało sprawność komórek nowotworowych, podczas gdy organoidy z pokrewnego nowotworu mózgu pozbawionego mutacji SWI/SNF były w dużej mierze niewrażliwe. Kiedy organoidy z wyłączonym PHIP wszczepiono do mózgów myszy, zwierzęta przeżywały znacznie dłużej niż te z kontrolnymi guzami. Guzy, które ostatecznie nawrociły w grupie z knockoutem PHIP, miały częściowo przywrócone poziomy PHIP, co wskazuje, że komórki nowotworowe, które uniknęły utraty PHIP, to te, które mogły odrosnąć.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Praca ta wskazuje PHIP jako molekularnego „ochroniarza”, który chroni aktywność genów w nowotworach, gdzie zdolność aktywująca SWI/SNF jest osłabiona. Rekrutując ligazę znakującą, aby zepchnąć represyjny kompleks NuRD z kluczowych promotorów, PHIP pozwala nowotworom z mutacjami SWI/SNF utrzymywać włączone geny napędzające wzrost. Ponieważ większość innych typów nowotworów — i przypuszczalnie wiele normalnych komórek — nie polega tak mocno na PHIP, leki blokujące jego unikalne miejsce wiążące mogłyby potencjalnie uderzać w wrażliwe guzy rabdoidalne i pokrewne znacznie silniej niż w tkanki zdrowe. Choć takie terapie muszą zostać opracowane i przetestowane klinicznie, badanie dostarcza jasnego, mechanistycznego uzasadnienia dla celowania w PHIP jako nowej strategii przeciw niektórym z najtrudniejszych nowotworów z mutacjami SWI/SNF.
Cytowanie: Malone, H.A., Myers, J.A., Gruss, E.G. et al. PHIP suppresses NuRD to enable the growth of SWI/SNF-mutant cancers. Nat Commun 17, 2877 (2026). https://doi.org/10.1038/s41467-026-70699-3
Słowa kluczowe: epigenetyczna terapia nowotworowa, mutacje SWI/SNF, kompleks NuRD, remodeling chromatyny, guzy rabdoidalne