Clear Sky Science · ru
PHIP подавляет NuRD, позволяя расти опухолям с мутациями SWI/SNF
Почему это исследование важно для онкологии
Рак часто возникает, когда механизмы клетки, отвечающие за включение и выключение генов, дают сбой. В этой работе изучают, как малоизвестный белок PHIP помогает выживанию некоторых высоко агрессивных детских и яичниковых опухолей и почему блокировка PHIP может дать новый селективный подход к лечению опухолей, для которых сейчас мало эффективных вариантов.
Перетягивание каната вокруг генетического сценария
Внутри клеток ДНК намотана на белковые котушки и формирует хроматин; крупные молекулярные машины постоянно меняют его структуру, открывая гены для работы или закрывая их. Одним из ключевых «открывающих» механизмов является комплекс SWI/SNF, который использует энергию для ослабления упаковки ДНК и допускает активацию генов. С другой стороны действуют репрессивные комплексы вроде NuRD, которые уплотняют хроматин и снимают химические метки, благоприятствующие экспрессии. Примерно в 20% случаев рака, включая редкие, но смертельно опасные рабдоидные опухоли и родственные им яичниковые опухоли, утрачиваются ключевые компоненты SWI/SNF, что серьёзно ослабляет сторону, ответственную за активацию генов.
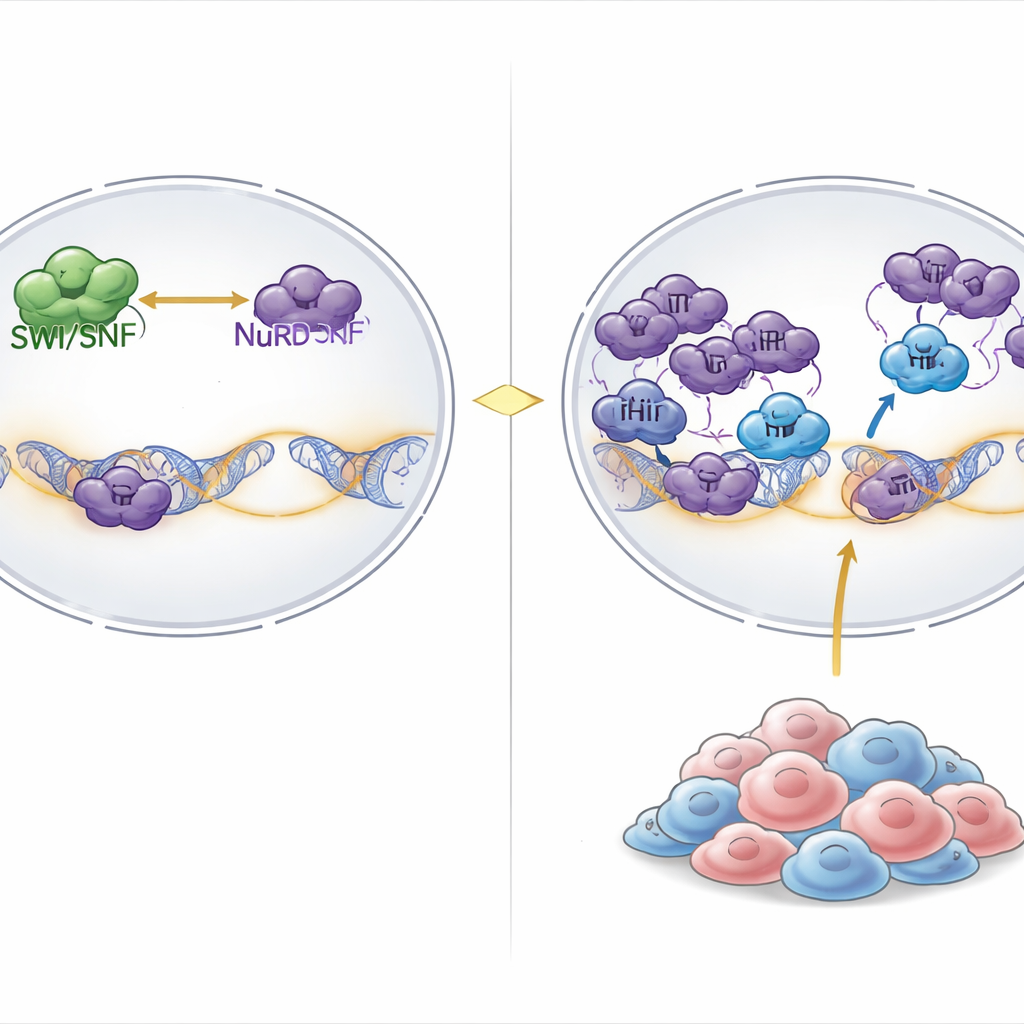
Поиск скрытой уязвимости в опухолях с мутациями SWI/SNF
Исследователи проанализировали результаты широкомасштабных CRISPR-экранов удаления генов в более чем тысяче линий раковых клеток. Они искали гены, которые оказываются исключительно необходимыми в опухолях с сильным нарушением SWI/SNF. Одним из ключевых открытий стал PHIP — белок, связывающийся с хроматином, ранее связанный с репликацией ДНК, но не явно с контролем генов. При инактивировании PHIP рост рабдоидных и яичниковых клеток с мутациями SWI/SNF резко снижался, тогда как большинство других типов рака переносило потерю PHIP. Введение дефектов SWI/SNF в обычно резистентные клетки делало их чувствительными к утрате PHIP, что показывает: зависимость от PHIP — прямое следствие нарушения SWI/SNF, а не характеристика ткани.
Как PHIP поддерживает включённость генов роста
Чтобы понять функцию PHIP, команда определила его расположение на хроматине и проследила изменения активности генов при повышении или понижении уровней PHIP. PHIP локализовался рядом с участками начала транскрипции, уже помеченными химически как активные. Снижение PHIP приводило к подавлению многих этих генов, особенно тех, что стимулируют деление клеток, тогда как увеличение PHIP давало обратный эффект. PHIP оказался важен для поддержания специфических ацетильных меток на гистонах — химических сигналов открытого, пригодного для транскрипции состояния хроматина — на этих промоторах. Без PHIP ацетилирование ослабевало, и соответствующие гены замолкали, что согласуется с ролью PHIP как локального защитника активных участков генома.
PHIP как «швейцар» для репрессивного комплекса
PHIP не обладает собственной ферментативной активностью, поэтому авторы проверили, работает ли он через привлечение других факторов. Они обнаружили, что PHIP привлекает на хроматин ферментный комплекс CRL4 — убиквитин-лигазу. Эта лигаза прикрепляет маленькие убиквитиновые метки к белкам-мишеням, часто меняя их поведение или локализацию. Мас-спектрометрия и биохимические тесты показали, что комплекс PHIP–CRL4 напрямую метит ключевые компоненты NuRD, в частности ремоделирующую субъединицу CHD4. В раковых клетках PHIP был необходим для того, чтобы CRL4 взаимодействовал с NuRD на ДНК, приводя к убиквитинированию NuRD и его удалению с промоторов. При потере PHIP NuRD накапливался на началах генов, локальные ацетильные метки падали, и близлежащие гены выключались. Важно, что снижение уровня CHD4 могло обратить потерю ацетилирования, вызванную инактивацией PHIP, указывая на то, что эффект зависит от ремоделирующей активности NuRD.
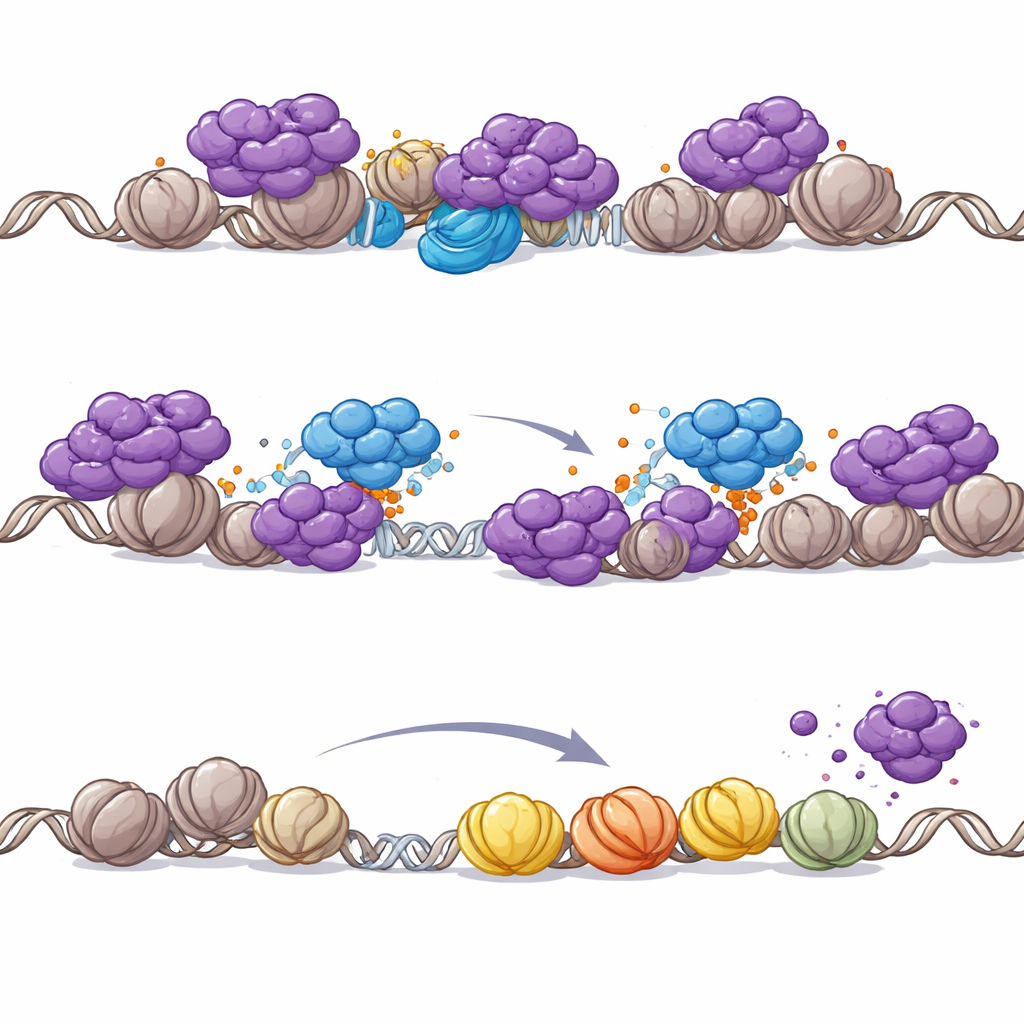
Почему PHIP становится критичным при повреждении SWI/SNF
Команда затем изучила, почему взаимодействие PHIP и NuRD особенно важно в опухолях с мутациями SWI/SNF. Восстановление отсутствующей субъединицы SWI/SNF в рабдоидных клетках изменяло распределение NuRD по геному: NuRD отодвигался от промоторов к энхансерам, повторно активированным SWI/SNF. Однако при отсутствии SWI/SNF NuRD перераспределяется на промоторы, угрожая массовым выключением генов, необходимых для выживания. В такой уязвимой ситуации изгнание NuRD, опосредованное PHIP, становится жизненно важным для поддержания экспрессии генов, управляемых промоторами. Даже в нормальных клетках химическое разрушение основных двигателей SWI/SNF было достаточно, чтобы вызвать PHIP-зависимое удаление NuRD с хроматина, что подтверждает тесную связь роли PHIP с потерей SWI/SNF.
От культур в чашках к опухолям, полученным от пациентов
Чтобы проверить значимость вне клеточных линий, исследователи обратились к органоидам мозговых опухолей, полученным от пациентов, и к мышиным моделям рабдоидных опухолей. В трёхмерных культурах опухолей, выращенных из детских опухолей с дефектами SWI/SNF, нарушение PHIP заметно снижало жизнеспособность опухолевых клеток, тогда как органоиды из родственной мозговой опухоли без мутаций SWI/SNF были в основном невоздействованы. Когда органоиды с нокаутом PHIP имплантировали в мозг мышей, животные жили значительно дольше по сравнению с теми, у кого были контрольные опухоли. Опухоли, которые в итоге рецидивировали в группе с нокаутом PHIP, частично восстанавливали уровни PHIP, что указывает на то, что клетки, избежавшие потери PHIP, были способны к повторному росту.
Что это означает для будущих методов лечения рака
Эта работа выявляет PHIP как молекулярного «телохранителя», который защищает активность генов в опухолях, где обычная активирующая роль SWI/SNF нарушена. Привлекая убиквитин-лигазу для удаления репрессивного комплекса NuRD с критических промоторов, PHIP позволяет опухолям с мутациями SWI/SNF поддерживать включённость ключевых генов роста. Поскольку большинство других типов рака — и, вероятно, многие нормальные клетки — не так сильно зависят от PHIP, препараты, нацеленные на его уникальный карман связывания, теоретически могли бы поражать уязвимые рабдоидные и родственные опухоли сильнее, чем здоровую ткань. Хотя такие терапевтические подходы ещё предстоит разработать и клинически протестировать, исследование прокладывает ясную механистическую основу для таргетирования PHIP как новой стратегии против некоторых из самых трудноподдающихся опухолей с мутациями SWI/SNF.
Цитирование: Malone, H.A., Myers, J.A., Gruss, E.G. et al. PHIP suppresses NuRD to enable the growth of SWI/SNF-mutant cancers. Nat Commun 17, 2877 (2026). https://doi.org/10.1038/s41467-026-70699-3
Ключевые слова: эпигенетическая терапия рака, мутации SWI/SNF, комплекс NuRD, ремоделирование хроматина, рабдоидные опухоли