Clear Sky Science · tr
Dinamik althücre proteomikleri, adiposit insulin etkisini düzenleyenleri tanımlar
Günlük sağlık açısından neden önemli
İnsülin, kan şekerini kontrol altında tutmasıyla bilinen bir hormondur; görevini yapamadığında tip 2 diyabet gibi durumlar gelişebilir. Bu çalışma, yağ hücrelerinin içinde, insülin geldiğinde binlerce proteinin konumlarının nasıl ve ne kadar hızlı değiştiğini benzersiz bir ayrıntı düzeyinde inceliyor. Bu moleküler yeniden dağılımı izleyerek, araştırmacılar yağ hücrelerinin insüline doğru yanıt vermesine yardımcı olan yeni oyuncuları ortaya koyuyor ve insülinin bazen neden düzgün çalışmayı bıraktığına dair yeni ipuçları sunuyor.
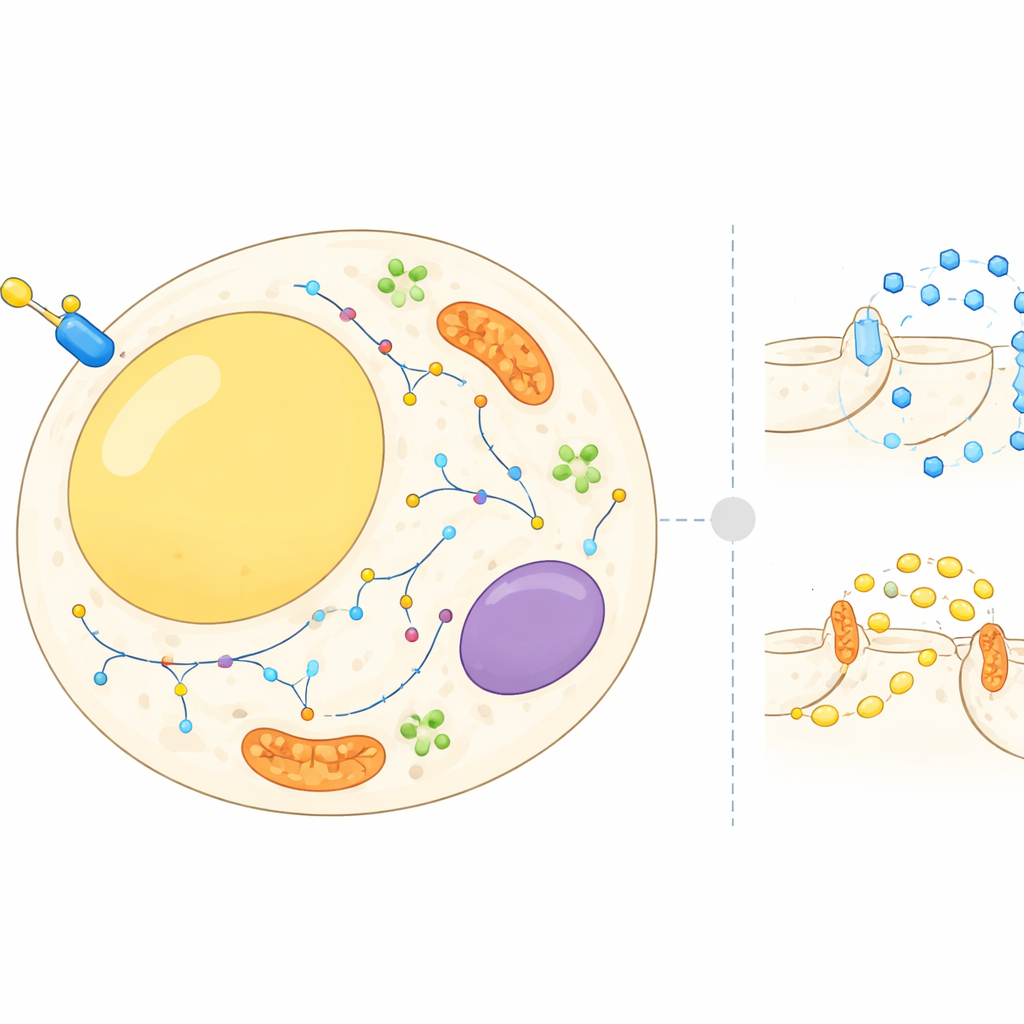
Yağ hücrelerinin içindeki hareketli harita
Yağ hücreleri yalnızca pasif depolama birimleri değildir; hormonlara ve besinlere yanıt olarak enerji depolamak ve serbest bırakmak arasında sürekli bir denge kurarlar. İnsülin bu hücrelere kandaki şekeri çekmelerini ve depolanmış yağın parçalanmasını yavaşlatmalarını söyler. Bunu yapmak için, birçok proteinin hücre yüzeyi, iç membranlar ve küçük taşıyıcı veziküller gibi farklı hücresel bölümler arasında hareket etmesi gerekir. Şimdiye kadar çoğu araştırma birkaç iyi bilinen proteine odaklanmıştı. Bu çalışmada yazarlar, bir insülin patlamasından önce ve sonra binlerce proteinin yağ hücrelerinde nerede bulunduğuna ve konumlarının dakikalar içinde nasıl değiştiğine dair hücre genelinde bir atlas oluşturmayı hedeflediler.
Protein manzarası nasıl haritalandı
Ekip, althücre proteomikleri adı verilen; hücre fraksiyonasyonu ve kütle spektrometrisini birleştirerek proteinleri hücrenin farklı bölümlerinde aynı anda ölçen bir yaklaşım kullandı. Standart bir fare yağ hücresi modeli olan 3T3-L1 hücreleri ile çalıştılar ve her örneği hücre yüzeyi, enerji fabrikaları, geri dönüşüm kompartmanları ve yağ damlacıkları gibi yapılarda zenginleştirilmiş birden çok fraksiyona ayırdılar. Bir istatistiksel çerçeve daha sonra dinlenme halindeki hücreler ile insülinle uyarılmış hücreler arasındaki her bir proteinin dağılımını karşılaştırdı. Paralel olarak, araştırmacılar hücrenin dış yüzeyine maruz kalan proteinleri seçici olarak etiketleyen ayrı bir yöntem de kullandılar; bu yöntem, insülin tedavisinden sonra her bir yüzey proteininin miktarının ne kadar arttığını veya azaldığını nicelendirilebilmelerini sağladı.
İnsülin geniş çaplı protein yeniden dağılımını tetikliyor
Birleştirilmiş veri setleri, insülinin çarpıcı bir yeniden düzenlemeyi tetiklediğini ortaya koydu: 500’den fazla protein konumunda yüksek güvenle değişiklik gösterdi. Birçoğu besinleri algılayan ve büyümeyi düzenleyen bileşenler de dahil olmak üzere bilinen sinyal yolaklarına aitti; ayrıca diğer proteinleri açıp kapatan protein kinazları da vardı. Diğerleri, molekülleri iç bölmeler ile hücre yüzeyi arasında taşıyan yük taşıyan veziküllerin trafiği ile ilişkiliydi. Bazı taşıma kompleksleri insüline yanıt olarak belirgin şekilde yer değiştirdi, bazıları ise yerinde kaldı; bu durum hormonun hücrenin taşıma ağının belirli dallarını hedeflediğini düşündürüyor. Yüzeye odaklanan deneyler, dış membrandaki 300’den fazla proteinin bolluğunun değiştiğini göstererek hücrenin çevresi ile olan “ara yüzünün” insülin yanıtı sırasında yeniden şekillendiğini doğruladı.
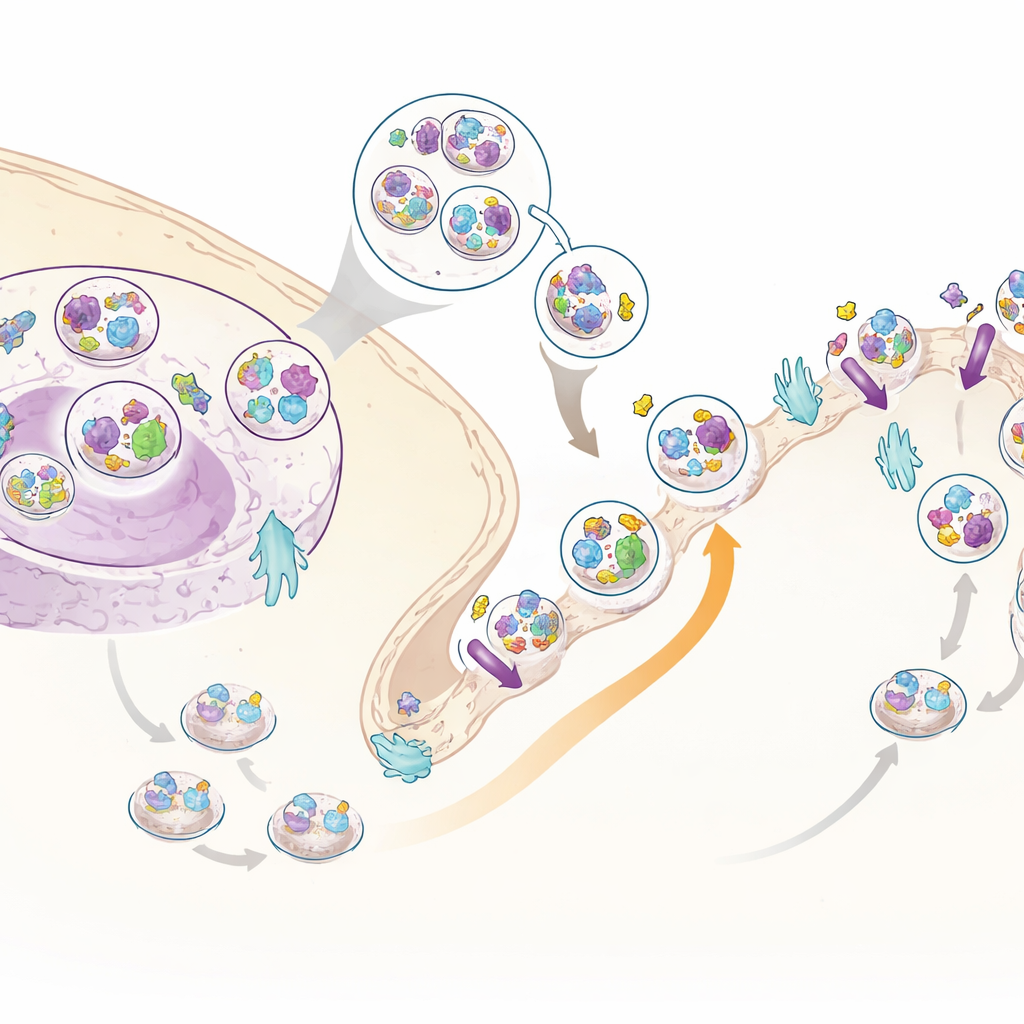
Yeni bir insülin yardımcısı: C3ORF18
Hareket eden birçok protein arasından öne çıkan biri az çalışılmış bir protein olan C3ORF18 idi. Hem hücre-geneli hem de yüzeye özgü veri setlerinde insülin tarafından güçlü şekilde hücre yüzeyine çekildi. Mikroskopi, C3ORF18’in hücrenin merkezine yakın ve küçük veziküllerde bulunduğunu, bunların birçoğunun iyi bilinen bir geri dönüşüm proteini olan transferrin reseptörünü taşıyan veziküller ve ana şeker taşıyıcı GLUT4 ile örtüştüğünü gösterdi. İnsülin veya büyüme faktörleri eklendiğinde C3ORF18 hızla GLUT4’ün kullandığı aynı sinyal dalına bağımlı olarak hücre yüzeyine hareket etti. Bu davranış, C3ORF18’in önemli taşıyıcıları zar yüzeyine ulaştırmaya yardımcı olan insüline duyarlı bir geri dönüşüm yolunda seyahat ettiğini öne sürüyor.
Yeni oyuncu eksik olunca ne oluyor
C3ORF18’in sadece eşlik etmekten öte bir işlevi olup olmadığını test etmek için araştırmacılar olgun fare ve insan yağ hücrelerinde seviyelerini seçici olarak azalttılar. Birkaç gün içinde C3ORF18 eksik hücreler insüline daha az duyarlı hale geldi: şeker alımı düştü ve hem GLUT4 hem de başka bir şeker taşıyıcı olan GLUT1 daha az bulundu. GLUT4 ve transferrin reseptörünün yüzeye insülinle yönlendirilmesi de zayıfladı ve insülin reseptörünün aşağısındaki temel sinyal adımları zayıfladı. C3ORF18 azalımının erken döneminde sorunlar önce transferrin reseptörlerinin geri dönüşümünde ortaya çıktı; bu da endosomal geri dönüşümdeki bozulmaların nihayetinde insülinin daha geniş etkilerini zayıflatan başlangıç noktası olabileceğine işaret ediyor. İnsan yağ dokusundan elde edilen veriler de bu görüşü destekledi: daha yüksek kan şekeri ve uzun dönem glukoz göstergelerine sahip kişilerde C3ORF18 ifadesi eğilimle daha düşük bulunuyordu ve kilo kaybıyla seviyeleri yükseliyordu.
İnsülin duyarlılığını anlamak için büyük resmi çıkarımlar
Bu çalışma, yağ hücrelerinde başarılı bir insülin yanıtının yalnızca hangi proteinlerin mevcut olmasına değil, aynı zamanda bu proteinlerin hücrenin herhangi bir anında nerede bulunduğuna da bağlı olduğunu gösteriyor. İnsülin kısa sürede yüzlerce proteini, özellikle hücre yüzeyinde ve geri dönüşüm kompartmanlarında yeniden dağıtıyor ve bu konum değişiklikleri fosforilasyon gibi kimyasal değişikliklerle birlikte çalışıyor. Bu hareketi sistematik şekilde haritalayarak yazarlar, verimli şeker alımı ve sağlıklı insülin sinyallemesini destekleyen geri dönüşüm yollarına yardımcı olan daha önce tanınmamış bir oyuncu olan C3ORF18’i keşfettiler. Bu tür mekânsal dinamikleri anlamak, metabolik hastalıkta insülin duyarlılığının neden zayıfladığını araştırmak için yeni yollar açıyor ve nihayetinde bu kritik hormon yanıtını korumaya veya geri kazanmaya yönelik hedeflere işaret edebilir.
Atıf: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
Anahtar kelimeler: insülin direnci, adiposit, protein taşınması, mekânsal proteomik, glukoz alımı