Clear Sky Science · he
פרוטאומיקה תת-תאית דינמית מזהה רגולטורים של תגובת האינסולין בתא שומן
מדוע זה חשוב לבריאות היומיומית
אינסולין הוא הורמון שמוכר בעיקר בכך שהוא שומר על רמת הסוכר בדם בטווח תקין, וכאשר הוא מפשל עלולות להתפתח מצבים כמו סוכרת מסוג 2. המחקר הזה בוחן את התא השומני מבפנים ורואה, בפירוט חסר תקדים, כיצד אלפי חלבונים מזיזים את מקומם במהירות כשהאינסולין מגיע. על ידי מעקב אחרי השינוי המולקולרי הזה, החוקרים חושפים שחקנים חדשים שעוזרים לתאי השומן להגיב כראוי לאינסולין, ומספקים רמזים חדשים מדוע לעיתים אינסולין מפסיק לפעול כמו שצריך.
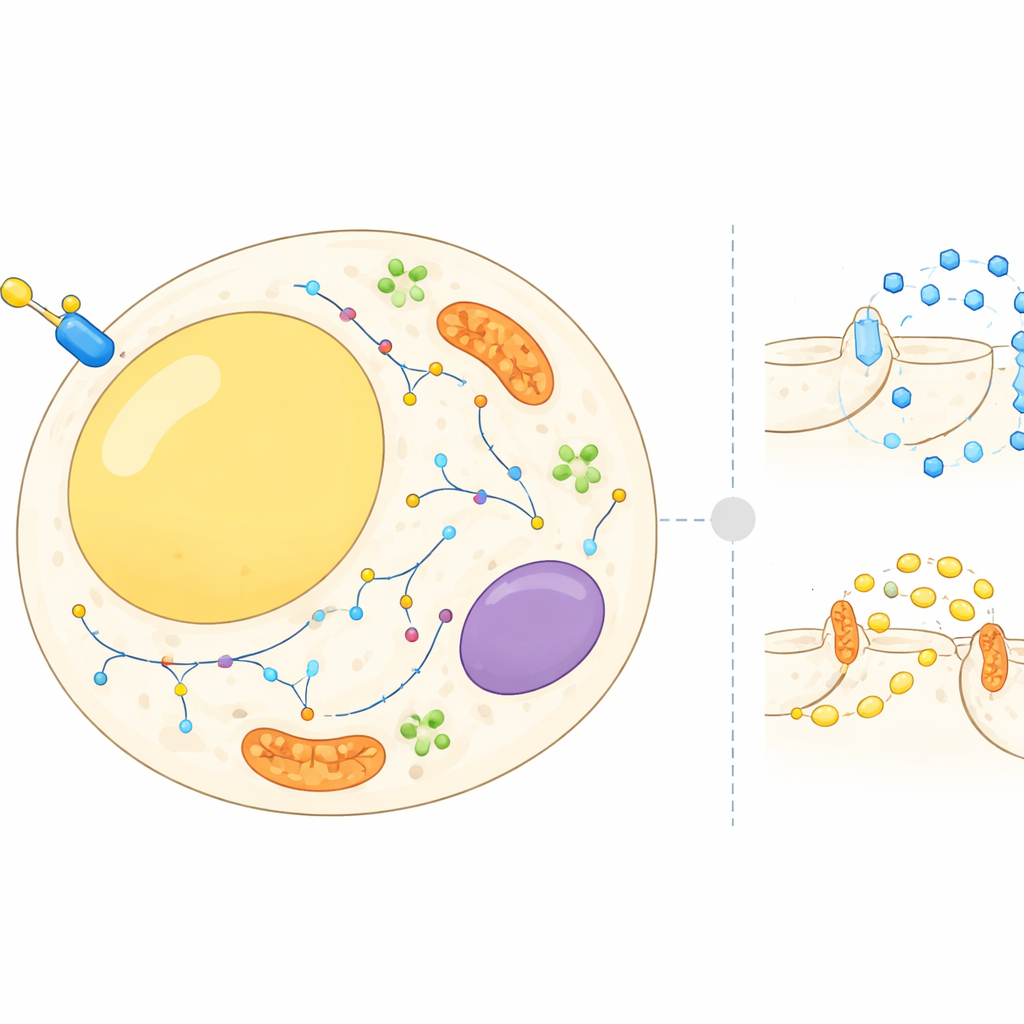
מפה נעה בתוך תאי השומן
תאי שומן הם לא רק מחסני אנרגיה פסיביים; הם מאזנים ללא הרף בין אגירה ושחרור של אנרגיה בתגובה להורמונים ולמצבי תזונה. אינסולין מורה לתאים אלה לשאוב סוכר מהדם ולבלום את פירוק השומן המאוחסן. כדי לעשות זאת, חלבונים רבים חייבים לנוע בין קומפלקסים תאיים שונים, כמו הממברנה החיצונית, ממברנות פנימיות וכיסים נשאיים זעירים. עד כה המחקר התמקד בעיקר בכמה חלבונים מוכרים. בעבודה זו המחברים שאפו לבנות אתלאס תאי רחב היקף של מיקומי אלפי חלבונים בתאי שומן לפני ואחרי פיצוץ אינסולין, וכיצד מיקומם משתנה בתוך דקות.
איך נשרטטה נוף החלבונים
הצוות השתמש בגישה שנקראת פרוטאומיקה תת-תאית, שמשלבת שבר תאי ומסת מסה כדי למדוד חלבונים בחלקים שונים של התא במקביל. הם עבדו עם תאי 3T3-L1, מודל עכברי סטנדרטי לתאי שומן, והפרידו כל דגימה למספר חלקים המעוררים מבנים כמו המשטח החיצוני של התא, תחנות האנרגיה, מחלקות הממחזרות וטיפות השומן. מסגרת סטטיסטית השוותה לאחר מכן את התפלגות כל חלבון בתאים במצבי רגיעה מול תאים מוסטימולוּת באינסולין. במקביל השתמשו החוקרים בשיטה נוספת שסימנה באופן סלקטיבי חלבונים החשופים על פני התא החיצוניים, מה שאיפשר לכמת כמה מכל חלבון בממברנה החיצונית עלה או ירד אחרי טיפול באינסולין.
אינסולין מעורר מהפכה רחבת היקף בחלבונים
המערכות המשולבות חשפו כי אינסולין מצית ארגון מחודש מרשים: יותר מ-500 חלבונים הראו שינויים ברמת ביטחון גבוהה במיקומם. רבים שויכו למסלולי איתות ידועים, כולל רכיבים החשים נוטריינטים ומווסתים גדילה, וכן קינאזות שמכבות או מדליקות חלבונים אחרים. אחרים היו מעורבים בתנועה של וזיקולות נשאיות מטען שמשנעות מולקולות בין מחלקות פנימיות למשטח התא. קומפלקסים מסוימים של הובלה הראו תנועה בולטת בתגובה לאינסולין, בעוד שאחרים נשארו במקום, מה שמעיד כי ההורמון פונה לענפים ספציפיים ברשת התחבורה התאית. הניסויים הממוקדים במשטח הראו כי למעלה מ-300 חלבונים השתנו בשפעם בממברנה החיצונית, ואישרו כי ה"ממשק" של התא עם סביבתו משתנה במהלך תגובת אינסולין.
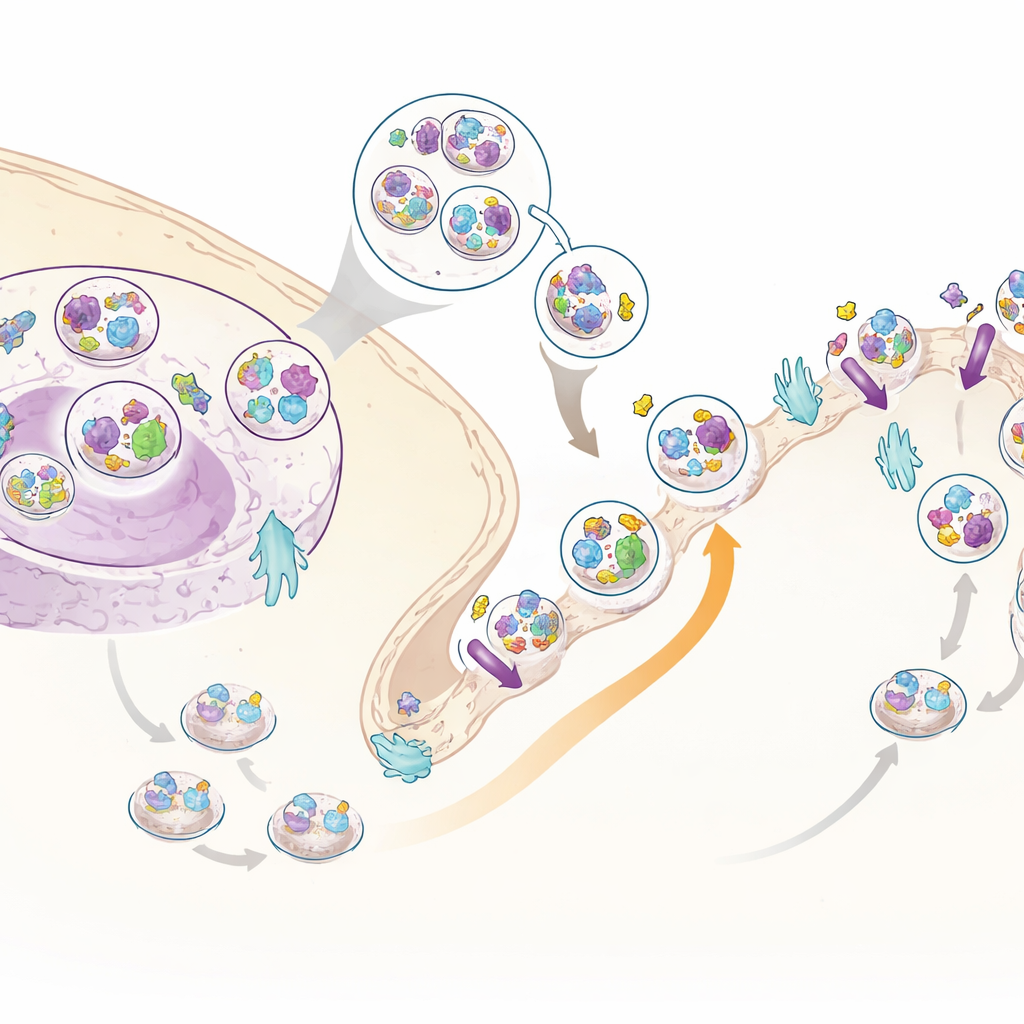
עוזר חדש לאינסולין: C3ORF18
מבין החלבונים הרבים שנעו, אחד בלט במיוחד: חלבון שעוד לא נחקר רבות בשם C3ORF18. הוא נמשך בחוזקה לעבר משטח התא על ידי אינסולין הן בנתוני התא השלם והן בנתוני המשטח הספציפי. מיקרוסקופיה הראתה כי C3ORF18 ישב בקרבת מרכז התא ובוזיקולות קטנות, רבות מהן חופפות לאלה שנושאות את קולטני הטרנספרין, חלבון מחזורי ידוע, ול-GLUT4, נשא סוכר מרכזי. כשנוספו אינסולין או גורמי גדילה, C3ORF18 נדד במהירות למשטח התאי בצורה שתלויה בענף האיתות המשמש גם את GLUT4. התנהגות זו מרמזת ש-C3ORF18 נוסע במסלול מיחזור הרגיש לאינסולין שעוזר להעביר נשאים חשובים לממברנה.
מה קורה כשחסר השחקן החדש
כדי לבדוק האם C3ORF18 עושה יותר מללוות, החוקרים הפחיתו באופן סלקטיבי את רמתו בתאי שומן בוגרים של עכברים ובני אדם. במשך מספר ימים, תאים חסרי C3ORF18 הפכו לפחות רגישים לאינסולין: קליטת הסוכר ירדה, ושני נשאים מרכזיים — GLUT4 ונשא נוסף GLUT1 — היו בעדינות פחות שופעים. תנועת GLUT4 וקולטני הטרנספרין למשטח שהונעה על ידי אינסולין נחלשה גם היא, ושלבי איתות מרכזיים אחרי קולטן האינסולין נחלשו. מוקדם אחרי דילול C3ORF18 הופיעו בעיות תחילה במחזור קולטני הטרנספרין, מה שמרמז שהפרעות במיחזור האנדוזומלי עשויות להיות הנקודה ההתחלתית שמאוחר יותר מחלישה את השפעות האינסולין הרחבות יותר. נתונים מרקמה שומנית אנושית תמכו גם הם בתמונה: אנשים עם רמות סוכר גבוהות בדם וסמנים כרוניים גבוהים של גלוקוז נטו לבטא פחות C3ORF18, ורמותיו עלו באובדן משקל.
מסקנות ברמת התמונה הרחבה להבנה של רגישות לאינסולין
המחקר מראה כי תגובת אינסולין מוצלחת בתאי שומן תלויה לא רק באילו חלבונים קיימים, אלא גם באיפה הם נמצאים בתא בכל רגע נתון. אינסולין מפזר במהירות מאות חלבונים, במיוחד על פני הממברנה החיצונית ובמחלקות המיחזור, והשינויים במיקום אלה פועלים לצד שינויים כימיים כמו פוספורילציה. על ידי מיפוי מערכתי של תנועה זו, המחברים גילו את C3ORF18 כעוזר בלתי-מוכר קודם שתומך במסלולי המיחזור הנחוצים לקליטת סוכר יעילה ולאיתות אינסוליני בריא. הבנת דינמיקות מרחביות כאלה פותחת דרכים חדשות לחקור מדוע רגישות לאינסולין נשחקת במחלות מטבוליות, ועשויה בסופו של דבר להצביע על מטרות לשימור או לשיקום תגובת ההורמון החיונית הזו.
ציטוט: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
מילות מפתח: עמידות לאינסולין, תא שומן, תנועת חלבונים, פרוטאומיקה מרחבית, קליטת גלוקוז