Clear Sky Science · pt
Proteômica subcelular dinâmica identifica reguladores da ação da insulina em adipócitos
Por que isso importa para a saúde cotidiana
A insulina é um hormônio mais conhecido por controlar o nível de açúcar no sangue e, quando falha, condições como o diabetes tipo 2 podem se desenvolver. Este estudo examina o interior das células de gordura para ver, com detalhes inéditos, como milhares de proteínas mudam rapidamente de posição quando a insulina chega. Ao rastrear esse reorganização molecular, os pesquisadores revelam novos atores que ajudam os adipócitos a responder adequadamente à insulina, oferecendo pistas novas sobre por que a insulina às vezes deixa de funcionar como deveria.
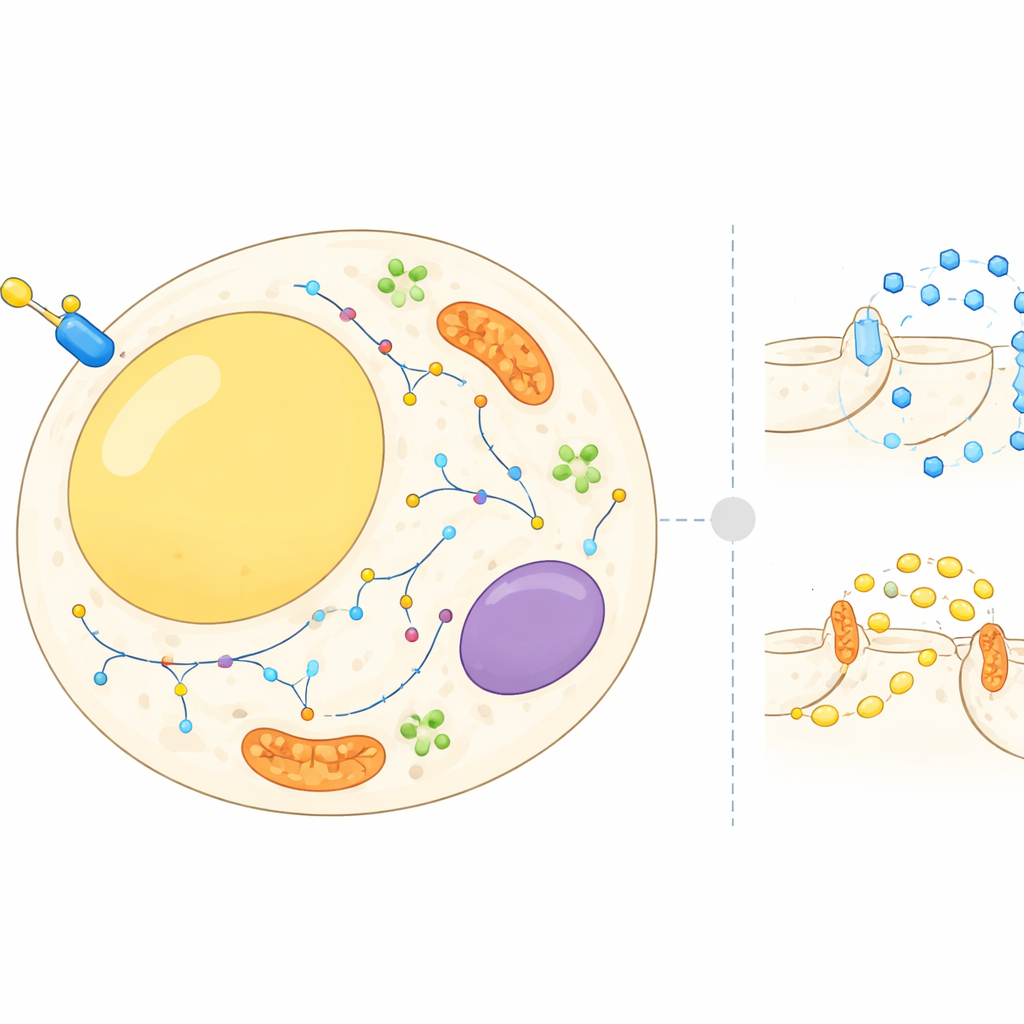
Um mapa em movimento dentro dos adipócitos
As células de gordura não são apenas depósitos passivos; elas equilibram continuamente o armazenamento e a liberação de energia em resposta a hormônios e nutrientes. A insulina diz a essas células para retirar açúcar da corrente sanguínea e reduzir a degradação da gordura armazenada. Para isso, muitas proteínas precisam se deslocar entre diferentes compartimentos celulares, como a superfície celular, membranas internas e pequenas vesículas de transporte. Até agora, a maior parte das pesquisas se concentrou em algumas proteínas bem conhecidas. Neste trabalho, os autores procuraram construir um atlas celular de onde milhares de proteínas se localizam em adipócitos antes e depois de um pico de insulina, e como suas posições mudam em questão de minutos.
Como o panorama proteico foi mapeado
A equipe usou uma abordagem chamada proteômica subcelular, que combina fracionamento celular e espectrometria de massa para medir proteínas em diferentes partes da célula ao mesmo tempo. Trabalharam com células 3T3-L1, um modelo padrão de adipócitos de camundongo, e separaram cada amostra em múltiplas frações enriquecidas para estruturas como a superfície celular, fábricas de energia, compartimentos de reciclagem e gotículas de gordura. Um arcabouço estatístico comparou então a distribuição de cada proteína em células em repouso versus células estimuladas com insulina. Em paralelo, os pesquisadores usaram um método separado que marcou seletivamente proteínas expostas na superfície externa da célula, permitindo quantificar quanto de cada proteína de superfície aumentou ou diminuiu após o tratamento com insulina.
A insulina provoca uma ampla reorganização proteica
Os conjuntos de dados combinados revelaram que a insulina desencadeia uma reorganização marcante: mais de 500 proteínas apresentaram deslocamentos de localização com alta confiança. Muitas pertenciam a vias de sinalização conhecidas, incluindo componentes que detectam nutrientes e regulam o crescimento, assim como quinases que ligam ou desligam outras proteínas. Outras estavam envolvidas no tráfego de vesículas que transportam cargas entre compartimentos internos e a superfície celular. Alguns complexos de transporte deslocaram-se visivelmente em resposta à insulina, enquanto outros permaneceram estáticos, sugerindo que o hormônio mira ramos específicos da rede de transporte da célula. Os experimentos focados na superfície mostraram que mais de 300 proteínas mudaram em abundância na membrana externa, confirmando que a “interface” da célula com o ambiente é remodelada durante a resposta à insulina.
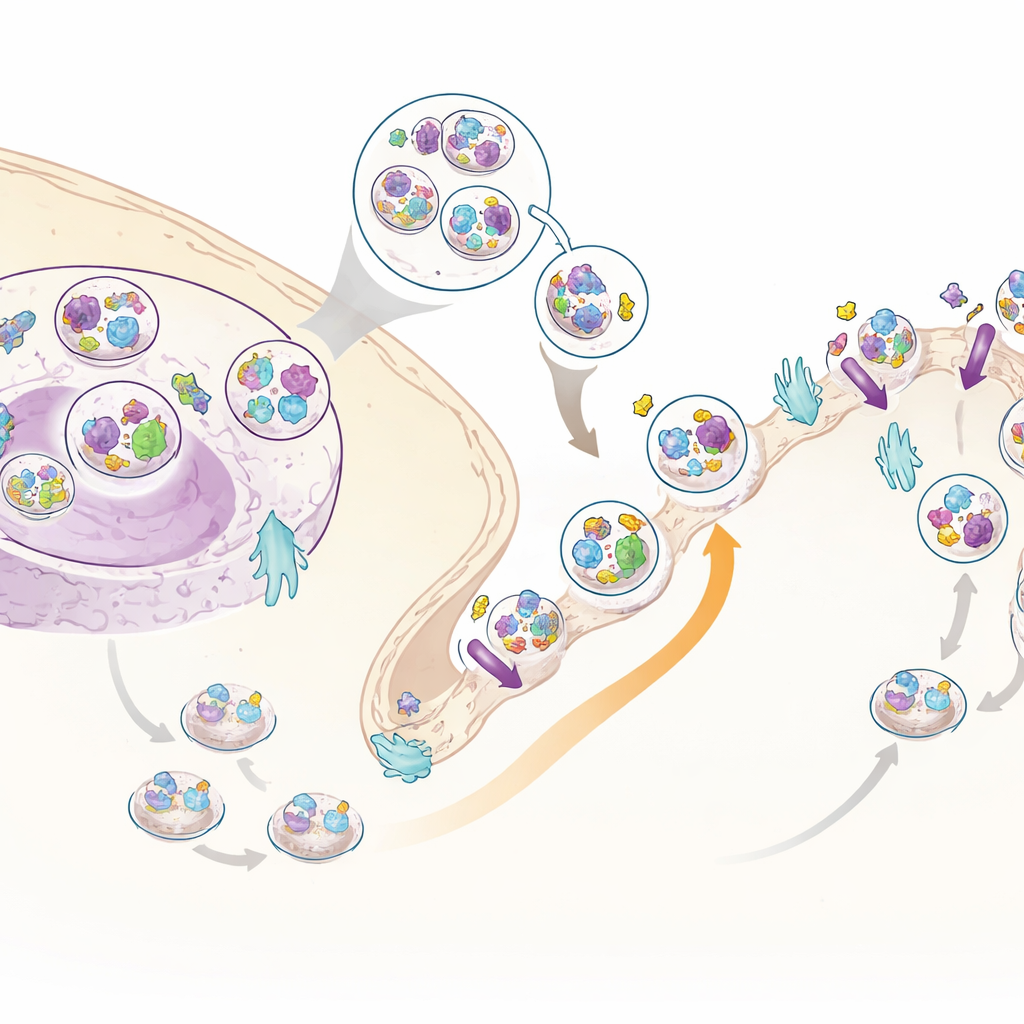
Um novo auxiliar da insulina: C3ORF18
Entre as muitas proteínas em movimento, uma se destacou: uma proteína pouco estudada chamada C3ORF18. Ela foi fortemente direcionada para a superfície celular pela insulina, tanto nos conjuntos de dados de célula inteira quanto nos específicos de superfície. Microscopia mostrou que a C3ORF18 se localiza perto do centro da célula e em pequenas vesículas, muitas das quais se sobrepõem às que carregam o receptor de transferrina, uma proteína de reciclagem bem conhecida, e ao GLUT4, um transportador de glicose chave. Quando insulina ou fatores de crescimento foram adicionados, a C3ORF18 moveu-se rapidamente para a superfície celular de uma forma dependente do mesmo ramo de sinalização usado pelo GLUT4. Esse comportamento sugere que a C3ORF18 trafega por uma rota de reciclagem sensível à insulina que ajuda a levar transportadores importantes até a membrana.
O que acontece quando o novo ator está ausente
Para testar se a C3ORF18 faz mais do que apenas acompanhar, os pesquisadores reduziram seletivamente seus níveis em adipócitos maduros de camundongo e humanos. Ao longo de vários dias, células sem C3ORF18 tornaram-se menos responsivas à insulina: a captação de açúcar caiu, e tanto o GLUT4 quanto outro transportador de glicose, o GLUT1, estavam em menor abundância. O movimento induzido pela insulina do GLUT4 e do receptor de transferrina para a superfície também foi atenuado, e etapas centrais da sinalização a jusante do receptor de insulina ficaram enfraquecidas. Logo após a depleção de C3ORF18, problemas apareceram primeiro na reciclagem dos receptores de transferrina, sugerindo que perturbações na reciclagem endossomal podem ser o ponto de partida que eventualmente compromete os efeitos mais amplos da insulina. Dados de tecido adiposo humano corroboraram essa visão: pessoas com glicemia mais alta e marcadores de glicose de longo prazo tendiam a ter expressão menor de C3ORF18, e seus níveis aumentaram com a perda de peso.
Principais conclusões para entender a sensibilidade à insulina
Este estudo mostra que uma resposta bem-sucedida à insulina em adipócitos depende não apenas de quais proteínas estão presentes, mas também de onde elas se encontram na célula em cada momento. A insulina redistribui rapidamente centenas de proteínas, especialmente na superfície celular e em compartimentos de reciclagem, e essas mudanças de localização atuam em conjunto com modificações químicas como a fosforilação. Ao mapear sistematicamente esse movimento, os autores descobriram a C3ORF18 como um auxiliar até então não reconhecido que sustenta as rotas de reciclagem necessárias para uma captação eficiente de glicose e uma sinalização insulínica saudável. Compreender essa dinâmica espacial abre novas vias para explorar por que a sensibilidade à insulina se deteriora em doenças metabólicas e pode, eventualmente, apontar para alvos para preservar ou restaurar essa resposta hormonal crucial.
Citação: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
Palavras-chave: resistência à insulina, adipócito, transporte de proteínas, proteômica espacial, captação de glicose