Clear Sky Science · de
Dynamische subzelluläre Proteomik identifiziert Regulatoren der Insulinwirkung in Adipozyten
Warum das für die tägliche Gesundheit wichtig ist
Insulin ist ein Hormon, das vor allem dafür bekannt ist, den Blutzucker zu regulieren; versagt diese Regulation, können Erkrankungen wie Typ-2-Diabetes entstehen. Diese Studie blickt in bislang unerreichter Detailtiefe in Fettzellen, um zu sehen, wie Tausende von Proteinen ihre Positionen innerhalb von Minuten verändern, sobald Insulin eintrifft. Durch das Verfolgen dieses molekularen Umzugs identifizieren die Forschenden neue Akteure, die Adipozyten helfen, angemessen auf Insulin zu reagieren, und liefern damit frische Hinweise darauf, warum Insulin manchmal seine Wirkung verliert.
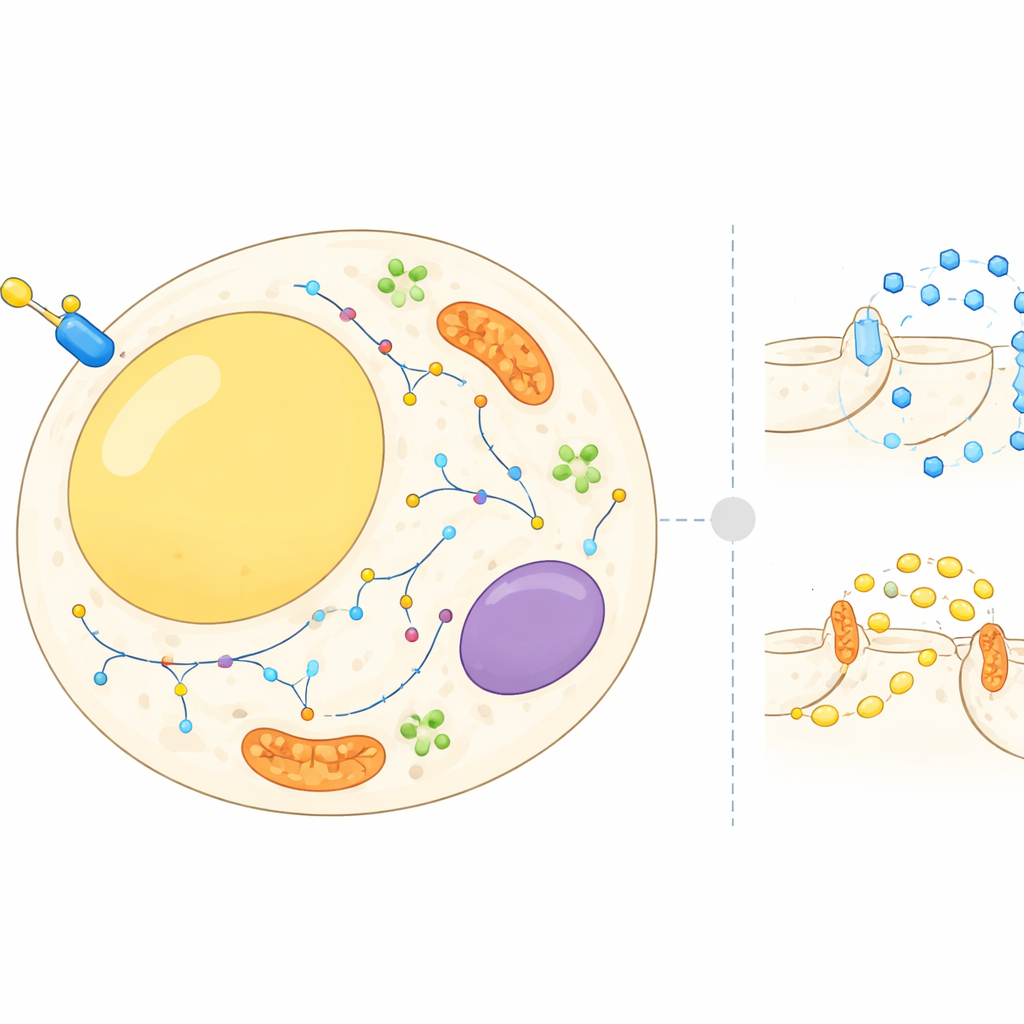
Eine bewegliche Karte innerhalb der Fettzelle
Fettzellen sind keine passiven Speicher; sie balancieren fortlaufend Speicherung und Freisetzung von Energie als Reaktion auf Hormone und Nährstoffe. Insulin signalisiert diesen Zellen, Zucker aus dem Blut aufzunehmen und den Abbau gespeicherter Fette zu drosseln. Dazu müssen viele Proteine zwischen verschiedenen zellulären Kompartimenten wandern, etwa der Zelloberfläche, inneren Membranen und kleinen Transportvesikeln. Bisher konzentrierte sich die Forschung meist auf einige gut bekannte Proteine. In dieser Arbeit erstellten die Autorinnen und Autoren eine zellweite Karte, die zeigt, wo Tausende von Proteinen in Adipozyten vor und nach einem Insulinschub liegen und wie sich ihre Standorte innerhalb weniger Minuten verändern.
Wie die Proteinlandschaft kartiert wurde
Das Team nutzte einen Ansatz namens subzelluläre Proteomik, der Zellfraktionierung und Massenspektrometrie kombiniert, um Proteine in verschiedenen Zellbereichen gleichzeitig zu messen. Sie arbeiteten mit 3T3-L1-Zellen, einem etablierten Mausmodell für Fettzellen, und trennten jede Probe in mehrere Fraktionen, die für Strukturen wie Zelloberfläche, Energiefabriken, Recycling-Kompartimente und Fetttropfen angereichert waren. Ein statistisches Framework verglich dann die Verteilung jedes Proteins in ruhenden Zellen mit der in insulinstimulierenden Zellen. Parallel dazu verwendeten die Forschenden eine separate Methode, die selektiv Proteine markiert, die an der äußeren Zelloberfläche exponiert sind, sodass sie quantifizieren konnten, wie viel von jedem Oberflächenprotein nach Insulinbehandlung zu- oder abnahm.
Insulin löst weitreichende Proteinumverteilung aus
Die kombinierten Datensätze zeigten, dass Insulin eine auffällige Neuordnung auslöst: Mehr als 500 Proteine wiesen hochsignifikante Positionsverschiebungen auf. Viele gehörten zu bekannten Signalwegen, darunter Komponenten, die Nährstoffe wahrnehmen und Wachstum steuern, sowie Proteinkinasen, die andere Proteine an- oder abschalten. Andere waren am Verkehr von vesikulärem Frachttransport beteiligt, der Moleküle zwischen inneren Kompartimenten und der Zelloberfläche shuttlelt. Einige Transportkomplexe verschoben sich deutlich als Reaktion auf Insulin, andere blieben stationär, was darauf hindeutet, dass das Hormon spezifische Zweige des zellulären Transportnetzwerks anvisiert. Die oberflächenfokussierten Experimente zeigten, dass über 300 Proteine in ihrer Häufigkeit an der äußeren Membran variierten, was bestätigt, dass die „Schnittstelle“ der Zelle zur Umgebung während einer Insulinantwort umgestaltet wird.
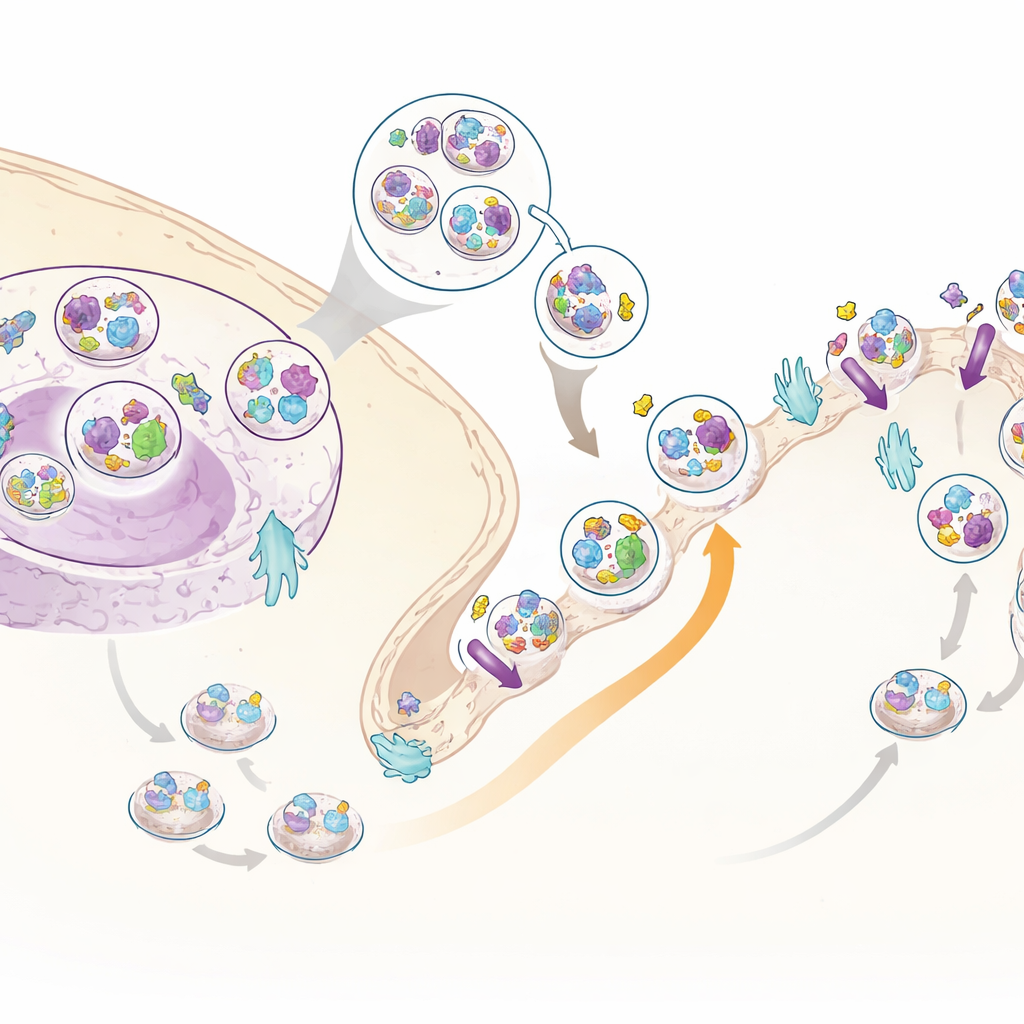
Ein neuer Insulinhelfer: C3ORF18
Unter den vielen wandernden Proteinen stach eines hervor: ein wenig untersuchtes Protein namens C3ORF18. Es wurde in beiden Datensätzen — dem Ganzzell- und dem Oberflächenspezifischen — stark in Richtung Zelloberfläche verschoben. Mikroskopie zeigte, dass C3ORF18 nahe dem Zellzentrum und in kleinen Vesikeln sitzt, von denen viele mit solchen überlappen, die den Transferrinrezeptor, ein bekanntes Recyclingprotein, und GLUT4, einen wichtigen Zuckertransporter, tragen. Nach Zugabe von Insulin oder Wachstumsfaktoren wanderte C3ORF18 rasch zur Zelloberfläche, und zwar auf eine Weise, die vom gleichen Signalzweig abhängt wie GLUT4. Dieses Verhalten legt nahe, dass C3ORF18 in einer insulin-sensitiven Recyclingroute mitreist, die hilft, wichtige Transporter zur Membran zu bringen.
Was passiert, wenn der neue Akteur fehlt
Um zu prüfen, ob C3ORF18 mehr als nur ein Mitläufer ist, reduzierten die Forschenden selektiv dessen Gehalt in ausgereiften Maus- und menschlichen Fettzellen. Innerhalb weniger Tage wurden Zellen ohne C3ORF18 weniger insulinempfindlich: Die Zuckeraufnahme sank, und sowohl GLUT4 als auch ein weiterer Zuckertransporter, GLUT1, waren weniger abundant. Die insulingetriebene Bewegung von GLUT4 und des Transferrinrezeptors zur Oberfläche war ebenfalls abgeschwächt, und zentrale Signalereignisse stromabwärts des Insulinrezeptors waren geschwächt. Kurz nach C3ORF18-Reduktion traten zunächst Störungen im Recycling des Transferrinrezeptors auf, was darauf hindeutet, dass Fehlfunktionen im endosomalen Recycling der Ausgangspunkt sein könnten, der schließlich die breiteren Effekte von Insulin untergräbt. Daten aus menschlichem Fettgewebe stützten diese Sicht: Personen mit höheren Blutzuckerwerten und Langzeit-Glukosemarkern hatten tendenziell eine geringere C3ORF18-Expression, und deren Spiegel stiegen mit Gewichtsverlust an.
Wesentliche Erkenntnisse für das Verständnis der Insulinempfindlichkeit
Die Studie zeigt, dass eine erfolgreiche Insulinantwort in Fettzellen nicht nur davon abhängt, welche Proteine vorhanden sind, sondern auch davon, wo sie sich zu einem gegebenen Zeitpunkt in der Zelle befinden. Insulin verteilt hunderte Proteine schnell um, besonders an der Zelloberfläche und in Recyclingkompartimenten, und diese Ortsänderungen wirken zusammen mit chemischen Modifikationen wie Phosphorylierung. Durch das systematische Kartieren dieser Bewegungen entdeckten die Autoren C3ORF18 als zuvor unerkannte Hilfe, die die Recyclingwege unterstützt, die für effiziente Zuckeraufnahme und gesunde Insulinsignale nötig sind. Das Verständnis solcher räumlicher Dynamiken eröffnet neue Wege, Ursachen des Verlusts der Insulinempfindlichkeit bei Stoffwechselerkrankungen zu erforschen und kann langfristig auf Ziele hinweisen, um diese wichtige Hormonantwort zu erhalten oder wiederherzustellen.
Zitation: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
Schlüsselwörter: Insulinresistenz, Adipozyt, Proteintransport, räumliche Proteomik, Glukoseaufnahme