Clear Sky Science · fr
La protéomique subcellulaire dynamique identifie des régulateurs de l’action de l’insuline dans les adipocytes
Pourquoi c’est important pour la santé quotidienne
L’insuline est une hormone surtout connue pour maintenir la glycémie sous contrôle, et lorsque son action échoue, des affections comme le diabète de type 2 peuvent apparaître. Cette étude explore l’intérieur des cellules adipeuses pour montrer, avec un niveau de détail inédit, comment des milliers de protéines déplacent rapidement leur position à l’arrivée de l’insuline. En suivant ce remaniement moléculaire, les chercheurs révèlent de nouveaux acteurs qui aident les cellules graisseuses à répondre correctement à l’insuline, fournissant des pistes inédites pour comprendre pourquoi l’insuline cesse parfois d’agir comme elle devrait.
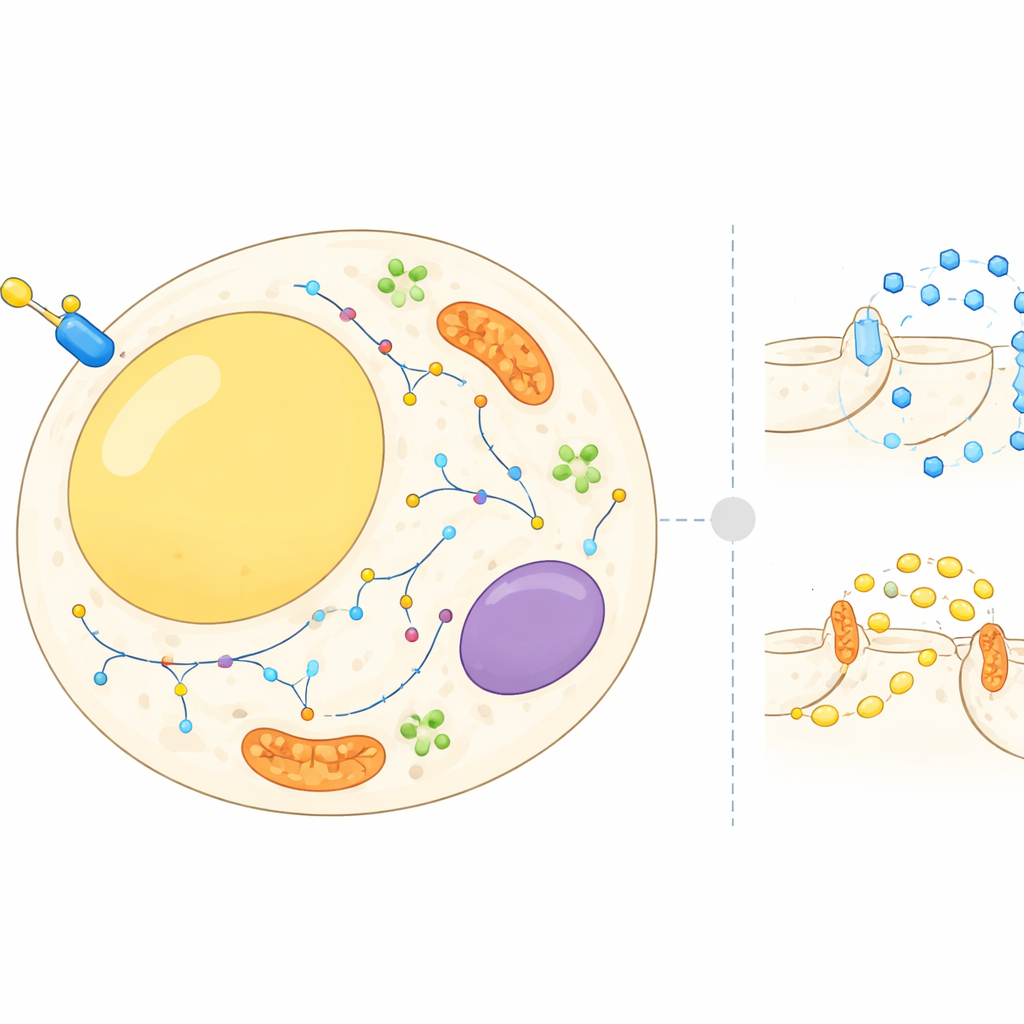
Une carte mobile à l’intérieur des cellules graisseuses
Les adipocytes ne sont pas de simples dépôts de stockage ; ils équilibrent en permanence le stockage et la libération d’énergie en réponse aux hormones et aux nutriments. L’insuline indique à ces cellules de capter le sucre présent dans le sang et de ralentir la dégradation des graisses stockées. Pour cela, de nombreuses protéines doivent se déplacer entre différents compartiments cellulaires, comme la surface cellulaire, les membranes internes et de petites vésicules de transport. Jusqu’à présent, la plupart des travaux se concentraient sur quelques protéines bien connues. Dans ce travail, les auteurs ont entrepris de construire une atlas cellulaire global indiquant où se trouvent des milliers de protéines dans les adipocytes avant et après une stimulation par l’insuline, et comment leurs localisations changent en quelques minutes.
Comment le paysage protéique a été cartographié
L’équipe a utilisé une approche appelée protéomique subcellulaire, qui combine fractionnement cellulaire et spectrométrie de masse pour mesurer simultanément les protéines présentes dans différentes parties de la cellule. Ils ont travaillé avec des cellules 3T3-L1, un modèle murin standard des adipocytes, et ont séparé chaque échantillon en plusieurs fractions enrichies pour des structures comme la surface cellulaire, les centrales énergétiques, les compartiments de recyclage et les gouttelettes lipidiques. Un cadre statistique a ensuite comparé la distribution de chaque protéine dans les cellules au repos versus les cellules stimulées par l’insuline. En parallèle, les chercheurs ont utilisé une méthode distincte qui marque sélectivement les protéines exposées à la surface externe de la cellule, leur permettant de quantifier l’augmentation ou la diminution de chaque protéine de surface après le traitement à l’insuline.
L’insuline déclenche un remaniement protéique généralisé
Les jeux de données combinés ont révélé que l’insuline provoque une réorganisation spectaculaire : plus de 500 protéines ont montré des déplacements de localisation avec un haut degré de confiance. Beaucoup appartenaient à des voies de signalisation connues, incluant des composants qui détectent les nutriments et régulent la croissance, ainsi que des kinases protéiques qui activent ou désactivent d’autres protéines. D’autres intervenaient dans le trafic de vésicules transportant des cargaisons entre les compartiments internes et la surface cellulaire. Certains complexes de transport se déplaçaient de façon marquée en réponse à l’insuline, tandis que d’autres restaient en place, ce qui suggère que l’hormone cible des branches spécifiques du réseau de transport cellulaire. Les expériences focalisées sur la surface ont montré que plus de 300 protéines changeaient en abondance à la membrane externe, confirmant que « l’interface » de la cellule avec son environnement est remodelée lors d’une réponse à l’insuline.
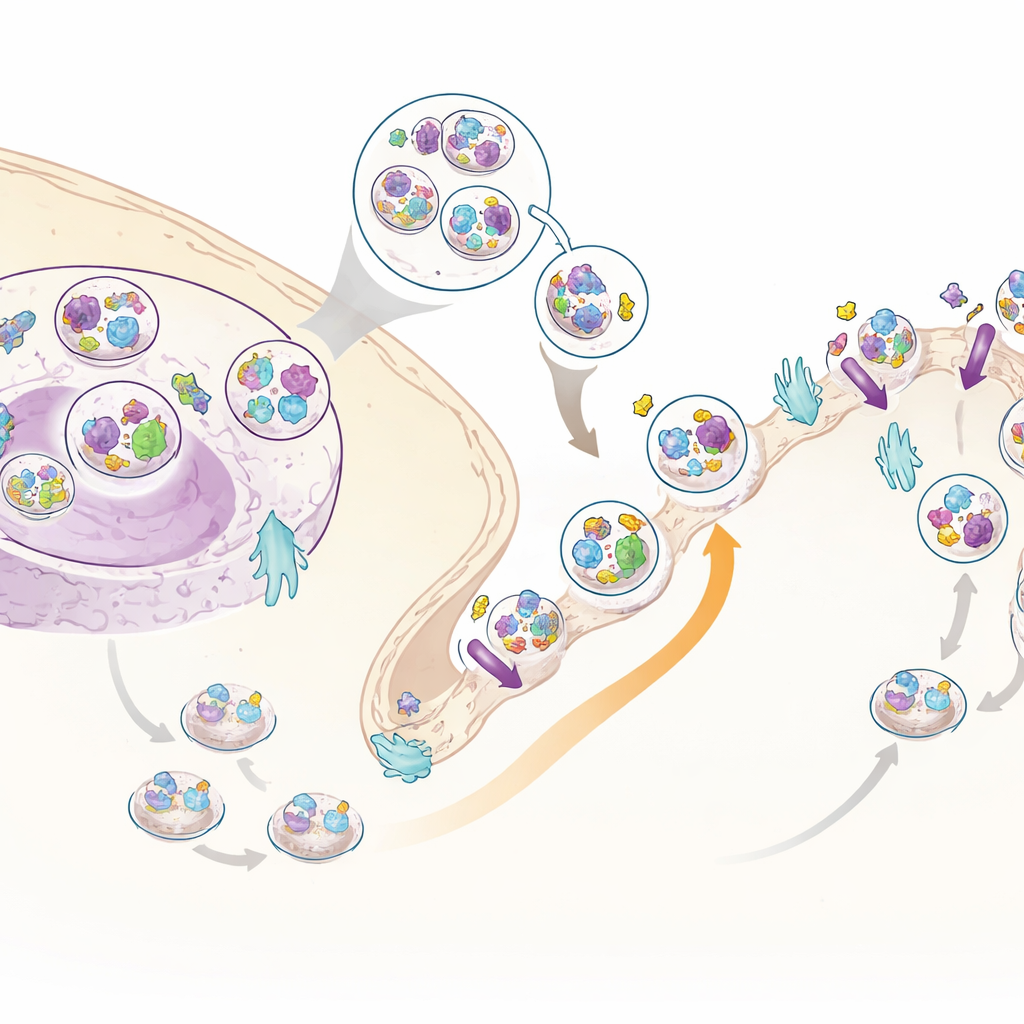
Un nouvel assistant de l’insuline : C3ORF18
Parmi les nombreuses protéines en mouvement, une a attiré l’attention : une protéine peu étudiée nommée C3ORF18. Elle a été fortement attirée vers la surface cellulaire par l’insuline dans les jeux de données global et ceux spécifiques à la surface. La microscopie a montré que C3ORF18 se situe près du centre de la cellule et dans de petites vésicules, dont beaucoup chevauchent celles transportant le récepteur de la transferrine, une protéine de recyclage bien connue, et le GLUT4, un transporteur de sucre clé. Lorsqu’on ajoute de l’insuline ou des facteurs de croissance, C3ORF18 se déplace rapidement vers la surface cellulaire d’une manière dépendante de la même branche de signalisation utilisée par GLUT4. Ce comportement suggère que C3ORF18 circule via une voie de recyclage sensible à l’insuline qui aide à amener des transporteurs importants à la membrane.
Que se passe-t-il lorsque le nouvel acteur manque
Pour tester si C3ORF18 fait plus que suivre le mouvement, les chercheurs ont réduit sélectivement son niveau dans des adipocytes murins et humains matures. Sur plusieurs jours, les cellules dépourvues de C3ORF18 sont devenues moins réactives à l’insuline : la captation du sucre a diminué, et GLUT4 ainsi qu’un autre transporteur de sucre, GLUT1, étaient moins abondants. Le déplacement induit par l’insuline de GLUT4 et du récepteur de la transferrine vers la surface était également atténué, et les étapes clés de la signalisation en aval du récepteur de l’insuline étaient affaiblies. Peu après l’épuisement de C3ORF18, des problèmes sont apparus d’abord dans le recyclage des récepteurs de la transferrine, ce qui laisse penser que des perturbations du recyclage endosomal pourraient être le point de départ qui finit par compromettre les effets plus larges de l’insuline. Des données provenant de tissus adipeux humains soutiennent en outre cette interprétation : les personnes ayant une glycémie plus élevée et des marqueurs glycémiques à long terme plus élevés avaient tendance à exprimer moins de C3ORF18, et ses niveaux augmentaient avec la perte de poids.
Conclusions générales pour comprendre la sensibilité à l’insuline
Cette étude montre qu’une réponse efficace à l’insuline dans les adipocytes dépend non seulement des protéines présentes, mais aussi de leur localisation au sein de la cellule à un instant donné. L’insuline redistribue rapidement des centaines de protéines, en particulier à la surface cellulaire et dans les compartiments de recyclage, et ces changements de localisation fonctionnent de concert avec des modifications chimiques comme la phosphorylation. En cartographiant systématiquement ces mouvements, les auteurs ont identifié C3ORF18 comme un auxiliaire jusque-là méconnu qui soutient les voies de recyclage nécessaires à une captation efficace du sucre et à une signalisation insulinique saine. Comprendre de telles dynamiques spatiales ouvre de nouvelles voies pour explorer pourquoi la sensibilité à l’insuline se dégrade dans les maladies métaboliques et pourrait éventuellement orienter vers des cibles visant à préserver ou restaurer cette réponse hormonale cruciale.
Citation: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
Mots-clés: résistance à l’insuline, adipocyte, trafic des protéines, protéomique spatiale, captation du glucose