Clear Sky Science · es
Proteómica subcelular dinámica identifica reguladores de la acción de la insulina en adipocitos
Por qué esto importa para la salud cotidiana
La insulina es una hormona conocida por mantener el azúcar en sangre bajo control, y cuando falla pueden desarrollarse enfermedades como la diabetes tipo 2. Este estudio examina el interior de las células grasas para ver, con un nivel de detalle sin precedentes, cómo miles de proteínas cambian rápidamente de posición cuando llega la insulina. Al rastrear este reordenamiento molecular, los autores descubren nuevos actores que ayudan a que las células adiposas respondan correctamente a la insulina, ofreciendo pistas frescas sobre por qué la insulina a veces deja de funcionar como debería.
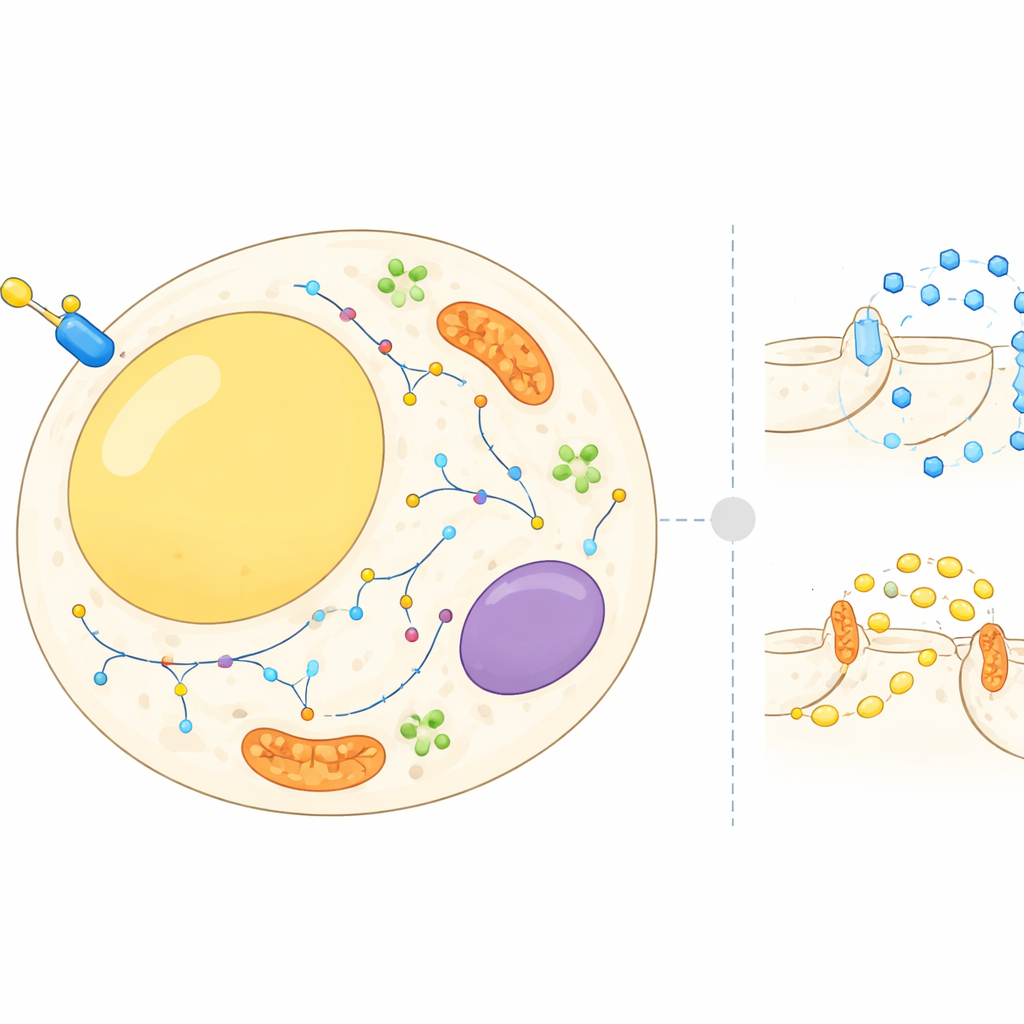
Un mapa en movimiento dentro de las células grasas
Las células grasas no son meros depósitos pasivos; equilibran constantemente el almacenamiento y la liberación de energía en respuesta a hormonas y nutrientes. La insulina indica a estas células que retiren glucosa del torrente sanguíneo y que ralenticen la descomposición de la grasa almacenada. Para ello, muchas proteínas deben moverse entre distintos compartimentos celulares, como la superficie celular, membranas internas y pequeñas vesículas de transporte. Hasta ahora, la mayoría de las investigaciones se centraban en unas pocas proteínas bien conocidas. En este trabajo, los autores se propusieron construir un atlas a escala celular de dónde se localizan miles de proteínas en las células adiposas antes y después de un pulso de insulina, y cómo cambian sus ubicaciones en cuestión de minutos.
Cómo se cartografió el paisaje proteico
El equipo utilizó un enfoque llamado proteómica subcelular, que combina fraccionamiento celular y espectrometría de masas para medir proteínas en distintas partes de la célula a la vez. Trabajaron con células 3T3-L1, un modelo murino estándar de adipocitos, y separaron cada muestra en múltiples fracciones enriquecidas en estructuras como la superficie celular, las fábricas de energía, compartimentos de reciclaje y gotas lipídicas. Un marco estadístico comparó entonces la distribución de cada proteína en células en reposo frente a células estimuladas con insulina. En paralelo, los investigadores usaron un método separado que marcaba selectivamente las proteínas expuestas en la superficie externa de la célula, permitiéndoles cuantificar cuánto aumentó o disminuyó cada proteína superficial tras el tratamiento con insulina.
La insulina provoca un amplio reordenamiento de proteínas
Los conjuntos de datos combinados revelaron que la insulina desencadena una reorganización llamativa: más de 500 proteínas mostraron desplazamientos con alta confianza en su localización. Muchas pertenecían a vías de señalización conocidas, incluidos componentes que detectan nutrientes y regulan el crecimiento, así como quinasas que activan o desactivan otras proteínas. Otras estaban implicadas en el tráfico de vesículas que transportan carga entre compartimentos internos y la superficie celular. Algunos complejos de transporte se movieron de forma notable en respuesta a la insulina, mientras que otros permanecieron fijos, lo que sugiere que la hormona apunta a ramas específicas de la red de transporte celular. Los experimentos centrados en la superficie mostraron que más de 300 proteínas cambiaron en abundancia en la membrana externa, confirmando que la "interfaz" de la célula con su entorno se remodela durante la respuesta a la insulina.
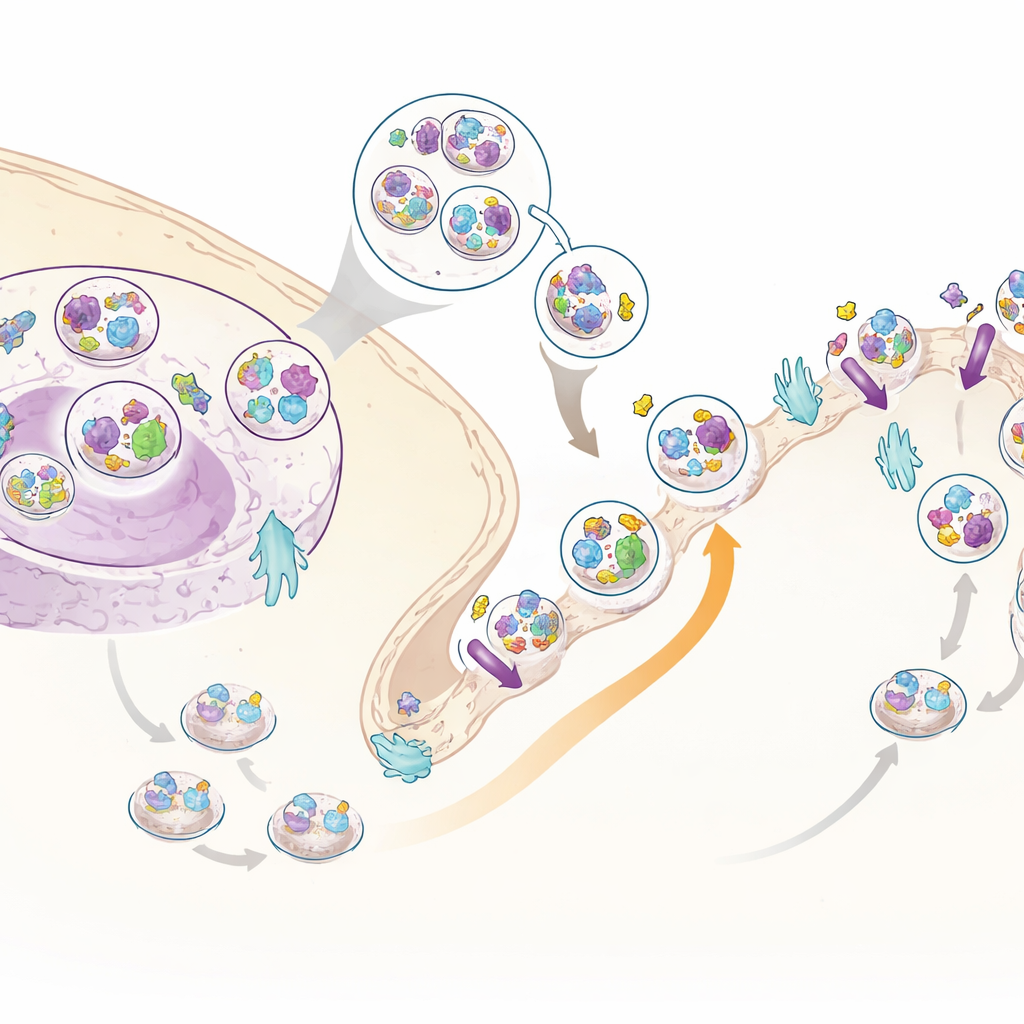
Un nuevo colaborador de la insulina: C3ORF18
Entre las muchas proteínas en movimiento, destacó una: una proteína poco estudiada llamada C3ORF18. La insulina la desplazó con fuerza hacia la superficie celular tanto en los conjuntos de datos globales como en los específicos de la superficie. Microscopía mostró que C3ORF18 se sitúa cerca del centro celular y en pequeñas vesículas, muchas de las cuales se solapan con las que llevan el receptor de transferrina, una proteína de reciclaje bien conocida, y con GLUT4, un transportador clave de glucosa. Cuando se añadió insulina o factores de crecimiento, C3ORF18 se dirigió rápidamente a la superficie celular de una manera dependiente de la misma rama de señalización utilizada por GLUT4. Este comportamiento sugiere que C3ORF18 viaja en una ruta de reciclaje sensible a la insulina que ayuda a llevar transportadores importantes a la membrana.
Qué ocurre cuando falta este nuevo actor
Para comprobar si C3ORF18 hace algo más que acompañar, los investigadores redujeron selectivamente sus niveles en adipocitos maduros de ratón y humanos. A lo largo de varios días, las células sin C3ORF18 se volvieron menos sensibles a la insulina: la captación de glucosa disminuyó y tanto GLUT4 como otro transportador de glucosa, GLUT1, se mostraron menos abundantes. El movimiento impulsado por insulina de GLUT4 y del receptor de transferrina hacia la superficie también se vio atenuado, y los pasos centrales de la señalización aguas abajo del receptor de insulina se debilitaron. Temprano tras la depleción de C3ORF18, los problemas aparecieron primero en el reciclaje del receptor de transferrina, lo que sugiere que las alteraciones en el reciclaje endosomal pueden ser el punto de partida que finalmente socava los efectos más amplios de la insulina. Datos de tejido adiposo humano apoyaron esta idea: personas con niveles más altos de glucosa en sangre y marcadores de glucosa a largo plazo tendían a tener menor expresión de C3ORF18, y sus niveles aumentaron con la pérdida de peso.
Conclusiones generales para entender la sensibilidad a la insulina
Este estudio muestra que una respuesta exitosa a la insulina en las células grasas depende no solo de qué proteínas están presentes, sino también de dónde se encuentran en la célula en cada momento. La insulina redistribuye rápidamente cientos de proteínas, especialmente en la superficie celular y dentro de los compartimentos de reciclaje, y estos cambios de localización actúan junto con modificaciones químicas como la fosforilación. Al mapear sistemáticamente este movimiento, los autores descubrieron a C3ORF18 como un colaborador hasta ahora no reconocido que sostiene las rutas de reciclaje necesarias para una captación eficiente de glucosa y una señalización insulínica sana. Entender estas dinámicas espaciales abre nuevas vías para explorar por qué la sensibilidad a la insulina se erosiona en la enfermedad metabólica y puede eventualmente señalar objetivos para preservar o restaurar esta respuesta hormonal crucial.
Cita: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
Palabras clave: resistencia a la insulina, adipocito, transporte de proteínas, proteómica espacial, captación de glucosa