Clear Sky Science · sv
Dynamic subcellular proteomics identifies regulators of adipocyte insulin action
Varför detta spelar roll för vardagshälsan
Insulin är ett hormon mest känt för att hålla blodsockret under kontroll, och när det sviktar kan tillstånd som typ 2-diabetes utvecklas. Denna studie granskar fettceller på molekylär nivå för att, i en aldrig tidigare skådad detalj, se hur tusentals proteiner snabbt ändrar sina positioner när insulin kommer. Genom att följa denna molekylära omfördelning hittar forskarna nya aktörer som hjälper fettceller att reagera korrekt på insulin, vilket ger nya ledtrådar till varför insulin ibland slutar fungera som det ska.
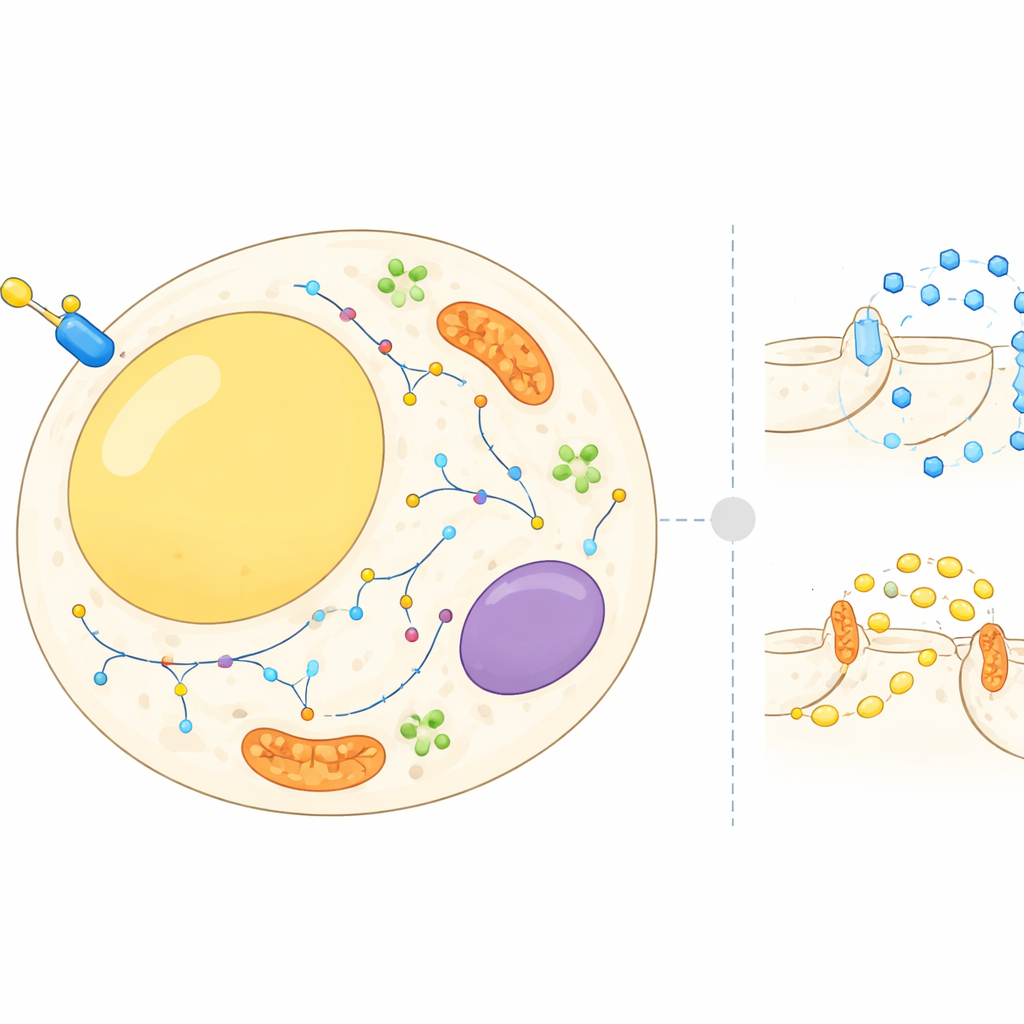
En rörlig karta inne i fettceller
Fettceller är inte bara passiva förråd; de balanserar ständigt lagring och frisättning av energi i respons till hormoner och näringsämnen. Insulin signalerar åt dessa celler att ta upp socker från blodet och att bromsa nedbrytningen av lagrat fett. För att göra detta måste många proteiner flytta sig mellan olika cellulära fack, såsom cellytan, interna membran och små transportblåsor. Fram tills nu har de flesta studier fokuserat på ett fåtal välkända proteiner. I detta arbete byggde författarna en cellomfattande atlas över var tusentals proteiner finns i fettceller före och efter en insulinpuls, och hur deras lägen förändras inom minuter.
Hur proteinlandskapet kartlades
Teamet använde en metod som kallas subcellulär proteomik, som kombinerar cellfraktionering och masspektrometri för att mäta proteiner i olika delar av cellen samtidigt. De arbetade med 3T3-L1-celler, en standard modell för musfettceller, och separerade varje prov i flera fraktioner som är berikade för strukturer som cellytan, energifabriker, återvinningskompartiment och fettkroppar. Ett statistiskt ramverk jämförde sedan fördelningen av varje protein i vilande celler mot insulinstimulerade celler. Parallellt använde forskarna en separat metod som selektivt märkte proteiner exponerade på cellens yttre yta, vilket gjorde det möjligt att kvantifiera hur mycket av varje ytprotein som ökade eller minskade efter insulinbehandling.
Insulin utlöser omfattande proteinomfördelning
De sammanslagna datasetten visade att insulin triggar en slående omorganisation: mer än 500 proteiner uppvisade högt förtroende för skift i sin lokalisering. Många tillhörde kända signalvägar, inklusive komponenter som känner av näringsämnen och reglerar tillväxt, samt proteinkinaser som slår andra proteiner på eller av. Andra var involverade i trafiken hos vesiklar som transporterar last mellan interna kompartiment och cellytan. Vissa transportkomplex flyttade märkbart som svar på insulin, medan andra stannade kvar, vilket tyder på att hormonet riktar sig mot specifika grenar av cellens transportsystem. De yt-fokuserade experimenten visade att över 300 proteiner förändrade sin förekomst vid det yttre membranet, vilket bekräftar att cellens "gränssnitt" med omgivningen omformas under en insulinrespons.
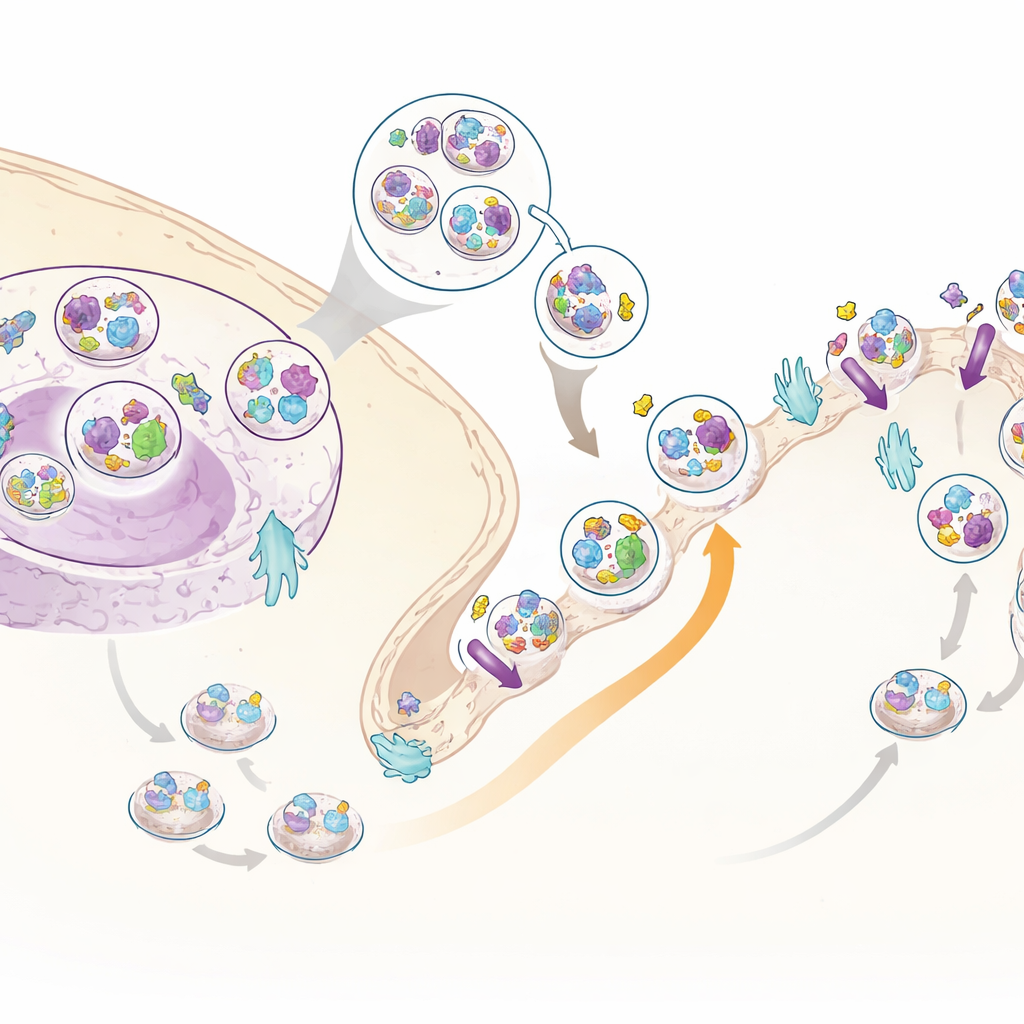
En ny insulinhjälpare: C3ORF18
Bland de många rörliga proteinerna stack ett ut: ett lite studerat protein kallat C3ORF18. Det drogs kraftigt mot cellytan av insulin i både helcells- och ytspecifika dataset. Mikroskopi visade att C3ORF18 sitter nära cellens centrum och i små vesiklar, många av dem överlappande med dem som bär transferrinreceptorn, ett välkänt återvinningsprotein, och med GLUT4, en nyckeltransportör för socker. När insulin eller tillväxtfaktorer tillsattes, rörde sig C3ORF18 snabbt till cellytan på ett sätt som var beroende av samma signalgren som används av GLUT4. Detta beteende tyder på att C3ORF18 färdas i en insulin-känslig återvinningsväg som hjälper till att leverera viktiga transportörer till membranet.
Vad händer när den nya aktören saknas
För att testa om C3ORF18 gör mer än att bara följa med, minskade forskarna selektivt dess nivåer i mogna mus- och människofettceller. Efter några dagar blev celler utan C3ORF18 mindre responsiva mot insulin: glukosupptaget sjönk, och både GLUT4 och en annan glukostransportör, GLUT1, var mindre talrika. Insulin-drivna förflyttningar av GLUT4 och transferrinreceptorn till ytan dämpades också, och centrala signaleringssteg nedströms om insulinreceptorn försvagades. Tidigt efter C3ORF18-nedreglering uppstod problem först i återvinningen av transferrinreceptorer, vilket antyder att störningar i endosomal återvinning kan vara startpunkten som så småningom undergräver insulins bredare effekter. Data från mänsklig fettvävnad stödde denna bild: personer med högre blodsocker och långsiktiga glukosmarkörer tenderade att ha lägre uttryck av C3ORF18, och nivåerna ökade vid viktnedgång.
Stora slutsatser för förståelsen av insulinkänslighet
Denna studie visar att en framgångsrik insulinrespons i fettceller beror inte bara på vilka proteiner som finns, utan också på var de befinner sig i cellen vid varje givet ögonblick. Insulin omfördelar snabbt hundratals proteiner, särskilt vid cellytan och inom återvinningskompartiment, och dessa lägesförändringar verkar tillsammans med kemiska modifieringar som fosforylering. Genom att systematiskt kartlägga denna rörelse upptäckte författarna C3ORF18 som en tidigare oupptäckt hjälpare som stöder de återvinningsvägar som behövs för effektiv glukosupptagning och sund insulins signalering. Att förstå sådana rumsliga dynamiker öppnar nya vägar för att utforska varför insulinkänsligheten minskar vid metabola sjukdomar och kan så småningom peka på mål för att bevara eller återställa denna avgörande hormonrespons.
Citering: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
Nyckelord: insulinresistens, adipocyt, proteintrafik, rumslig proteomik, glukosupptag