Clear Sky Science · ja
動的な細胞内プロテオミクスが脂肪細胞のインスリン作用の調節因子を同定する
日常の健康にとってなぜ重要か
インスリンは血糖を調整することでよく知られるホルモンで、その働きが損なわれると2型糖尿病のような状態が生じます。本研究は脂肪細胞の内部を詳しく調べ、インスリンが到来したときに数千のタンパク質がどのように素早く位置を変えるかを前例のない解像度で明らかにします。この分子レベルの再配列を追跡することで、脂肪細胞がインスリンに適切に応答するのを助ける新たな因子が発見され、インスリンの作用が不十分になる理由に新しい手がかりを与えます。
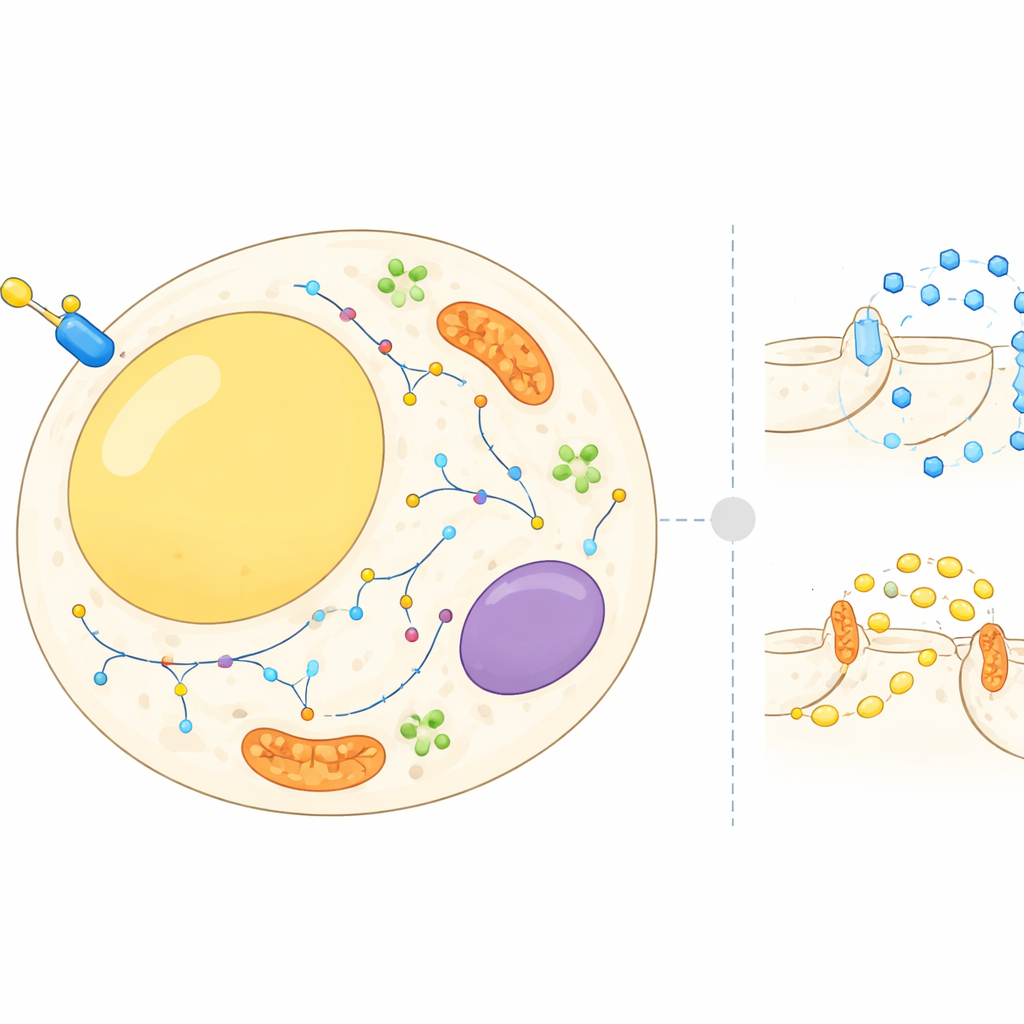
脂肪細胞内の動く地図
脂肪細胞は単なるエネルギーの貯蔵庫ではなく、ホルモンや栄養状態に応じて貯蔵と放出を絶えず調整しています。インスリンはこれらの細胞に血流から糖を取り込ませ、貯蔵脂肪の分解を抑えるよう指示します。そのために、多くのタンパク質が細胞表面、内部膜、小さな輸送小胞など、さまざまな細胞コンパートメント間を移動する必要があります。これまでの研究は少数のよく知られたタンパク質に焦点を当てることが多かったのに対し、本研究ではインスリン刺激の前後で数千のタンパク質が脂肪細胞内のどこに存在し、数分のうちにその位置がどのように変化するかを細胞全体のアトラスとして構築しようとしました。
タンパク質の分布はどのように描かれたか
研究チームはサブセルラー・プロテオミクスと呼ばれる手法を用い、細胞分画と質量分析を組み合わせて同時に異なる細胞部位のタンパク質を計測しました。対象は脂肪細胞の標準モデルである3T3-L1細胞で、各サンプルを細胞表面、エネルギー産生の場、リサイクリング区画、脂肪滴などの構造に富んだ複数の分画に分けました。統計的枠組みで安静時の細胞とインスリン刺激細胞における各タンパク質の分布を比較しました。並行して、細胞外表面に露出するタンパク質を選択的に標識する別法を用い、インスリン処理後に各表面タンパク質がどれだけ増減したかを定量しました。
インスリンは広範なタンパク質の再編を引き起こす
これらのデータを統合すると、インスリンは顕著な再編成を誘発することが明らかになりました:500以上のタンパク質が高信頼度で位置を変えました。多くは栄養を感知し成長を制御する既知のシグナル経路に属し、他のタンパク質のオン・オフを切り替えるプロテインキナーゼも含まれていました。さらに、内在区画と細胞表面の間で分子を輸送する小胞の輸送に関わるタンパク質も多く見られました。いくつかの輸送複合体はインスリンに応じて明確に移動し、他は動かなかったことから、ホルモンが細胞の輸送ネットワークの特定の枝を標的にしていることが示唆されます。表面に焦点を当てた実験では、300以上のタンパク質が外膜での存在量を変え、インスリン応答時に細胞の「界面」が形を変えることが裏付けられました。
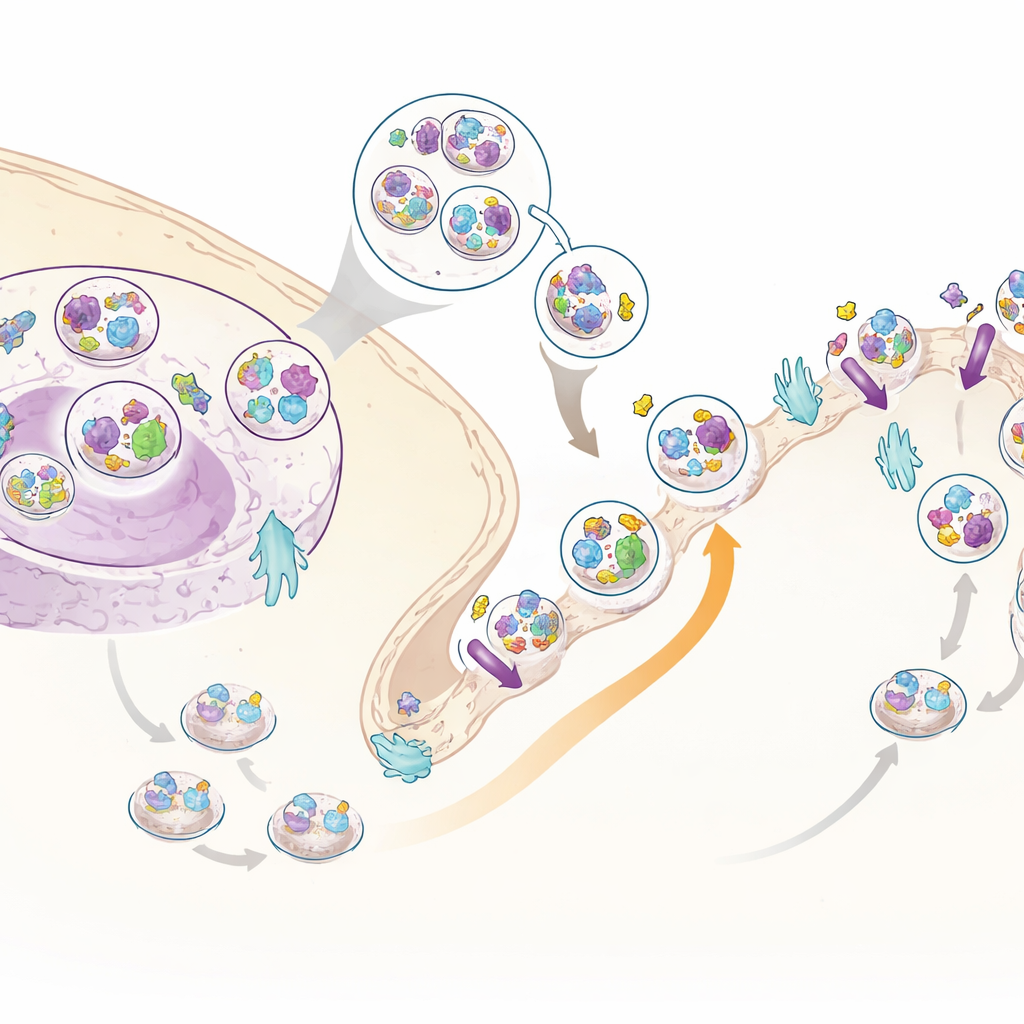
新たなインスリンの助っ人:C3ORF18
多くの移動するタンパク質の中で際立っていたのが、ほとんど研究されていないC3ORF18というタンパク質でした。C3ORF18は全細胞データと表面特異的データのいずれでもインスリンにより強く細胞表面へ引き寄せられていました。顕微鏡観察では、C3ORF18は細胞中心付近や小さな小胞に局在し、それらの多くが既知のリサイクリングタンパク質であるトランスフェリン受容体や主要な糖輸送体GLUT4と重なることが示されました。インスリンや成長因子を加えると、C3ORF18はGLUT4と同じシグナル分岐に依存して迅速に細胞表面へ移動しました。これは、C3ORF18が重要な輸送体を膜へ届けるインスリン感受性のリサイクリング経路を共有していることを示唆します。
この新規因子が欠けると何が起きるか
C3ORF18が単に移動しているだけかどうかを調べるために、研究者は成熟したマウスおよびヒトの脂肪細胞でその量を選択的に減少させました。数日後、C3ORF18を欠く細胞はインスリンへの応答性が低下しました:糖の取り込みが減少し、GLUT4ともう一つの糖輸送体であるGLUT1の量が減りました。GLUT4やトランスフェリン受容体の表面へのインスリン誘導移動も鈍り、インスリン受容体下流の主要なシグナル伝達ステップも弱まりました。C3ORF18枯渇の早期にはまずトランスフェリン受容体のリサイクリングに問題が現れ、エンドソームリサイクリングの障害が最終的にインスリンの広範な作用を損なう出発点であることを示唆しました。ヒト脂肪組織のデータもこの見解を支持しており、高血糖や長期的な血糖指標が高い人ではC3ORF18の発現が低く、体重減少に伴ってそのレベルが上昇する傾向がありました。
インスリン感受性理解への大局的な示唆
本研究は、脂肪細胞における成功するインスリン応答は、どのタンパク質が存在するかだけでなく、それらがその時点で細胞内のどこにいるかにも依存することを示しています。インスリンは数百のタンパク質を特に細胞表面やリサイクリング区画内で急速に再配置し、これらの位置変化はリン酸化のような化学的修飾と協調して働きます。この移動を系統的にマッピングすることで、著者らは効率的な糖取り込みと健全なインスリンシグナルを支えるリサイクリング経路を助ける未認識の因子C3ORF18を発見しました。こうした空間的ダイナミクスを理解することは、代謝疾患でインスリン感受性が低下する理由を探る新たな道を開き、最終的にはこの重要なホルモン応答を維持または回復するための標的を示す可能性があります。
引用: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
キーワード: インスリン抵抗性, 脂肪細胞, タンパク質輸送, 空間プロテオミクス, グルコース取り込み