Clear Sky Science · ru
Динамическая субклеточная протеомика выявляет регуляторы инсулинового действия адипоцитов
Почему это важно для повседневного здоровья
Инсулин — гормон, наиболее известный своей ролью в поддержании уровня сахара в крови; при нарушении его действия могут развиться такие состояния, как сахарный диабет 2 типа. В этом исследовании изучают внутреннее устройство жировых клеток, чтобы с беспрецедентной детализацией проследить, как тысячи белков быстро меняют свои локализации при поступлении инсулина. Отслеживая это молекулярное перемещение, авторы обнаруживают новые участники, которые помогают адипоцитам правильно отвечать на инсулин, что дает свежие подсказки о причинах нарушения его действия.
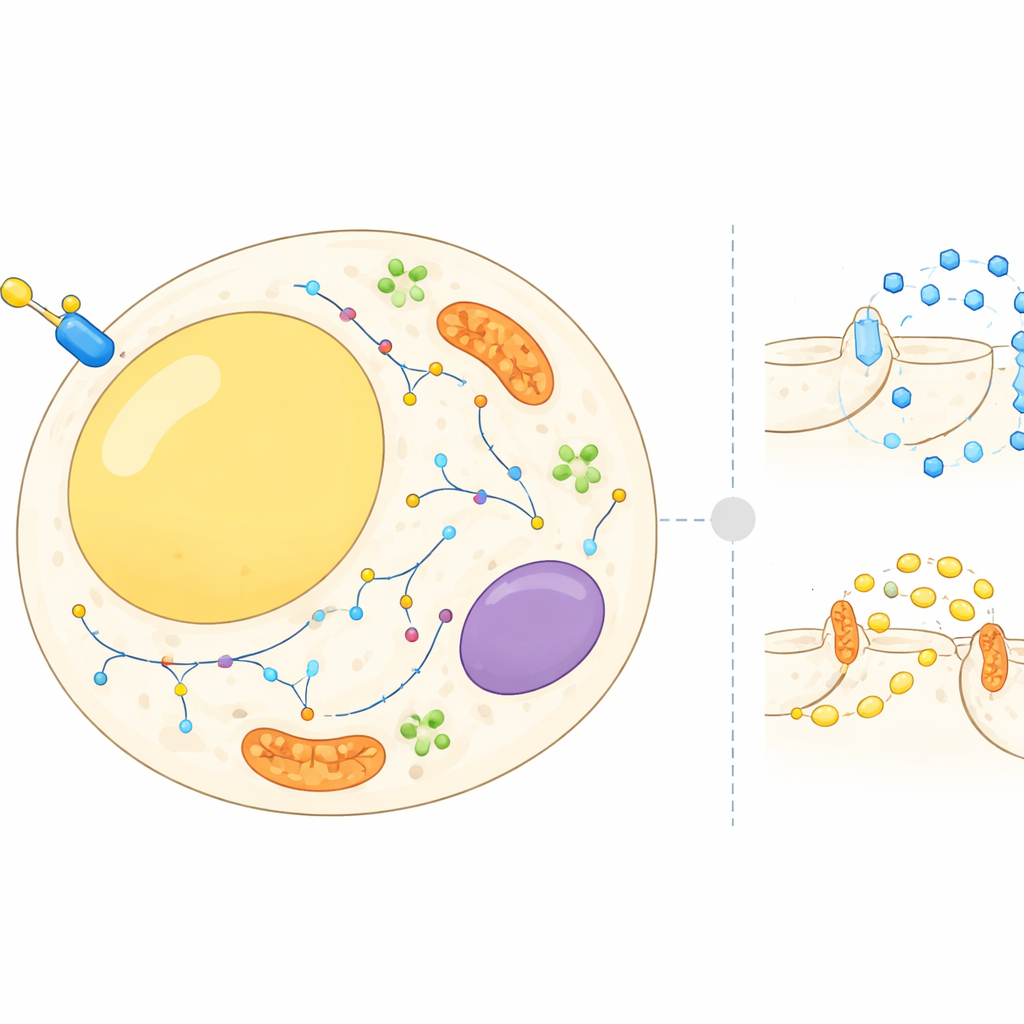
Динамическая карта внутри жировых клеток
Жировые клетки — не просто пассивные депо для хранения; они постоянно балансируют между накоплением и отдачей энергии в ответ на гормоны и питательные вещества. Инсулин дает сигнал этим клеткам забирать сахар из крови и замедлять распад запасенного жира. Для этого множество белков должны перемещаться между разными субклеточными компартментами — например, между поверхностью клетки, внутренними мембранами и малыми транспортными пузырьками. До сих пор большинство работ сосредоточивалось на нескольких хорошо изученных белках. В этой работе авторы поставили цель создать клеточный атлас, показывающий, где находятся тысячи белков в адипоците до и после вспышки инсулина и как их локализации меняются в течение нескольких минут.
Как картировался ландшафт белков
Команда использовала подход, называемый субклеточной протеомикой, который сочетает фракционирование клеток и масс-спектрометрию для измерения белков в разных частях клетки одновременно. Они работали с клетками 3T3-L1, стандартной мышиной моделью жировых клеток, и разделяли каждый образец на несколько фракций, обогащённых структурами вроде клеточной поверхности, энергетических фабрик, рециклирующих компартментов и жировых капель. Статистическая методика затем сравнивала распределение каждого белка в покоящихся клетках и в клетках, стимулированных инсулином. Параллельно исследователи применили отдельный метод, который селективно маркирует белки на наружной поверхности клетки, что позволило им количественно оценить, насколько увеличивалось или уменьшалось присутствие каждого поверхностного белка после обработки инсулином.
Инсулин вызывает широкомасштабное перераспределение белков
Комбинация наборов данных показала, что инсулин запускает впечатляющую реорганизацию: более 500 белков продемонстрировали с высокой уверенностью смещение своих локализаций. Многие из них принадлежали известным сигнальным путям, включая компоненты, чувствительные к питательным веществам и регулирующие рост, а также протеинкиназы, которые включают или выключают другие белки. Другие участвовали в транспортировке грузов в пузырьках, которые перемещают молекулы между внутренними компартментами и поверхностью клетки. Некоторые транспортные комплексы заметно перемещались в ответ на инсулин, в то время как другие оставались на месте, что указывает на то, что гормон затрагивает отдельные ветви транспортной сети клетки. Эксперименты, сфокусированные на поверхности, показали, что более 300 белков изменяли свою концентрацию в наружной мембране, подтверждая, что «интерфейс» клетки с окружением перестраивается во время инсулинового ответа.
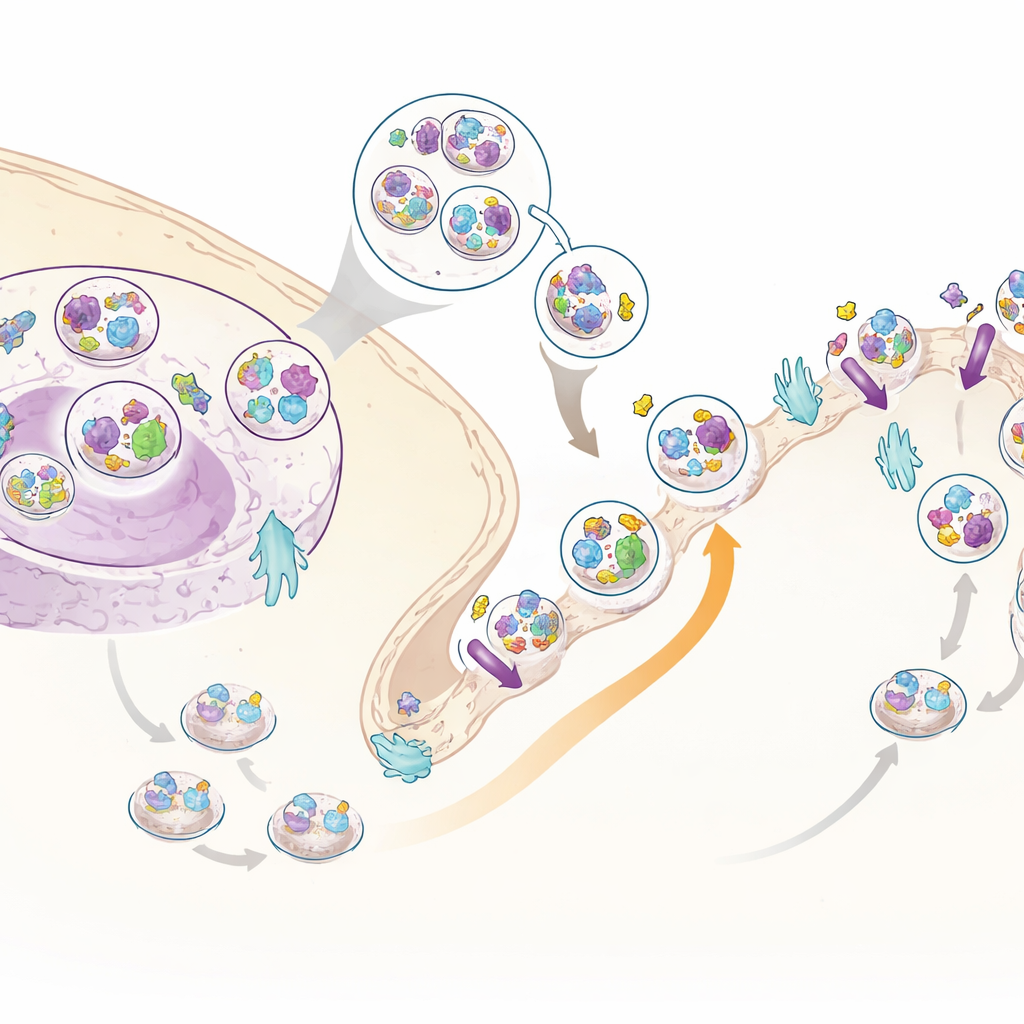
Новый помощник инсулина: C3ORF18
Среди множества перемещающихся белков один выделялся: малоизученный белок C3ORF18. Он значительно перемещался к поверхности клетки под действием инсулина как в результате анализа всего клетки, так и в данных, специфичных для поверхности. Микроскопия показала, что C3ORF18 локализуется рядом с центром клетки и в мелких везикулах, многие из которых перекрываются с везикулами, несущими трансферриновый рецептор, известный белок рециклинга, и с GLUT4 — ключевым транспортёром глюкозы. При добавлении инсулина или факторов роста C3ORF18 быстро перемещался к поверхности клетки способами, зависящими от той же сигнальной ветви, что и GLUT4. Такое поведение указывает на то, что C3ORF18 движется по инсулинчувствительному рециклирующему маршруту, который помогает доставлять важные транспортеры к мембране.
Что происходит, когда новый участник отсутствует
Чтобы проверить, делает ли C3ORF18 нечто большее, чем просто сопутствует, исследователи селективно снизили его уровни в зрелых мышиных и человеческих жировых клетках. В течение нескольких дней клетки с дефицитом C3ORF18 становились менее чувствительными к инсулину: поглощение сахара падало, а уровни как GLUT4, так и другого транспортерa глюкозы, GLUT1, снижались. Инсулин-индуцируемое перемещение GLUT4 и трансферринового рецептора к поверхности также было ослаблено, а ключевые сигнальные этапы ниже по цепочке от инсулинового рецептора оказались подорванными. Ранние нарушения после истощения C3ORF18 появились прежде всего в рециклинге трансферриновых рецепторов, что намекает на то, что сбои в эндосомальном рециклинге могут быть начальной точкой, которая со временем подрывает более широкие эффекты инсулина. Данные из образцов жировой ткани человека дополнительно поддерживают эту картину: у людей с более высоким уровнем сахара в крови и повышенными долгосрочными маркерами гликемии, как правило, регистрировалось более низкое экспрессивное значение C3ORF18, а его уровни повышались при снижении веса.
Основные выводы для понимания инсулиновой чувствительности
Это исследование демонстрирует, что успешный инсулиновый ответ в жировых клетках зависит не только от того, какие белки присутствуют, но и от того, где они находятся в клетке в каждый данный момент. Инсулин быстро перераспределяет сотни белков, особенно на поверхности клетки и в рециклирующих компартментах, и эти изменения локализации работают наряду с химическими модификациями, такими как фосфорилирование. Систематически картируя это движение, авторы выявили C3ORF18 как ранее не признанного помощника, который поддерживает маршруты рециклинга, необходимые для эффективного поглощения сахара и здоровой инсулиновой сигнализации. Понимание таких пространственных динамик открывает новые пути для изучения причин утраты инсулиновой чувствительности при метаболических заболеваниях и может в конечном итоге указать на мишени для сохранения или восстановления этого важного гормонального ответа.
Цитирование: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
Ключевые слова: инсулинорезистентность, адипоцит, транспорт белков, пространственная протеомика, поглощение глюкозы