Clear Sky Science · ar
علم البروتيوميات تحت الخلوية الديناميكي يحدد منظمات استجابة الخلايا الدهنية للإنسولين
لماذا يهم هذا للصحة اليومية
الإنسولين هرمون معروف بأنه يحافظ على مستوى السكر في الدم، وعندما يفشل قد تتطور حالات مثل داء السكري من النوع 2. تنظر هذه الدراسة داخل الخلايا الدهنية لتظهر، بتفصيل غير مسبوق، كيف يتحرك آلاف البروتينات بسرعة إلى مواضع جديدة عند وصول الإنسولين. من خلال تتبع هذا إعادة التوزيع الجزيئي، يكشف الباحثون عن عوامل جديدة تساعد الخلايا الدهنية على الاستجابة للإنسولين بشكل صحيح، مما يقدم دلائل جديدة عن سبب تعطّل عمل الإنسولين في بعض الأحيان.
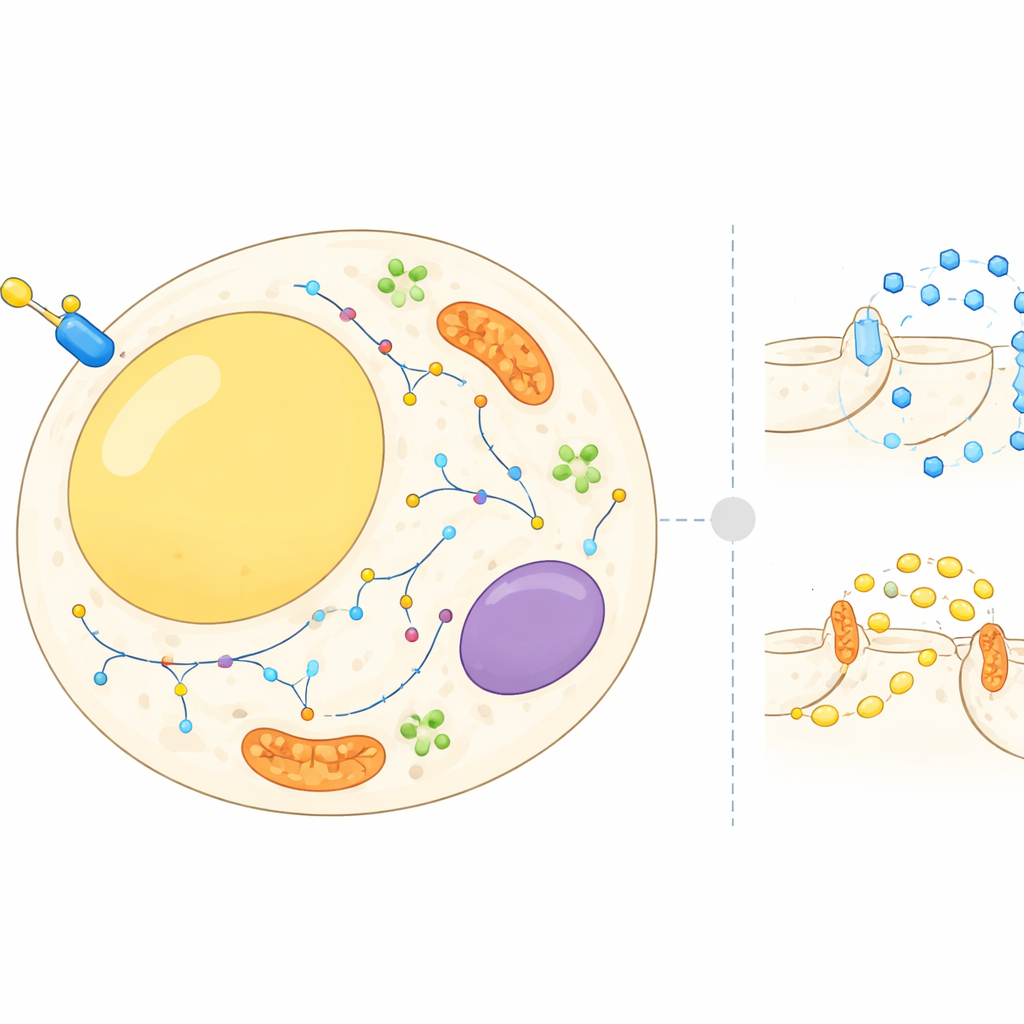
خريطة متحركة داخل الخلايا الدهنية
الخلايا الدهنية ليست مجرد مخازن خاملة؛ فهي توازن باستمرار بين تخزين وإطلاق الطاقة استجابةً للهرمونات والمغذيات. يوجّه الإنسولين هذه الخلايا لسحب السكر من مجرى الدم وإبطاء تكسير الدهون المخزنة. لتحقيق ذلك، يجب أن تنتقل العديد من البروتينات بين مقصورات خلوية مختلفة، مثل سطح الخلية والأغشية الداخلية والحويصلات الناقلة الصغيرة. حتى الآن ركّزت معظم الأبحاث على عدد محدود من البروتينات المعروفة. في هذا العمل، هدف المؤلفون إلى بناء أطلس على مستوى الخلية لمواضع آلاف البروتينات في الخلايا الدهنية قبل وبعد اندفاع الإنسولين، وكيف تتغير مواقعها خلال دقائق.
كيف تم رسم خريطة البروتينات
استخدم الفريق نهجًا يُدعى البروتيوميات تحت الخلوية، الذي يجمع بين تجزئة الخلايا والقياس الطيفي الكتلي لقياس البروتينات في أجزاء مختلفة من الخلية في آن واحد. عملوا مع خلايا 3T3-L1، وهو نموذج فأري معياري للخلايا الدهنية، وفَصّلوا كل عينة إلى كسور متعددة مُعزّزة لهياكل مثل سطح الخلية، مصانع الطاقة، مقصورات إعادة التدوير وقطيرات الدهون. بعد ذلك قارن إطار إحصائي توزيع كل بروتين في الخلايا الساكنة مقابل الخلايا المحفّزة بالإنسولين. بالتوازي، استخدم الباحثون طريقة منفصلة وسمت اختيارياً البروتينات المكشوفة على السطح الخارجي للخلية، مما أتاح لهم قياس مقدار ازدياد أو نقصان كل بروتين سطحي بعد معالجة الإنسولين.
الإنسولين يطلق إعادة توزيع واسعة للبروتينات
كشفت مجموعتا البيانات المجمعتان أن الإنسولين يحفز إعادة تنظيم لافتة للنظر: أكثر من 500 بروتين أظهر تغيّرات موضعية عالية الثقة. كان كثير منها ينتمي إلى مسارات إشارات معروفة، بما في ذلك مكونات تحسّس المغذيات وتنظيم النمو، وكذلك كينازات بروتينية تُشغّل أو تُطفئ بروتينات أخرى. والبعض الآخر شارك في نقل الحويصلات الحاملة للشحنات التي تنقل الجزيئات بين المقصورات الداخلية وسطح الخلية. تحرّكت بعض مجمعات النقل ملحوظًا استجابةً للإنسولين، بينما بقيت أخرى في مواضعها، ما يشير إلى أن الهرمون يستهدف فروعًا معينة من شبكة نقل الخلية. أظهرت التجارب المركزة على السطح أن أكثر من 300 بروتين تغيّرت كميتها على الغشاء الخارجي، مؤكدة أن «الواجهة» بين الخلية وبيئتها تُعاد تشكيلها خلال استجابة الإنسولين.
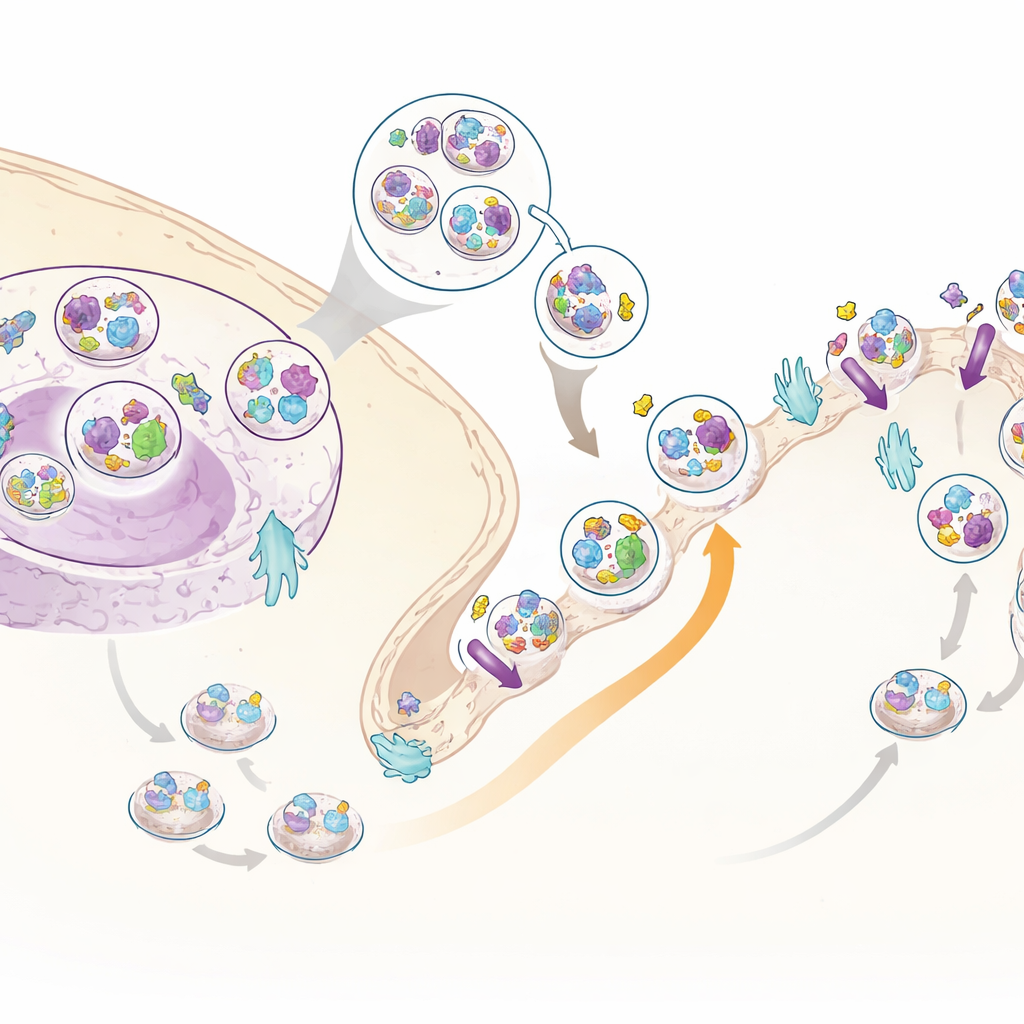
مساعد إنسولين جديد: C3ORF18
من بين البروتينات المتحركة، برز واحد قليل الدراسة اسمه C3ORF18. جذبه الإنسولين بقوة نحو سطح الخلية في كل من مجموعتي البيانات الشاملة والمخصصة للسطح. أظهرت الميكروسكوبي أن C3ORF18 موجود قرب مركز الخلية وفي حويصلات صغيرة، العديد منها يتداخل مع الحويصلات التي تحمل مستقبل الترانسفرين، وهو بروتين إعادة تدوير معروف، ومع GLUT4، ناقل السكر الرئيسي. عند إضافة الإنسولين أو عوامل النمو، انتقل C3ORF18 سريعًا إلى سطح الخلية بطريقة تعتمد على نفس الفرع الإشاراتي المستخدم لنقل GLUT4. يشير هذا السلوك إلى أن C3ORF18 يسافر في مسار إعادة تدوير حساس للإنسولين يساعد على توصيل الناقلات المهمة إلى الغشاء.
ماذا يحدث عند غياب اللاعب الجديد
لاختبار ما إذا كان C3ORF18 يفعل أكثر من مجرد المرافقة، خفّض الباحثون مستوياته انتقائيًا في خلايا دهنية ناضجة من فئران وبشر. على مدى عدة أيام، أصبحت الخلايا الخالية من C3ORF18 أقل استجابة للإنسولين: انخفض امتصاص السكر، وتناقصت كميات كل من GLUT4 وناقل سكر آخر هو GLUT1. كما تراجعت حركة GLUT4 ومستقبل الترانسفرين نحو السطح نتيجة الإنسولين، وضعفت خطوات الإشارة الجوهرية المتعاقبة لمستقبل الإنسولين. مبكرًا بعد نقص C3ORF18، ظهرت المشاكل أولًا في إعادة تدوير مستقبلات الترانسفرين، ملمّحة إلى أن اضطراب إعادة التدوير الإندوزومي قد يكون نقطة البداية التي تقود في النهاية إلى تقويض التأثيرات الأوسع للإنسولين. دعمت بيانات من نسيج دهني بشري هذا التصور أيضًا: الأشخاص ذوو مستويات سكر دم ونُظم الجلوكوز طويلة الأمد الأعلى ميالون إلى وجود تعبير أقل لـ C3ORF18، وزادت مستوياته مع فقدان الوزن.
خلاصات عامة لفهم حساسية الإنسولين
تُظهر هذه الدراسة أن استجابة الإنسولين الناجحة في الخلايا الدهنية تعتمد ليس فقط على أي البروتينات موجودة، بل أيضًا على أماكن تواجدها داخل الخلية في أي لحظة. يعيد الإنسولين بسرعة توزيع مئات البروتينات، خصوصًا على سطح الخلية وداخل مقصورات إعادة التدوير، وتعمل هذه التغييرات المكانية جنبًا إلى جنب مع التعديلات الكيميائية مثل الفسفرة. من خلال رسم هذه الحركة بشكل منهجي، اكتشف المؤلفون C3ORF18 كمساعد لم يكن معروفًا سابقًا يدعم مسارات إعادة التدوير اللازمة لامتصاص السكر بكفاءة والإشارات الصحية للإنسولين. يفتح فهم مثل هذه الديناميكيات المكانية آفاقًا جديدة لاستكشاف سبب تآكل حساسية الإنسولين في الأمراض الأيضية وقد يشير في نهاية المطاف إلى أهداف للحفاظ على هذه الاستجابة الهرمونية أو استعادتها.
الاستشهاد: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
الكلمات المفتاحية: مقاومة الإنسولين, خلية دهنية, نقل البروتينات, بروتيوميات مكانية, امتصاص الجلوكوز