Clear Sky Science · nl
Dynamische subcellulaire proteomica identificeert regulatoren van insulinewerking in adipocyten
Waarom dit belangrijk is voor alledaagse gezondheid
Insuline is een hormoon dat vooral bekendstaat om het reguleren van de bloedsuikerspiegel, en wanneer het faalt kunnen aandoeningen zoals type 2-diabetes ontstaan. Deze studie kijkt in vetcellen om — op ongekende detailniveau — te zien hoe duizenden eiwitten snel van plaats verschuiven wanneer insuline binnenkomt. Door deze moleculaire herschikking te volgen, onthullen de onderzoekers nieuwe spelers die vetcellen helpen goed op insuline te reageren, wat nieuwe aanwijzingen geeft waarom insuline soms zijn werking verliest.
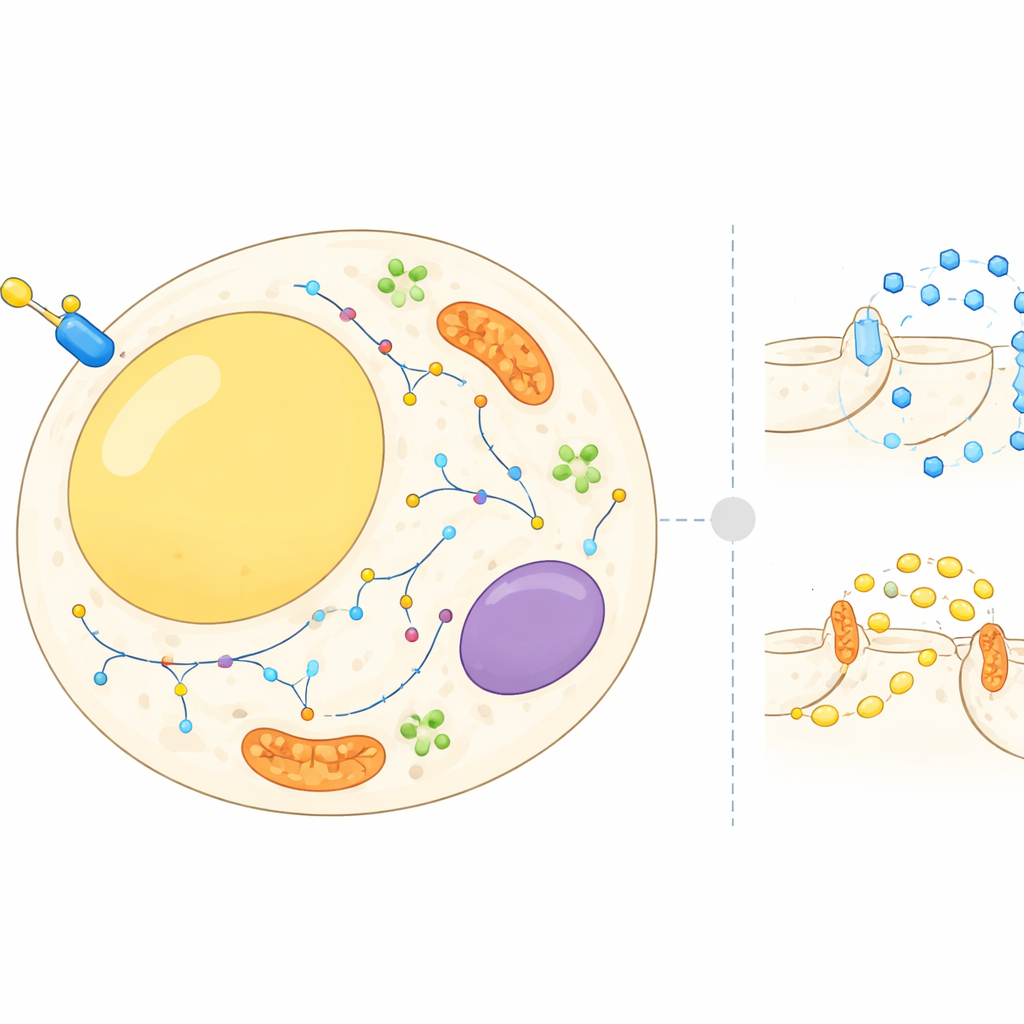
Een bewegende kaart binnen vetcellen
Vetcellen zijn niet alleen passieve opslagplaatsen; ze balanceren voortdurend tussen het opslaan en vrijgeven van energie als reactie op hormonen en voedingsstoffen. Insuline geeft deze cellen het signaal om suiker uit het bloed te halen en de afbraak van opgeslagen vet te remmen. Hiervoor moeten veel eiwitten tussen verschillende cellulaire compartimenten bewegen, zoals het celoppervlak, interne membranen en kleine transportblaasjes. Tot nu toe richtte het meeste onderzoek zich op een paar goed bestudeerde eiwitten. In dit werk bouwden de auteurs een celbrede atlas van waar duizenden eiwitten zich bevinden in vetcellen vóór en ná een insulinepiek, en hoe hun locaties binnen enkele minuten veranderen.
Hoe het eiwitlandschap in kaart is gebracht
Het team gebruikte een benadering die subcellulaire proteomica heet, een combinatie van celfragmentatie en massaspectrometrie om eiwitten in verschillende delen van de cel tegelijk te meten. Ze werkten met 3T3-L1-cellen, een standaard muismodel voor vetcellen, en scheidden elk monster in meerdere fracties die verrijkt waren voor structuren zoals het celoppervlak, energiefabriekjes, recyclingscompartimenten en vetdruppels. Een statistisch raamwerk vergeleek vervolgens de distributie van elk eiwit in rustende cellen versus insulinegestimuleerde cellen. Parallel gebruikten de onderzoekers een aparte methode die selectief eiwitten op het buitenoppervlak van de cel labelde, zodat ze konden kwantificeren hoeveel van elk membraaneiwit toe- of afnam na insulinebehandeling.
Insuline veroorzaakt wijdverbreide herschikking van eiwitten
De gecombineerde datasets toonden aan dat insuline een opvallende reorganisatie in gang zet: meer dan 500 eiwitten vertoonden verschuivingen in locatie met hoge betrouwbaarheid. Velen behoorden tot bekende signaalroutes, inclusief componenten die voedingsstoffen detecteren en groei reguleren, evenals proteïnekinasen die andere eiwitten aan- of uitzetten. Anderen waren betrokken bij het verkeer van vesikels die moleculen tussen interne compartimenten en het celoppervlak verplaatsen. Sommige transportcomplexen bewogen duidelijk als reactie op insuline, terwijl andere op hun plaats bleven, wat suggereert dat het hormoon specifieke takken van het cellulaire transportsysteem target. De op het oppervlakte gerichte experimenten lieten zien dat meer dan 300 eiwitten in hoeveelheid veranderden aan het buitenmembraan, wat bevestigt dat de ‘interface’ van de cel met zijn omgeving tijdens een insulinerespons wordt hervormd.
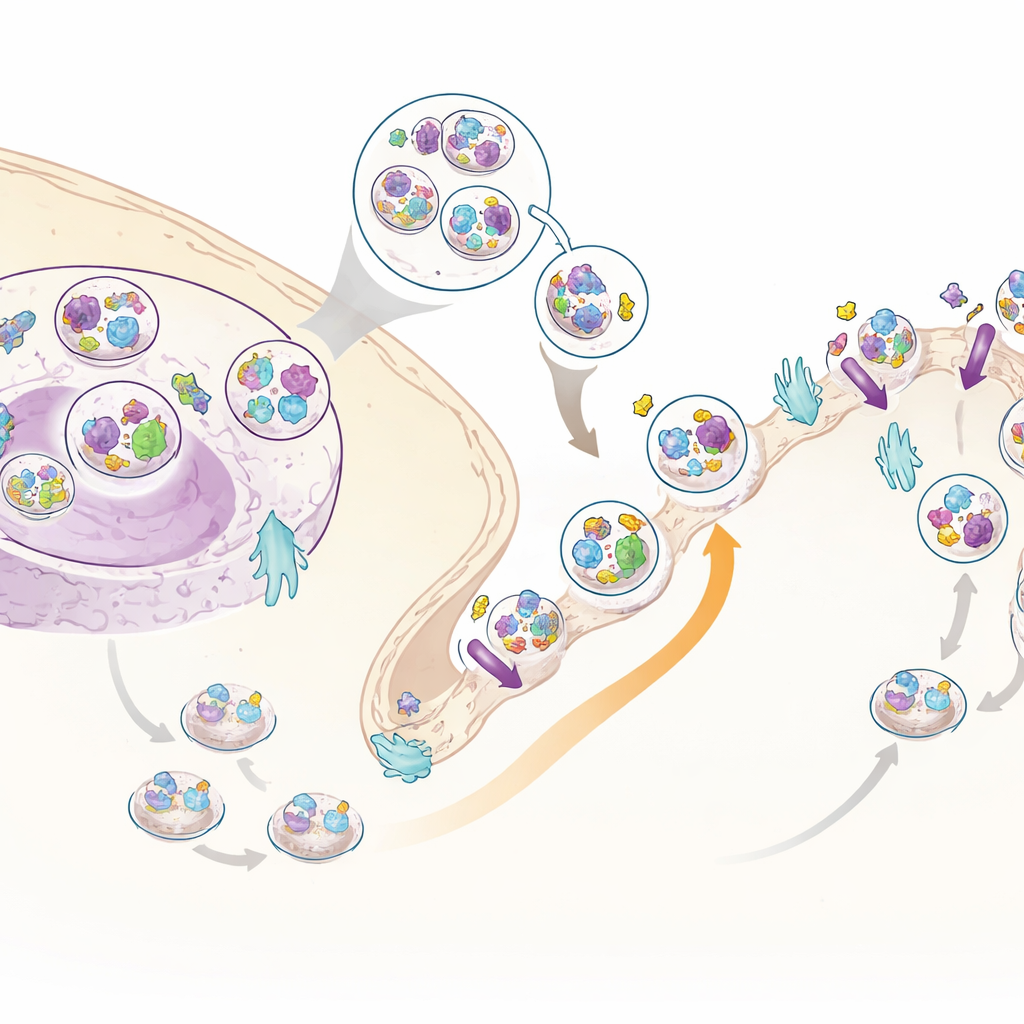
Een nieuwe insulinehelper: C3ORF18
Onder de vele bewegende eiwitten viel er één op: een weinig bestudeerd eiwit genaamd C3ORF18. Het werd sterk naar het celoppervlak getrokken door insuline in zowel de hele-cel- als de oppervlakte-specifieke datasets. Microscopen toonden dat C3ORF18 dicht bij het midden van de cel en in kleine vesikels zit, waarvan er veel overlappen met die die de transferrinereceptor vervoeren, een bekend recyclingeiwit, en met GLUT4, een belangrijke suikertransporter. Wanneer insuline of groeifactoren werden toegevoegd, bewoog C3ORF18 snel naar het celoppervlak op een manier die afhankelijk was van dezelfde signaalroute als GLUT4. Dit gedrag suggereert dat C3ORF18 meereist in een insulinegevoelige recyclingroute die helpt belangrijke transporters naar het membraan te brengen.
Wat gebeurt er als de nieuwe speler ontbreekt
Om te testen of C3ORF18 meer doet dan alleen meereizen, verlaagden de onderzoekers selectief de niveaus ervan in rijpe muis- en menselijke vetcellen. Na enkele dagen werden cellen zonder C3ORF18 minder responsief op insuline: de suikeropname daalde en zowel GLUT4 als een andere suikertransporter, GLUT1, waren minder overvloedig. Insulinegestuurde verplaatsing van GLUT4 en de transferrinereceptor naar het oppervlak werd ook afgezwakt, en kernstappen in de signaalweg stroomafwaarts van de insulinereceptor werden verzwakt. Vroeg na depletie van C3ORF18 deden zich eerst problemen voor in het recyclen van transferrinereceptoren, wat hint dat verstoringen in endosomaal recyclen het beginpunt kunnen zijn dat uiteindelijk de bredere effecten van insuline ondermijnt. Gegevens uit menselijk vetweefsel ondersteunden dit beeld: mensen met hogere bloedsuiker en langetermijnmarkers van glucose hadden de neiging lagere expressie van C3ORF18 te hebben, en de niveaus stegen bij gewichtsverlies.
Grote conclusies voor het begrijpen van insulinegevoeligheid
Deze studie laat zien dat een succesvolle insulinerespons in vetcellen niet alleen afhankelijk is van welke eiwitten aanwezig zijn, maar ook van waar ze zich op elk moment in de cel bevinden. Insuline herverdeelt snel honderden eiwitten, vooral aan het celoppervlak en binnen recyclingscompartimenten, en deze locatieveranderingen werken samen met chemische modificaties zoals fosforylering. Door deze beweging systematisch in kaart te brengen, ontdekten de auteurs C3ORF18 als een voorheen onontdekte helper die de recyclingroutes ondersteunt die nodig zijn voor efficiënte suikeropname en gezonde insulinesignalering. Het begrijpen van zulke ruimtelijke dynamiek opent nieuwe wegen om te onderzoeken waarom insulinegevoeligheid in metabole ziekten afneemt en kan uiteindelijk wijzen op targets om deze cruciale hormoonrespons te behouden of te herstellen.
Bronvermelding: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
Trefwoorden: insulineresistentie, adipocyt, proteïnetransport, ruimtelijke proteomica, glucoseopname