Clear Sky Science · pl
Dynamiczne subkomórkowe proteomiki identyfikuje regulatory działania insuliny w adipocytach
Dlaczego to ma znaczenie dla zdrowia codziennego
Insulina to hormon najbardziej znany z utrzymywania poziomu cukru we krwi pod kontrolą; gdy zawodzi, mogą rozwinąć się choroby takie jak cukrzyca typu 2. To badanie zagląda do wnętrza komórek tłuszczowych, aby z bezprecedensową szczegółowością zobaczyć, jak tysiące białek szybko zmieniają swoje położenie po pojawieniu się insuliny. Śledząc to molekularne przemieszczenie, autorzy odkrywają nowe elementy, które pomagają adipocytom prawidłowo reagować na insulinę, dając świeże wskazówki, dlaczego insulina czasem przestaje działać tak, jak powinna.
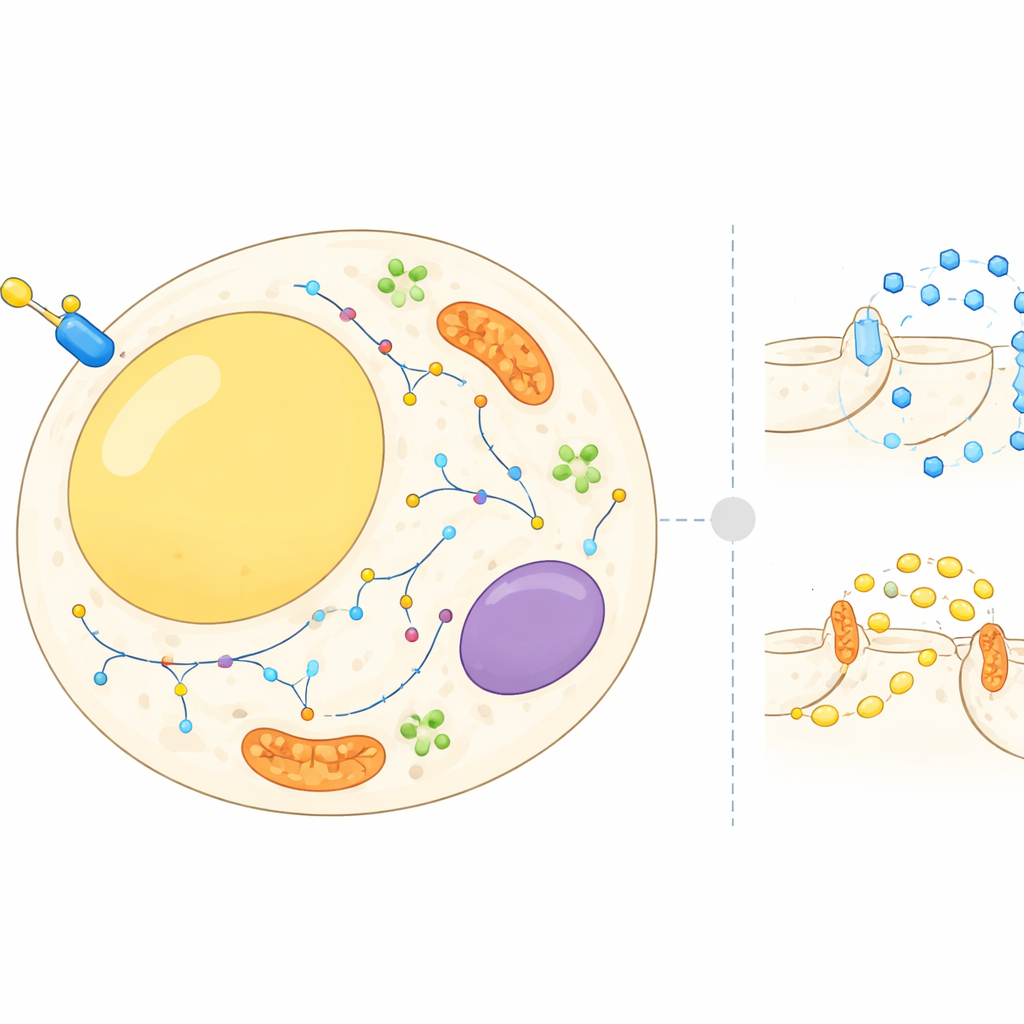
Ruchoma mapa wewnątrz komórek tłuszczowych
Komórki tłuszczowe to nie tylko bierne magazyny; nieustannie równoważą magazynowanie i uwalnianie energii w odpowiedzi na hormony i składniki odżywcze. Insulina nakazuje tym komórkom pobierać cukier z krwi i spowolnić rozkład zmagazynowanych tłuszczów. Aby to osiągnąć, wiele białek musi przemieszczać się między różnymi przedziałami komórkowymi, takimi jak powierzchnia komórki, wewnętrzne błony i drobne pęcherzyki transportowe. Dotychczas większość badań koncentrowała się na kilku dobrze znanych białkach. W tej pracy autorzy postawili sobie za cel stworzenie atlasu całej komórki pokazującego, gdzie tysiące białek znajdują się w adipocytach przed i po impulsie insulinowym oraz jak ich lokalizacje zmieniają się w ciągu kilku minut.
Jak sporządzono mapę białkowego krajobrazu
Zespół zastosował podejście zwane subkomórkową proteomiką, które łączy frakcjonowanie komórek i spektrometrię mas do jednoczesnego pomiaru białek w różnych częściach komórki. Pracowali na komórkach 3T3-L1, standardowym modelu mysich komórek tłuszczowych, i rozdzielili każdy próbkę na wiele frakcji wzbogaconych w struktury takie jak powierzchnia komórki, „fabryki” energii, przedziały recyklingowe i krople tłuszczu. Ramy statystyczne porównywały następnie rozkład każdego białka w komórkach spoczynkowych i po stymulacji insulinowej. Równolegle badacze użyli oddzielnej metody, która selektywnie znakowała białka eksponowane na zewnętrznej powierzchni komórki, co pozwoliło ilościowo ocenić, ile każdego białka powierzchniowego wzrosło lub spadło po leczeniu insuliną.
Insulina wywołuje szerokie przemieszczenia białek
Połączone zbiory danych ujawniły, że insulina wywołuje uderzającą reorganizację: ponad 500 białek wykazało przesunięcia o wysokim stopniu pewności. Wiele z nich należało do znanych szlaków sygnałowych, w tym składników wyczuwających składniki odżywcze i regulujących wzrost, a także kinaz białkowych, które włączają lub wyłączają inne białka. Inne uczestniczyły w transporcie pęcherzyków przenoszących ładunek między przedziałami wewnętrznymi a powierzchnią komórki. Niektóre kompleksy transportowe przemieszczały się wyraźnie w odpowiedzi na insulinę, podczas gdy inne pozostawały na miejscu, co sugeruje, że hormon celuje w określone gałęzie sieci transportowej komórki. Eksperymenty skupione na powierzchni wykazały, że ponad 300 białek zmieniło obfitość na błonie zewnętrznej, potwierdzając, że „interfejs” komórki z otoczeniem jest przekształcany podczas odpowiedzi na insulinę.
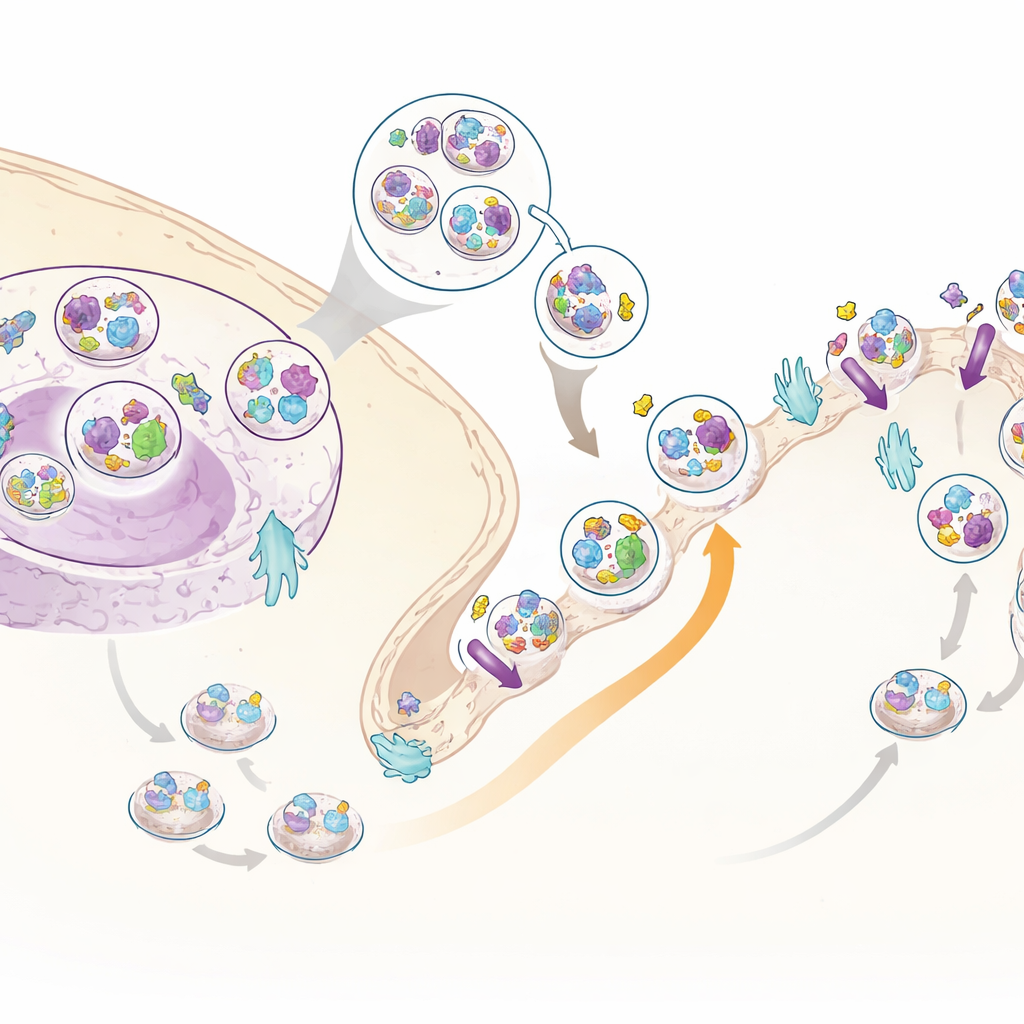
Nowy pomocnik insuliny: C3ORF18
Wśród wielu przemieszczających się białek jedno wyróżniało się: słabo zbadane białko o nazwie C3ORF18. Insulina silnie przesuwała je w kierunku powierzchni komórki zarówno w zestawie danych całokomórkowych, jak i w danych specyficznych dla powierzchni. Mikroskopia pokazała, że C3ORF18 lokalizuje się w pobliżu środka komórki i w małych pęcherzykach, z których wiele nakłada się z pęcherzykami niosącymi receptor transferyny, dobrze znane białko recyklingowe, oraz z GLUT4, kluczowym transporterem cukru. Po dodaniu insuliny lub czynników wzrostu C3ORF18 szybko przenosił się na powierzchnię komórki w sposób zależny od tej samej gałęzi sygnałowej, co GLUT4. To zachowanie sugeruje, że C3ORF18 podróżuje w insulinowrażliwej trasie recyklingowej, która pomaga dostarczać ważne transportery do błony.
Co się dzieje, gdy brakuje nowego gracza
Aby sprawdzić, czy C3ORF18 robi coś więcej niż tylko „towarzyszyć”, badacze selektywnie obniżyli jego poziomy w dojrzałych mysich i ludzkich komórkach tłuszczowych. W ciągu kilku dni komórki pozbawione C3ORF18 stały się mniej wrażliwe na insulinę: spadł pobór cukru, a zarówno GLUT4, jak i inny transporter glukozy, GLUT1, były mniej obfite. Ruch GLUT4 i receptora transferyny na powierzchnię komórki wywołany insuliną był również osłabiony, a kluczowe etapy sygnalizacji poniżej receptora dla insuliny zostały osłabione. Wczesne po wyczerpaniu C3ORF18 problemy pojawiły się najpierw w recyklingu receptorów transferyny, co sugeruje, że zaburzenia w endosomalnym recyklingu mogą być punktem wyjścia, który ostatecznie podważa szersze efekty insuliny. Dane z ludzkiej tkanki tłuszczowej dodatkowo wspierały ten obraz: osoby z wyższym poziomem cukru we krwi i podwyższonymi długoterminowymi markerami glikemii miały zwykle niższą ekspresję C3ORF18, a jego poziomy rosły wraz z utratą masy ciała.
Kluczowe wnioski dla zrozumienia wrażliwości na insulinę
Badanie pokazuje, że skuteczna odpowiedź na insulinę w komórkach tłuszczowych zależy nie tylko od tego, które białka są obecne, lecz także od tego, gdzie w danym momencie się znajdują. Insulina szybko przekierowuje setki białek, szczególnie na powierzchni komórki i w przedziałach recyklingowych, a te zmiany lokalizacji działają równolegle z modyfikacjami chemicznymi, takimi jak fosforylacja. Systematycznie mapując te przemieszczenia, autorzy odkryli C3ORF18 jako dotąd nieznanego pomocnika, który wspiera trasy recyklingowe niezbędne do efektywnego poboru cukru i prawidłowej sygnalizacji insulinowej. Zrozumienie takich dynamik przestrzennych otwiera nowe drogi badawcze wyjaśniające, dlaczego wrażliwość na insulinę eroduje w chorobach metabolicznych, i może w przyszłości wskazać cele do zachowania lub przywrócenia tej kluczowej odpowiedzi hormonalnej.
Cytowanie: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
Słowa kluczowe: oporność na insulinę, adipocyt, transport białek, proteomika przestrzenna, pobór glukozy