Clear Sky Science · it
Proteomica subcellulare dinamica identifica regolatori dell’azione dell’insulina negli adipociti
Perché questo è importante per la salute quotidiana
L’insulina è un ormone noto soprattutto per mantenere sotto controllo lo zucchero nel sangue e, quando non funziona correttamente, può portare a condizioni come il diabete di tipo 2. Questo studio esplora l’interno delle cellule adipose per osservare, con dettaglio senza precedenti, come migliaia di proteine cambino rapidamente posizione all’arrivo dell’insulina. Tracciando questo rimescolamento molecolare, i ricercatori individuano nuovi elementi che aiutano gli adipociti a rispondere correttamente all’insulina, offrendo indizi utili sul motivo per cui l’insulina a volte smette di funzionare come dovrebbe.
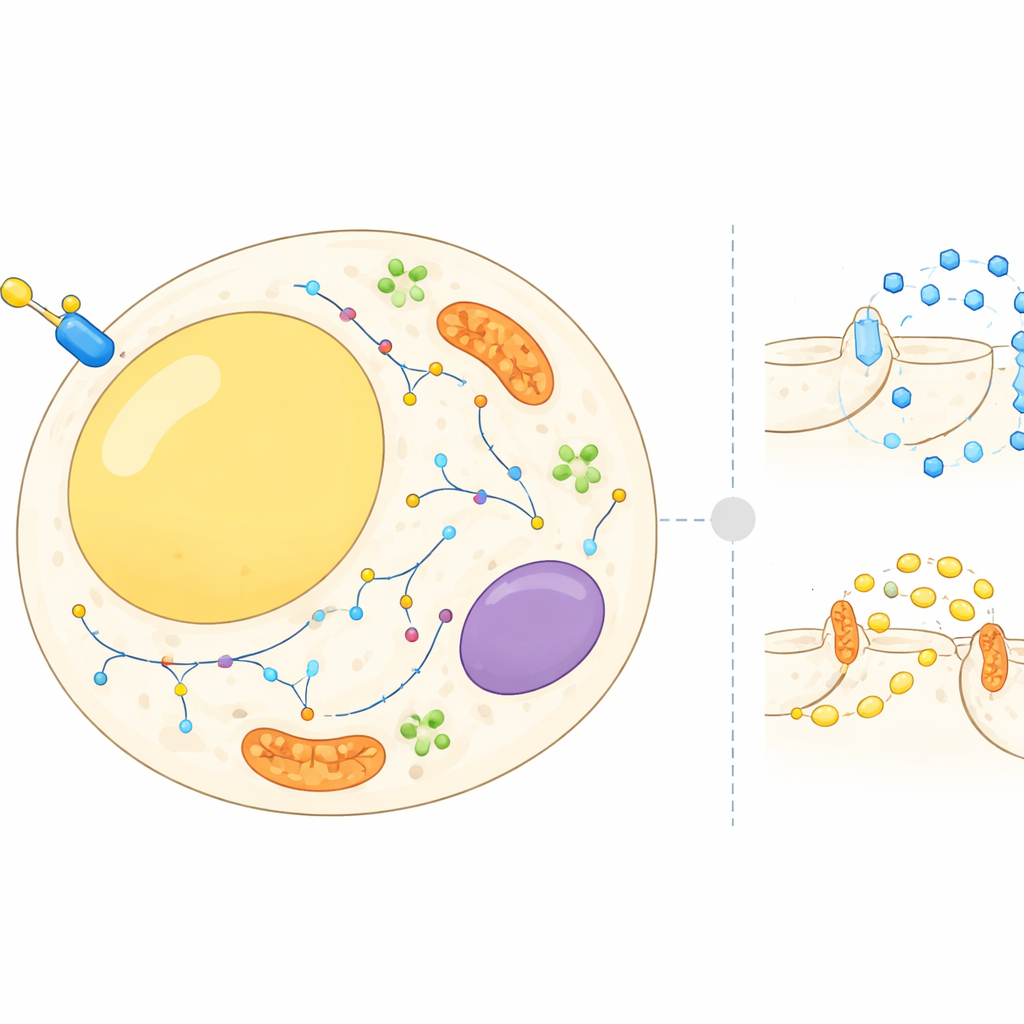
Una mappa in movimento all’interno delle cellule adipose
Le cellule adipose non sono semplici depositi passivi; bilanciano continuamente immagazzinamento e rilascio di energia in risposta a ormoni e nutrienti. L’insulina segnala a queste cellule di prelevare zucchero dal sangue e di rallentare la degradazione dei grassi immagazzinati. Per farlo, molte proteine devono spostarsi tra diversi compartimenti cellulari, come la superficie cellulare, le membrane interne e le piccole vescicole di trasporto. Finora, la maggior parte delle ricerche si è concentrata su poche proteine ben conosciute. In questo lavoro, gli autori si sono posti l’obiettivo di costruire un atlante cellulare su vasta scala delle posizioni di migliaia di proteine negli adipociti prima e dopo un picco di insulina e di come queste posizioni cambino nel giro di pochi minuti.
Come è stato tracciato il paesaggio proteico
Il gruppo ha utilizzato un approccio chiamato proteomica subcellulare, che combina frazionamento cellulare e spettrometria di massa per misurare le proteine nelle diverse parti della cellula contemporaneamente. Hanno lavorato con cellule 3T3-L1, un modello murino standard di adipociti, e hanno separato ogni campione in più frazioni arricchite per strutture come la superficie cellulare, le centrali energetiche, i compartimenti di riciclo e le gocce lipidiche. Un quadro statistico ha quindi confrontato la distribuzione di ciascuna proteina nelle cellule a riposo rispetto a quelle stimolate con insulina. Parallelamente, i ricercatori hanno usato un metodo separato che etichetta selettivamente le proteine esposte sulla superficie esterna della cellula, permettendo di quantificare quanto ciascuna proteina di superficie aumentasse o diminuisse dopo il trattamento con insulina.
L’insulina scatena un ampio rimescolamento proteico
I dataset combinati hanno rivelato che l’insulina induce una riorganizzazione significativa: più di 500 proteine hanno mostrato spostamenti con elevata confidenza nelle loro localizzazioni. Molte appartenevano a vie di segnalazione note, inclusi componenti che percepiscono i nutrienti e regolano la crescita, oltre a chinasi proteiche che attivano o disattivano altre proteine. Altre erano coinvolte nel traffico di vescicole che trasportano carichi tra i compartimenti interni e la superficie cellulare. Alcuni complessi di trasporto si sono mossi in modo evidente in risposta all’insulina, mentre altri sono rimasti stazionari, suggerendo che l’ormone colpisce rami specifici della rete di trasporto cellulare. Gli esperimenti focalizzati sulla superficie hanno mostrato che oltre 300 proteine cambiarono in abbondanza sulla membrana esterna, confermando che l’“interfaccia” della cellula con l’ambiente viene rimodellata durante la risposta all’insulina.
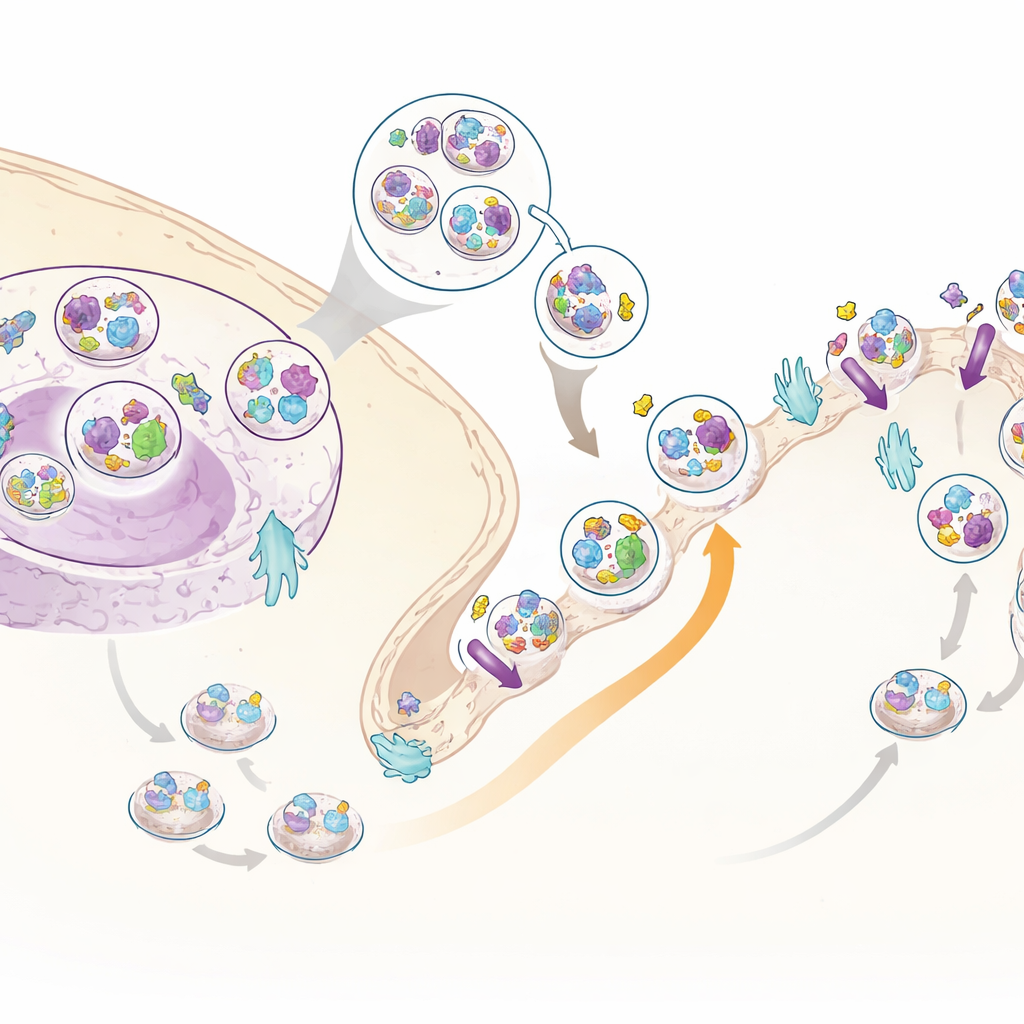
Un nuovo alleato dell’insulina: C3ORF18
Tra le molte proteine in movimento, una spiccava: una proteina poco studiata chiamata C3ORF18. Essa veniva fortemente richiamata verso la superficie cellulare dall’insulina sia nei dataset di ghiacciaio cellulare totale sia in quelli specifici per la superficie. La microscopia mostrò che C3ORF18 si trova vicino al centro della cellula e in piccole vescicole, molte delle quali si sovrappongono a quelle che trasportano il recettore per la transferrina, una proteina di riciclo nota, e con GLUT4, un trasportatore di zuccheri chiave. Quando sono stati aggiunti insulina o fattori di crescita, C3ORF18 si è spostata rapidamente verso la superficie cellulare in un modo che dipende dallo stesso ramo di segnalazione usato da GLUT4. Questo comportamento suggerisce che C3ORF18 viaggi in una via di riciclo sensibile all’insulina che aiuta a portare trasportatori importanti alla membrana.
Cosa succede quando il nuovo attore manca
Per testare se C3ORF18 facesse qualcosa di più che accompagnare altri componenti, i ricercatori ne hanno ridotto selettivamente i livelli in adipociti maturi di topo e umani. Nel giro di alcuni giorni, le cellule prive di C3ORF18 sono diventate meno reattive all’insulina: l’assorbimento di zucchero è diminuito e sia GLUT4 sia un altro trasportatore di zuccheri, GLUT1, sono risultati meno abbondanti. Anche il movimento indotto dall’insulina di GLUT4 e del recettore per la transferrina verso la superficie è stato attenuato, e i passaggi fondamentali della segnalazione a valle del recettore dell’insulina sono risultati indeboliti. Nelle fasi iniziali dopo la deplezione di C3ORF18, i problemi sono comparsi prima nel riciclo dei recettori per la transferrina, suggerendo che le alterazioni nel riciclo endosomiale possano essere il punto di partenza che alla fine compromette gli effetti più ampi dell’insulina. Dati provenienti da tessuto adiposo umano supportano ulteriormente questa visione: persone con livelli più alti di glucosio nel sangue e con marker glicemici a lungo termine tendevano ad avere un’espressione più bassa di C3ORF18, e i suoi livelli aumentavano con la perdita di peso.
Principali conclusioni per comprendere la sensibilità all’insulina
Questo studio dimostra che una risposta all’insulina efficace negli adipociti dipende non solo da quali proteine sono presenti, ma anche da dove si trovano nella cellula in un dato momento. L’insulina ridistribuisce rapidamente centinaia di proteine, soprattutto sulla superficie cellulare e nei compartimenti di riciclo, e questi cambiamenti di localizzazione operano insieme a modificazioni chimiche come la fosforilazione. Mappando sistematicamente questo movimento, gli autori hanno scoperto C3ORF18 come un alleato finora non riconosciuto che supporta le vie di riciclo necessarie per un efficiente assorbimento degli zuccheri e una segnalazione dell’insulina sana. Comprendere tali dinamiche spaziali apre nuove strade per esplorare perché la sensibilità all’insulina si deteriora nelle malattie metaboliche e potrebbe alla fine indicare obiettivi per preservare o ripristinare questa risposta ormonale cruciale.
Citazione: Conway, O.J., Christopher, J.A., Breckels, L.M. et al. Dynamic subcellular proteomics identifies regulators of adipocyte insulin action. Nat Commun 17, 3310 (2026). https://doi.org/10.1038/s41467-026-70116-9
Parole chiave: resistenza all’insulina, adipocita, traffico proteico, proteomica spaziale, assorbimento del glucosio