Clear Sky Science · tr
SHP2 üzerindeki bir sıcak nokta fosforilasyon bölgesi onkoprotein aktivasyonunu ve ilaç direncini tetikliyor
Gelecekteki kanser tedavileri için bunun önemi
Modern kanser ilaçlarının çoğu, tümör hücreleri içindeki aşırı aktif büyüme sinyallerini kapatmayı hedefliyor. Ümit vadeden hedeflerden biri, hücre yüzeyindeki sinyalleri hücrenin iç büyüme motoruna bağlayan anahtar bir geçiş noktası olan SHP2 proteini oldu. Buna karşın SHP2’yi kapatmak üzere tasarlanan ilaçlar erken klinik denemelerde neredeyse hiç fayda göstermedi. Bu makale SHP2 üzerinde saklı bir “açma düğmesini” ortaya koyuyor; bu, bu ilaçların neden sıklıkla başarısız olduğunu açıklamaya yardımcı oluyor ve dirençli tümörleri alt etmenin yeni yollarını işaret ediyor.
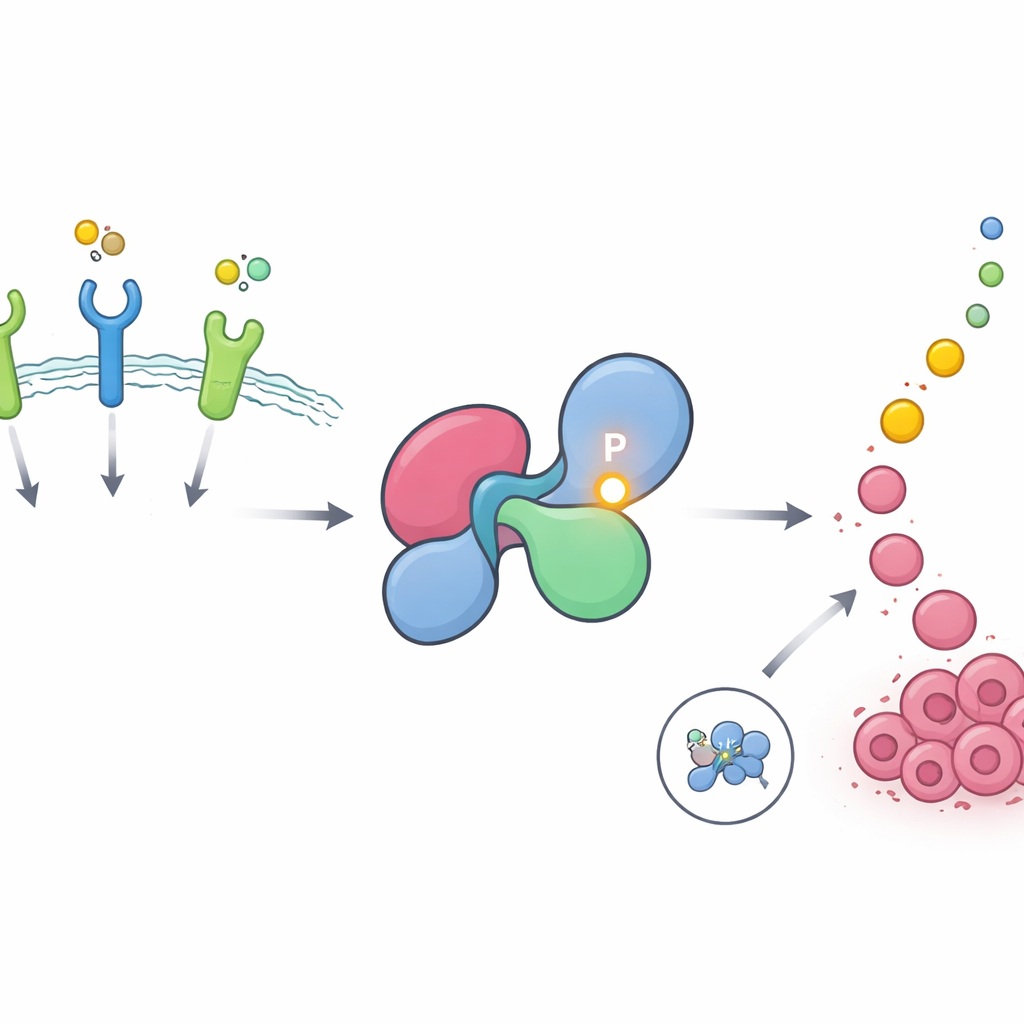
Hayati bir büyüme anahtarında saklı bir sıcak nokta
SHP2, hücre yüzeyindeki reseptör tirozin kinazlar olarak adlandırılan reseptörlerden gelen mesajları RAS–MAPK yoluna iletmeye yardım eder; bu yol hücre büyümesi ve bölünmesinin ana iticisidir. Sağlıklı hücrelerde SHP2 genellikle kapalı durumda kalır; kendi aktif bölgesini engelleyen katlanmış bir yapıdadır. Reseptörler uyarıldığında kısa süre açılır, sonra tekrar kapanır. Yazarlar, fosfat gruplarının eklenmesiyle sıkça modifiye edilen protein bölgelerini aramak için geniş fosfoproteomik veritabanlarını kullandılar. SHP2’deki belirli bir pozisyonun, tirozin 62 olarak adlandırılan yerin, tüm insan proteomunda en çok ve tekrarlayan şekilde fosforilasyon görülen bölgeler arasında olduğunu ve özellikle EGFR ve FGFR gibi büyüme faktörü reseptörleriyle tetiklenen tümörlerde zenginleştiğini buldular.
Farklı kanserler, aynı anahtara farklı bağımlılık
Hastaya ait tümör veri kümelerini inceleyerek araştırmacılar, SHP2’nin Y62 bölgesindeki fosforilasyonun EGFR değişiklikleri olan bazı akciğer kanserleri, safra yolu kanserleri, baş ve boyun tümörleri ve beyin tümörleri dahil olmak üzere birkaç reseptör kaynaklı kanserde güçlü biçimde arttığını gösterdiler. Dikkat çekici şekilde, bazı akciğer kanserlerinde SHP2 Y62 fosforilasyonu, reseptörün kendisindeki fosforilasyondan bile daha yüksek bulundu. Buna karşılık, aynı büyüme yolunu daha aşağıdan aktive eden mutant KRAS ile sürülen tümörlerde SHP2 Y62 fosforilasyon düzeyleri azalmıştı. Bu desen, reseptör sinyallerine bağlı kanserlerin genellikle devrelerinde SHP2 Y62’yi yükselttiğini, yolun daha aşağısında mutasyonlar olanların ise bu özel anahtara ihtiyaç duymadığını öne sürüyor.
Başka bir kinaz ailesi bu sıcak noktayı nasıl kontrol ediyor
İlk bakışta yüzey reseptörlerinin SHP2’yi doğrudan Y62 üzerinde modifiye ettiği düşünülebilirdi. Ancak ekip çeşitli reseptörleri hedefleyen ilaçlarla bloke ettiğinde, Y62 fosforilasyonu neredeyse değişmedi. Bunun yerine, modifikasyonu SRC ailesi kinazları olarak bilinen farklı bir enzim grubuna bağladılar. Geniş ve seçici SRC-aile inhibitörlerinin kombinasyonunu, SRC, YES1 ve FYN eksik genlerine sahip genetik yok etme hücrelerini ve saflaştırılmış proteinlerle tüpte yapılan reaksiyonları kullanarak bu kinazların SHP2’ye doğrudan Y62’de ve ayrıca SHP2 kuyruğundaki iki daha bilinen bölgede fosfat grupları eklediğini gösterdiler. Bu, etkinleşmiş reseptörler ile SHP2 arasında kritik aracılar olarak SRC-aile kinazlarını konumlandırır ve bir RTK–SRC–SHP2 sinyal ekseni oluşturur.
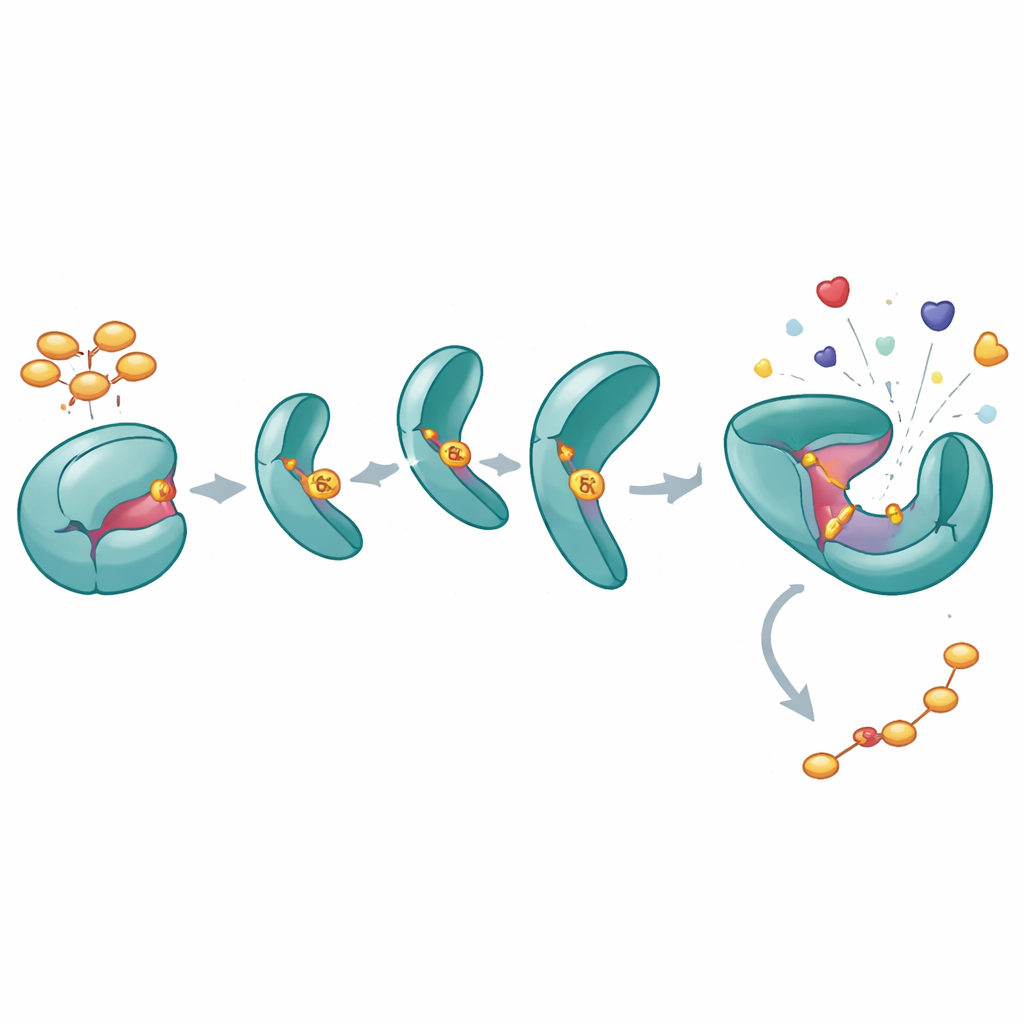
Bir fosfat nasıl SHP2’yi tamamen açık tutuyor
Y62 fosforilasyonunun SHP2 üzerinde ne yaptığını anlamak için yazarlar, Y62’nin sürekli fosforileymiş gibi davranan bir “fosfomimetik” versiyon (Y62D) tasarladılar. Biyokimyasal tahliller, bu varyantın daha yüksek katalitik aktiviteye sahip olduğunu ve tipik olarak SHP2’yi kapalı halinden “kilidi açan” aktive edici peptitlere normal şekilde yanıt vermediğini gösterdi. Termal stabilite ölçümleri ve hidrojen–deuteryum değişimi deneyleri, Y62D proteinin özellikle düzenleyici ve katalitik domainleri arasındaki ara yüzde daha açık, esnek konformasyonları daha sık örneklediğini ortaya koydu. Y62D’nin kristal yapısı kapalı formda yakalansa da dinamik ölçümler, çözelti içinde bu mutantın sıklıkla açık, aktif benzeri bir duruma geçiş yaptığını ve normal oto-inhibisyonu atladığını gösterdi.
Mevcut SHP2 ilaçlarının klinikte neden zorlandığı
Mevcut allosterik SHP2 inhibitörleri, SHP2’nin kapalı, inaktif şeklini stabilize ederek etkili biçimde domainlerini birbirine “yapıştırır”. Yazarlar, saflaştırılmış protein deneylerinde Y62D formunun bu ilaçlara daha az duyarlı olduğunu gösterdiler. Normal SHP2 geni Y62D ile değiştirilen kanser hücre hatlarında MAPK yoluyla büyüme sinyali, üç farklı klinik aşamadaki SHP2 inhibitörü ile muamele edildiğinde bile yüksek kaldı. Bu hücreler ayrıca SHP2’ye bağlı olan anahtar bir sinyal adaptörü olan GAB1’in fosforilasyonunu sürdürdü; bu, ilaç tedavisine rağmen SHP2’nin fonksiyonel olarak aktif kalmaya devam ettiğini vurguluyor. Birlikte veriler, SRC-aile kinazlarının SHP2’yi Y62’de fosforile ederek onu mevcut ilaçların verimli şekilde kilitleyemediği açık, aktif bir konformasyona zorladığı modelini destekliyor.
Yarınki kanser tedavileri için anlamı
Çalışma, SHP2 Y62 fosforilasyonunu, kalıcı aktive edici mutasyonların etkisini taklit eden fakat DNA’da değişiklik olmadan ortaya çıkan ortak ve ilaç açısından alaka düzeyi yüksek bir anahtar olarak tanımlıyor. Bu bulgu, büyüme faktörü reseptörleri tarafından sürülen kanserlerin, SHP2 genleri sekanslanmış olsa bile mevcut SHP2 inhibitörlerine karşı doğal olarak dirençli olmasının nedenini açıklamaya yardımcı olur. Y62 fosforilasyonunun ölçülmesi, hangi tümörlerin bu ilaçlara yanıt vermeyeceğini öngören bir biyobelirteç olarak hizmet edebilir. Daha da önemlisi, çalışma Y62-fosforile SHP2’yi ayrı bir yapısal hedef olarak vurguluyor ve etkili stratejilerin ya yukarı akışta SRC-aile kinazlarını bloke etmeyi ya da SHP2’nin açık, fosforile formunu doğrudan tanıyıp kapatabilecek yeni inhibitörler tasarlamayı gerektirebileceğini öne sürüyor.
Atıf: Karunaraj, P., Scheele, R., Wells, M.L. et al. A hotspot phosphorylation site on SHP2 drives oncoprotein activation and drug resistance. Nat Commun 17, 3383 (2026). https://doi.org/10.1038/s41467-026-70060-8
Anahtar kelimeler: SHP2, fosforilasyon, SRC kinazları, MAPK sinyalizasyonu, ilaç direnci