Clear Sky Science · ar
موقع فسفرة ساخن على SHP2 يحفز تنشيط البروتين المسرطِر ومقاومة الدواء
لماذا يهم هذا لعلاجات السرطان المستقبلية
تهدف العديد من أدوية السرطان الحديثة إلى إيقاف إشارات النمو المفرطة داخل خلايا الورم. كان الهدف الواعد أحد بروتينات تُدعى SHP2، وهو مفتاح رئيسي يربط الإشارات عند سطح الخلية بمحرك النمو الداخلي. ومع ذلك، أظهرت الأدوية المصممة لإيقاف SHP2 فوائد ضئيلة تقريبًا في التجارب السريرية المبكرة. يكشف هذا البحث عن «مفتاح تشغيل» مخفي على SHP2 يفسر سبب فشل هذه الأدوية غالبًا ويشير إلى طرق جديدة للتغلب على الأورام المقاومة.
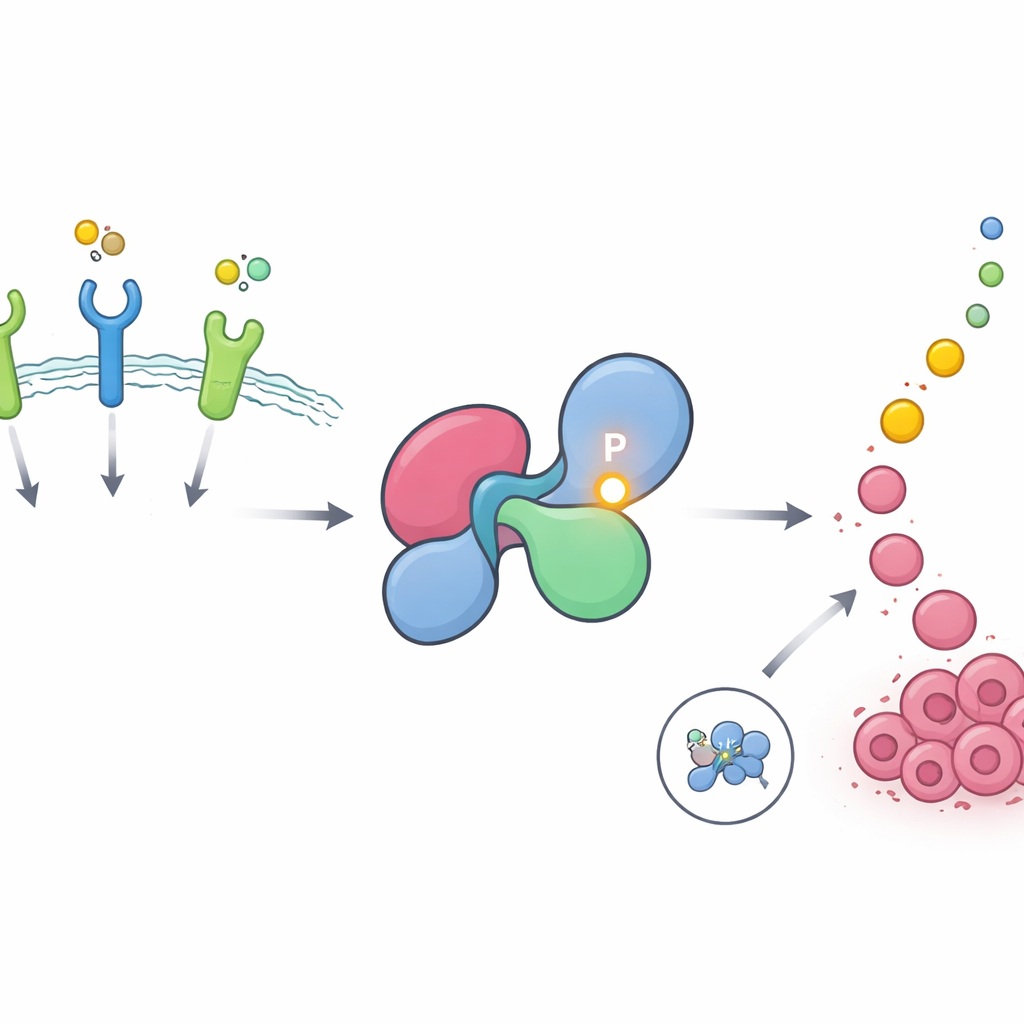
بؤرة ساخنة مخفية على مفتاح نمو حاسم
يساعد SHP2 في نقل الرسائل من مستقبلات على سطح الخلية، تُسمى مستقبلات التيروسين كيناز، إلى مسار RAS–MAPK، وهو محرك رئيسي لنمو وانقسام الخلايا. في الخلايا السليمة، يبقى SHP2 مُطفأً غالبًا، مطويًا في شكل مغلق يمنع موقعه النشط. يفتح لفترة وجيزة عند تنشيط المستقبلات ثم يغلق مجددًا. استخدم المؤلفون قواعد بيانات فسفوبروتينية واسعة للبحث عن مواقع بروتينية تُعدَّل بتكرار بإضافة مجموعات الفوسفات، وهي طريقة شائعة لتشغيل أو إيقاف الإشارات الخلوية. وجدوا أن موقعًا واحدًا على SHP2، يُسمى تيروسين 62، يُعدّ من أكثر المواقع فسفرةً بشكل كثيف ومتكرر في البروتيوم البشري بأكمله، ومُتَكَثِّف خصوصًا في الأورام المدفوعة بمستقبلات عوامل النمو مثل EGFR وFGFR.
سرطانات مختلفة، اعتماد مختلف على نفس المفتاح
من خلال تنقيبهم في مجموعات بيانات أورام المرضى، أظهر الباحثون أن الفسفرة عند موقع Y62 في SHP2 تزداد بقوة في عدة سرطانات مدفوعة بالمستقبلات، بما في ذلك أنواع معينة من سرطانات الرئة، وسرطان القناة الصفراوية، وأورام الرأس والعنق، وأورام الدماغ التي تحمل تغيرات في EGFR. من اللافت أنه في بعض سرطانات الرئة، كانت فسفرة SHP2 Y62 أعلى حتى من فسفرة المستقبل نفسه. في المقابل، أظهرت الأورام المدفوعة بطفرات KRAS، التي تنشط نفس مسار النمو في مستوى أدنى، مستويات منخفضة من فسفرة SHP2 Y62. يقترح هذا النمط أن السرطانات التي تعتمد على إشارات المستقبلات غالبًا ما تعزز فسفرة Y62 في SHP2 كجزء من شبكتها، بينما تلك التي لديها طفرات أسفل المسار لا تحتاج إلى هذا المفتاح بالذات.
كيف تسيطر عائلة كينازات أخرى على هذه البؤرة
من الوهلة الأولى، بدا من الطبيعي الاشتباه أن المستقبلات السطحية نفسها تعدل SHP2 مباشرة عند Y62. ومع ذلك، عندما قام الفريق بحظر مستقبلات مختلفة بأدوية مستهدفة، لم تتأثر فسفرة Y62 بشكل يذكر. بدلًا من ذلك، تتبعوا التعديل إلى مجموعة مختلفة من الإنزيمات تُعرف باسم كينازات عائلة SRC. باستخدام مزيج من مثبطات عائلة SRC العامة والانتقائية، وخلايا ذات حذف جيني لـ SRC وYES1 وFYN، وبروتينات مُنقَّاة في تجارب أنبوبية، أظهروا أن هذه الكينازات تضيف مجموعات الفوسفات مباشرة إلى SHP2 عند Y62، وكذلك عند موقعين معروفين أكثر في ذيل SHP2. وهذا يضع كينازات عائلة SRC كوسطاء حاسمين يجلسون بين المستقبلات النشطة وSHP2، مكوِّنين محور إشارة RTK–SRC–SHP2.
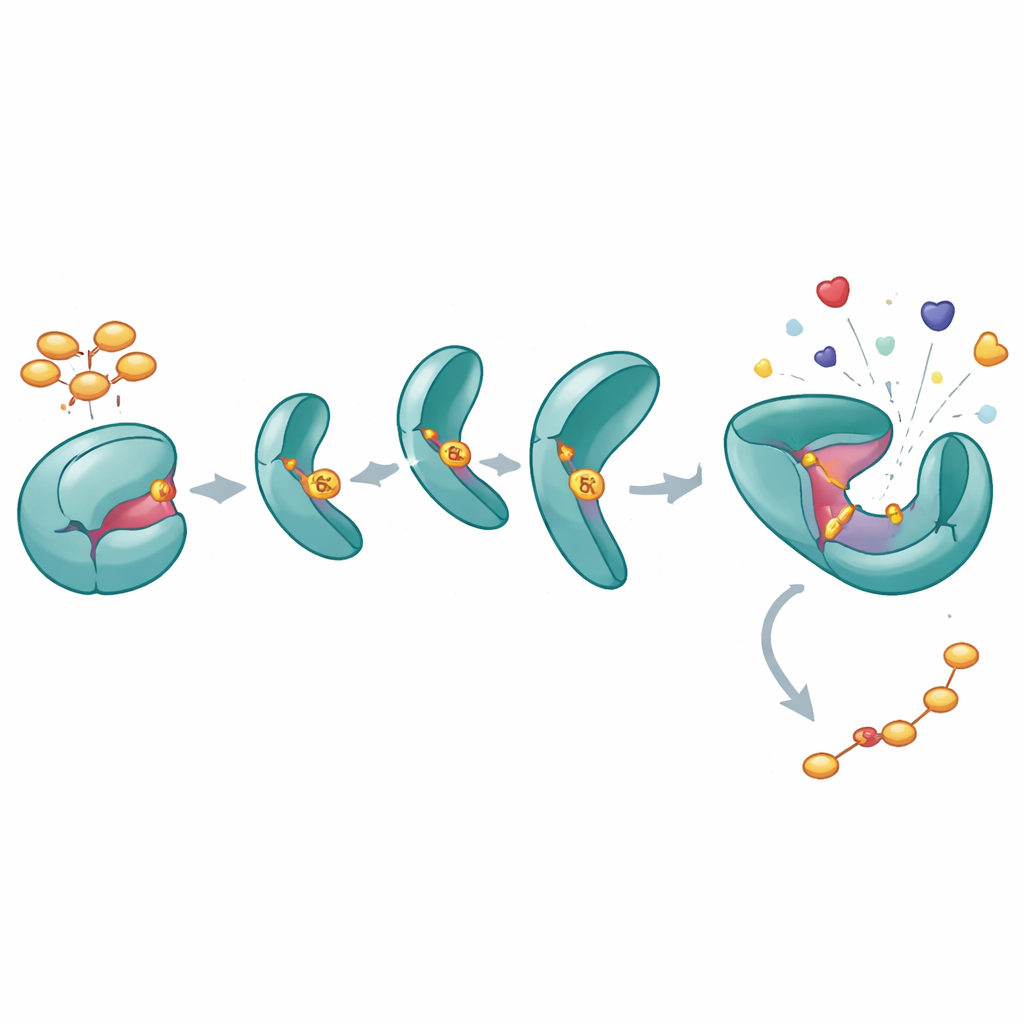
كيف يبقي فوسفات واحد SHP2 بازغًا على مصراعيه
لفهم ما تفعله فسفرة Y62 لـ SHP2، صنع المؤلفون نسخة «تحاكي الفسفرة» (Y62D) تتصرف كما لو أن Y62 مثبّت بشكل دائم بفسفرة. أظهرت الاختبارات الكيميائية الحيوية أن هذا المتغير يمتلك نشاطًا تحفيزيًا أعلى ولا يستجيب بالطريقة الاعتيادية للببتيدات المُنشِّطة التي عادةً «تفك قفل» SHP2 من حالته المغلقة. كشفت قياسات الاستقرار الحراري وتجارب تبادل الهيدروجين–الديتيريوم أن بروتين Y62D يتبنى طَوْرًا أكثر انفتاحًا ومرونة، خصوصًا عند الواجهة بين مجالاته التنظيمية والتحفيزية. بينما التُقطت بنية بلورية لـ Y62D في شكل مغلق، أشارت القياسات الديناميكية إلى أن هذا الطفرة في المحلول تقلب كثيرًا إلى حالة مفتوحة شبيهة بالنشطة، متجاوزة الكبح الذاتي الطبيعي.
لماذا تكافح أدوية SHP2 الحالية في العيادة
تعمل مثبطات SHP2 الالوستيرية الحالية عن طريق تثبيت الشكل المغلق غير النشط لـ SHP2، فعليًا «تلصق» مجالاته معًا. أظهر المؤلفون أن شكل Y62D من SHP2 أقل حساسية لهذه الأدوية في اختبارات البروتين المنقّى. في خطوط خلايا سرطانية استُبدل فيها جين SHP2 الطبيعي بمتغير Y62D، ظل إشارات النمو عبر مسار MAPK مرتفعة حتى عندما عولجت الخلايا بثلاثة مثبطات مختلفة لـ SHP2 قيد التجارب السريرية. كما حافظت هذه الخلايا على فسفرة GAB1، وهو موصل إشارة رئيسي يعتمد على SHP2، مما يبرز أن SHP2 بقي وظيفيًا نشطًا رغم العلاج الدوائي. تدعم هذه البيانات نموذجًا تفيد فيه كينازات عائلة SRC بفَسفرة SHP2 عند Y62، مما يجبره على حالة مفتوحة ونشطة لا تستطيع الأدوية الحالية قفلها بفعالية.
ماذا يعني هذا لعلاجات السرطان غدًا
تحدد الدراسة فسفرة SHP2 عند Y62 كمفتاح شائع وذو صلة دوائية يُحاكي تأثير الطفرات المنشِّطة الدائمة، ولكن دون تغييرات في الحمض النووي. يساعد هذا في تفسير سبب مقاومة السرطانات المدفوعة بمستقبلات عوامل النمو لمثبطات SHP2 الحالية بشكل جوهري، حتى لو بدا جين SHP2 طبيعيًا في اختبارات التسلسل. قد تكون قياسات فسفرة Y62 علامة حيوية للتنبؤ بالأورام التي من غير المرجح أن تستجيب لتلك الأدوية. والأهم من ذلك، تبرز النتائج SHP2 المفوسفَر عند Y62 كهدف بنيوي مميز وتقترح أن الاستراتيجيات الفعالة قد تتطلب إما حجب كينازات عائلة SRC في الأعلى، أو تصميم مثبطات SHP2 جديدة تتعرف مباشرة على شكله المفتوح والمفوسفَر وتغلقه.
الاستشهاد: Karunaraj, P., Scheele, R., Wells, M.L. et al. A hotspot phosphorylation site on SHP2 drives oncoprotein activation and drug resistance. Nat Commun 17, 3383 (2026). https://doi.org/10.1038/s41467-026-70060-8
الكلمات المفتاحية: SHP2, الفسفرة, كينازات SRC, إشارة MAPK, مقاومة الدواء