Clear Sky Science · ja
SHP2のホットスポットリン酸化部位がオンコタンパクの活性化と薬剤耐性を引き起こす
将来のがん治療にとってなぜ重要か
多くの現代的ながん治療薬は、腫瘍細胞内で過剰に働いている増殖シグナルを遮断することを目的としています。有望な標的のひとつがSHP2と呼ばれるタンパク質で、細胞表面のシグナルを細胞内の増殖エンジンにつなぐ重要なスイッチです。しかし、SHP2を抑えるように設計された薬剤は、初期の臨床試験でほとんど効果を示していません。本論文はSHP2上に隠れた「オン・スイッチ」を明らかにし、なぜこれらの薬がしばしば失敗するのかを説明するとともに、耐性腫瘍を打ち破るための新たな方策を示唆します。
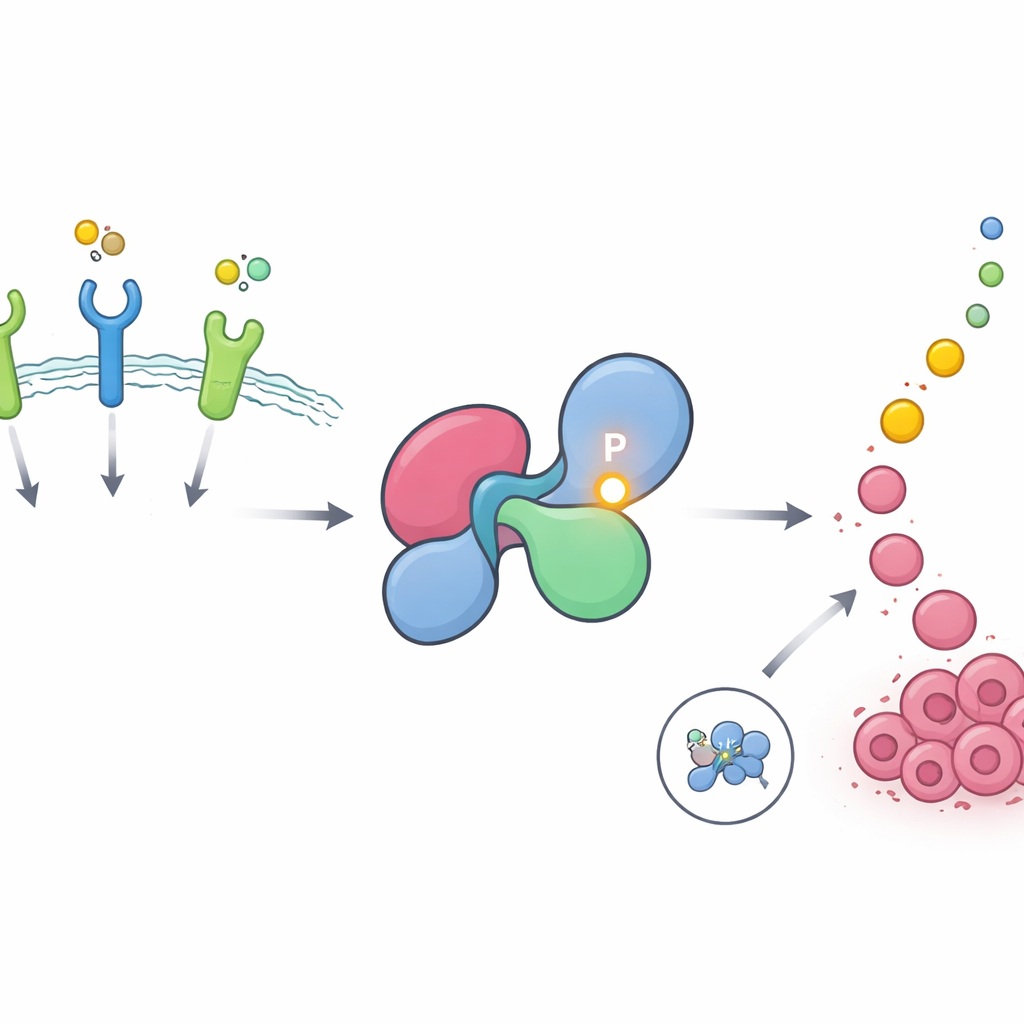
重要な成長スイッチ上の隠れたホットスポット
SHP2は受容体チロシンキナーゼと呼ばれる細胞表面の受容体からの信号をRAS–MAPK経路へ中継し、細胞の増殖・分裂を駆動する主要な役割を担います。健常な細胞ではSHP2は大部分がオフの状態で、自己の活性部位を遮る折りたたまれた閉じた構造をとっています。受容体が刺激されると一時的に開き、その後再び閉じます。著者らは大規模なホスホプロテオミクスデータベースを用いて、リン酸基の付加によって頻繁に修飾されるタンパク質部位を検索しました。その結果、SHP2のある特定の位置、チロシン62(Y62)がヒトプロテオーム全体でも特に強く、繰り返しリン酸化される部位のひとつであり、EGFRやFGFRのような増殖因子受容体に駆動される腫瘍で特に濃縮されていることがわかりました。
がんによって異なる同じスイッチへの依存性
患者腫瘍データセットを掘り下げることで、研究者らはSHP2のY62部位のリン酸化が、特定の肺がんや胆道がん、頭頸部腫瘍、EGFR変化を伴う脳腫瘍など、いくつかの受容体駆動型がんで強く増加していることを示しました。注目すべきは、ある種の肺がんではSHP2のY62リン酸化が受容体自体のリン酸化よりも高かったことです。一方、同じ増殖経路を下流で活性化する変異型KRASに駆動される腫瘍では、SHP2 Y62のリン酸化が低下していました。このパターンは、受容体シグナルに依存するがんが配線の一部としてしばしばSHP2 Y62を増強する一方で、経路の下流に変異があるがんはこの特定のスイッチを必要としないことを示唆しています。
別のキナーゼ群がこのホットスポットを制御する仕組み
一見すると、表面受容体自体が直接SHP2のY62を修飾していると考えるのが自然でした。しかし、研究チームが各種受容体を標的薬で遮断したところ、Y62のリン酸化はほとんど変化しませんでした。代わりに、彼らは修飾の原因をSRCファミリーキナーゼという別の酵素群にたどり着きました。広範かつ選択的なSRCファミリー阻害剤の使用、SRC、YES1、FYNを欠く遺伝子ノックアウト細胞、精製タンパク質を用いた試験管内反応の組み合わせにより、これらのキナーゼがSHP2のY62およびSHP2尾部の二つの既知の部位に直接リン酸基を付加することが示されました。これにより、活性化された受容体とSHP2の間にRTK–SRC–SHP2という重要な中間軸が存在することが位置づけられます。
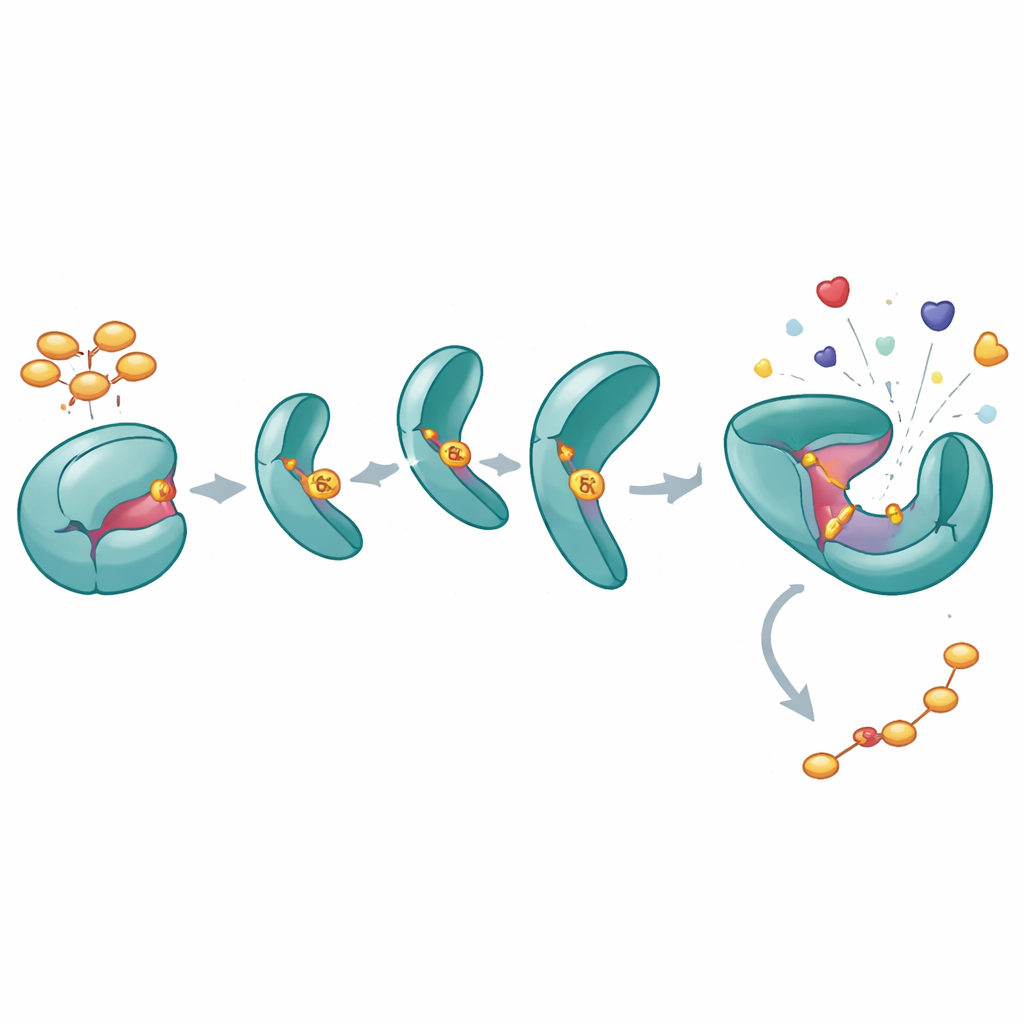
一つのリン酸化がSHP2を大きく開かせる仕組み
Y62リン酸化がSHP2に何をもたらすかを理解するために、著者らはY62が常にリン酸化されたかのように振る舞う「リン酸類似型」変異体(Y62D)を設計しました。生化学的アッセイでは、この変異体がより高い触媒活性を持ち、通常であればSHP2を閉じた状態から「解除」する活性化ペプチドに正常に応答しないことが示されました。熱安定性測定と水素-重水素置換実験は、Y62Dタンパク質が特に調節ドメインと触媒ドメインの界面で、より開いた柔軟なコンフォメーションをより多くサンプリングしていることを示しました。Y62Dの結晶構造は閉じた形を捕らえていましたが、動的測定は溶液中ではこの変異体が頻繁に開いた活性類似の状態に反転し、通常の自己抑制を回避していることを示しています。
なぜ現行のSHP2薬は臨床で苦戦するのか
現在のアロステリックSHP2阻害剤は、SHP2の閉じた不活性形状を安定化させ、実質的にそのドメインを「接着」することで作用します。著者らは精製タンパク質アッセイで、Y62D型のSHP2がこれらの薬剤に対して感受性が低いことを示しました。正規のSHP2遺伝子がY62Dに置き換えられたがん細胞株では、三種類の臨床段階にあるSHP2阻害剤で処理してもMAPK経路を介した増殖シグナルは高いままでした。これらの細胞はまた、SHP2に依存する重要なシグナルアダプターであるGAB1のリン酸化も維持しており、薬剤処理にもかかわらずSHP2が機能的に活性のままであることを強調しています。総じて、データはSRCファミリーキナーゼがSHP2をY62でリン酸化し、既存の薬剤が効率的に抑えられない開いた活性型構造へと駆り立てるというモデルを支持します。
明日のがん治療にとっての示唆
本研究はSHP2 Y62のリン酸化を、DNA変化を伴わないにもかかわらず恒常的な活性化変異の効果を模倣する一般的で薬剤に関連するスイッチとして同定しています。これは増殖因子受容体に駆動されるがんが、SHP2遺伝子に明らかな変化が見られなくとも現行のSHP2阻害剤に本質的に耐性を示す理由を説明する助けになります。Y62のリン酸化を測定することは、これらの薬に反応しにくい腫瘍を予測するバイオマーカーとして有用である可能性があります。さらに重要なのは、Y62がリン酸化されたSHP2を別個の構造的標的とみなし、効果的な戦略としては上流でSRCファミリーキナーゼを遮断するか、あるいは開いたリン酸化型のSHP2を直接認識して抑える新しい阻害剤を設計する必要があることを示唆している点です。
引用: Karunaraj, P., Scheele, R., Wells, M.L. et al. A hotspot phosphorylation site on SHP2 drives oncoprotein activation and drug resistance. Nat Commun 17, 3383 (2026). https://doi.org/10.1038/s41467-026-70060-8
キーワード: SHP2, リン酸化, SRCキナーゼ, MAPKシグナル伝達, 薬剤耐性