Clear Sky Science · nl
Een hotspot-fosforyleringsplaats op SHP2 drijft oncoproteïne-activatie en medicijnresistentie
Waarom dit ertoe doet voor toekomstige kankerbehandelingen
Veel moderne kankertherapieën zijn gericht op het uitschakelen van overactieve groeisignalen binnen tumorcellen. Een veelbelovend doelwit is het eiwit SHP2, een belangrijke schakel die signalen aan het celoppervlak verbindt met het interne groeimotor van de cel. Toch hebben middelen die SHP2 zouden moeten uitschakelen in vroege klinische onderzoeken vrijwel geen voordeel laten zien. Dit artikel ontdekt een verborgen "aan-schakelaar" op SHP2 die helpt verklaren waarom deze middelen vaak falen en wijst op nieuwe manieren om resistente tumoren te slim af te zijn.
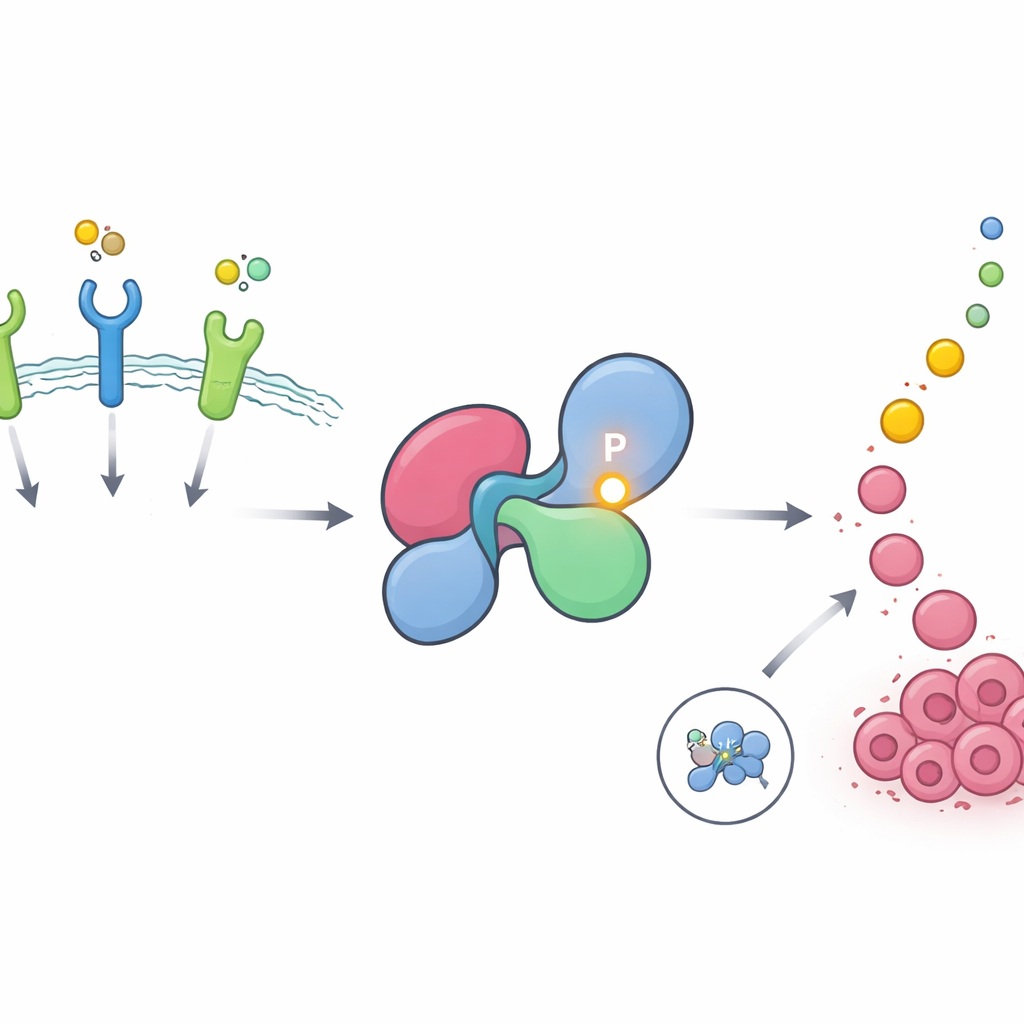
Een verborgen hotspot op een cruciale groeischakelaar
SHP2 helpt boodschappen doorgeven van receptoren op het celoppervlak, receptor-tyrosinekinasen genoemd, naar de RAS–MAPK-route, een belangrijke aanjager van celgroei en celdeling. In gezonde cellen is SHP2 grotendeels uitgeschakeld, opgevouwen in een gesloten vorm die zijn actieve centrum blokkeert. Het klapt kort open wanneer receptoren geactiveerd worden en sluit daarna weer. De auteurs gebruikten uitgebreide fosfoproteomische databases om naar eiwitplaatsen te zoeken die vaak worden gemodificeerd door de toevoeging van fosfaatgroepen, een gebruikelijke manier waarop cellen signalen aan- en uitzetten. Ze vonden dat één specifieke positie op SHP2, tyrosine 62 genoemd, tot de meest intensief en herhaaldelijk gefosforyleerde plekken in het gehele menselijke proteoom behoort en bijzonder verrijkt is in tumoren die worden aangedreven door groeifactorreceptoren zoals EGFR en FGFR.
Verschillende kankers, verschillende afhankelijkheid van dezelfde schakelaar
Door patiëntentumordatasets te doorzoeken lieten de onderzoekers zien dat fosforylering op SHP2’s Y62-positie sterk verhoogd is in meerdere receptor-gedreven kankers, waaronder bepaalde longkankers, galbuiskankers, hoofd-hals-tumoren en hersentumoren met EGFR-afwijkingen. Opvallend genoeg was in sommige longkankers de fosforylering van SHP2 Y62 zelfs hoger dan die op de receptor zelf. Ter vergelijking toonden tumoren die werden aangedreven door mutant KRAS, dat dezelfde groeiroute stroomafwaarts activeert, verlaagde niveaus van SHP2 Y62-fosforylering. Dit patroon suggereert dat kankers die vertrouwen op receptursignalen vaak SHP2 Y62 verhogen als onderdeel van hun bedrading, terwijl tumoren met mutaties verderop in de route deze specifieke schakelaar niet nodig hebben.
Hoe een andere kinasefamilie deze hotspot controleert
Op het eerste gezicht lag het voor de hand te veronderstellen dat de oppervlaktereceptoren zelf SHP2 op Y62 direct modificeren. Toen het team echter verschillende receptoren blokkeerde met gerichte geneesmiddelen, veranderde Y62-fosforylering nauwelijks. In plaats daarvan tracede ze de modificatie naar een andere groep enzymen, bekend als SRC-familiekinasen. Met een combinatie van brede en selectieve SRC-familie-remmers, genetische knockoutcellen zonder SRC, YES1 en FYN, en gezuiverde eiwitten in reageerbuisexperimenten, toonden ze aan dat deze kinasen rechtstreeks fosfaatgroepen aan SHP2 op Y62 toevoegen, en ook op twee beter bekende plaatsen in de staart van SHP2. Dit plaatst SRC-familiekinasen als cruciale tussenpersonen tussen geactiveerde receptoren en SHP2, en creëert een RTK–SRC–SHP2-signaleringsas.
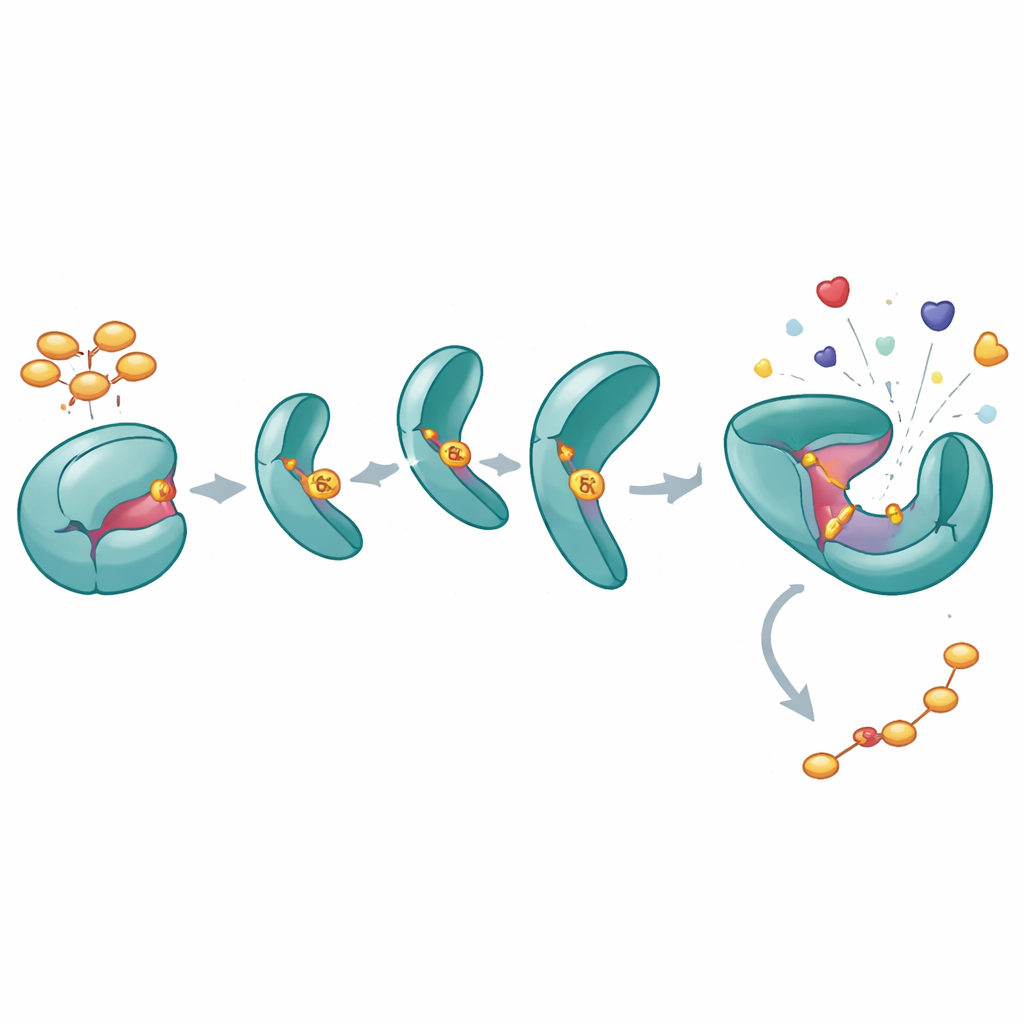
Hoe één fosfaat SHP2 wijd openhoudt
Om te begrijpen wat Y62-fosforylering met SHP2 doet, maakten de auteurs een "fosfomimetische" variant (Y62D) die zich gedraagt alsof Y62 permanent gefosforyleerd is. Biochemische assays toonden aan dat deze variant een hogere katalytische activiteit heeft en niet normaal reageert op activerende peptiden die SHP2 gewoonlijk uit zijn gesloten staat zouden "ontgrendelen". Metingen van thermische stabiliteit en waterstof–deuteriumuitwisselingsexperimenten toonden aan dat het Y62D-eiwit meer open, flexibele conformaties bemonstert, vooral bij het interface tussen zijn regulatorische en catalytische domeinen. Hoewel een kristalstructuur van Y62D het in een gesloten vorm vastlegde, wezen de dynamische metingen uit dat deze mutant in oplossing vaak omslaat naar een open, actief-achtige staat en zo de normale auto-inhibitie omzeilt.
Waarom huidige SHP2-medicijnen moeite hebben in de kliniek
Huidige allosterische SHP2-remmers werken door de gesloten, inactieve vorm van SHP2 te stabiliseren, en als het ware de domeinen aan elkaar te lijmen. De auteurs toonden aan dat de Y62D-vorm van SHP2 in gezuiverde eiwitassays minder gevoelig is voor deze geneesmiddelen. In kankercellijnen waarin het normale SHP2-gen werd vervangen door Y62D, bleef de groeisignalering via de MAPK-route hoog, zelfs wanneer de cellen werden behandeld met drie verschillende SHP2-remmers in klinische fase. Deze cellen behielden ook de fosforylering van GAB1, een belangrijk signaleringsadapter die afhankelijk is van SHP2, wat aangeeft dat SHP2 functioneel actief bleef ondanks medicijnbehandeling. Samen ondersteunen de gegevens een model waarin SRC-familiekinasen SHP2 op Y62 fosforyleren en het dwingen in een open, actieve conformatie die bestaande middelen niet efficiënt kunnen vastzetten.
Wat dit betekent voor de therapieën van morgen
De studie identificeert SHP2 Y62-fosforylering als een veelvoorkomende, medicijnrelevante schakelaar die het effect van permanente activerende mutaties nabootst, maar zonder veranderingen in het DNA. Dit helpt verklaren waarom tumoren die door groeifactorreceptoren worden aangestuurd intrinsiek resistent kunnen zijn tegen huidige SHP2-remmers, zelfs wanneer hun SHP2-gen normaal lijkt in sequentietests. Het meten van Y62-fosforylering kan dienen als biomarker om te voorspellen welke tumoren waarschijnlijk niet op deze middelen zullen reageren. Belangrijker nog benadrukt het werk SHP2 gefosforyleerd op Y62 als een onderscheidend structureel doelwit en suggereert dat effectieve strategieën mogelijk vereisen dat men ofwel SRC-familiekinasen stroomopwaarts blokkeert, of nieuwe SHP2-remmers ontwerpt die direct de open, gefosforyleerde vorm herkennen en uitschakelen.
Bronvermelding: Karunaraj, P., Scheele, R., Wells, M.L. et al. A hotspot phosphorylation site on SHP2 drives oncoprotein activation and drug resistance. Nat Commun 17, 3383 (2026). https://doi.org/10.1038/s41467-026-70060-8
Trefwoorden: SHP2, fosforylering, SRC-kinasen, MAPK-signaleringsweg, medicijnresistentie