Clear Sky Science · ru
Горячая точка фосфорилирования на SHP2 вызывает активацию онкопротеина и лекарственную устойчивость
Почему это важно для будущих противораковых терапий
Многие современные противораковые препараты нацелены на отключение чрезмерно активных сигналов роста внутри опухолевых клеток. Перспективной мишенью оказался белок SHP2 — ключевой переключатель, который связывает сигналы на поверхности клетки с её внутренним механизом роста. Тем не менее препараты, разработанные для блокирования SHP2, в ранних клинических испытаниях почти не показали пользы. В этой работе раскрыта скрытая «включающая» точка на SHP2, которая помогает объяснить, почему эти лекарства часто не срабатывают, и указывает новые пути обхода устойчивых опухолей.
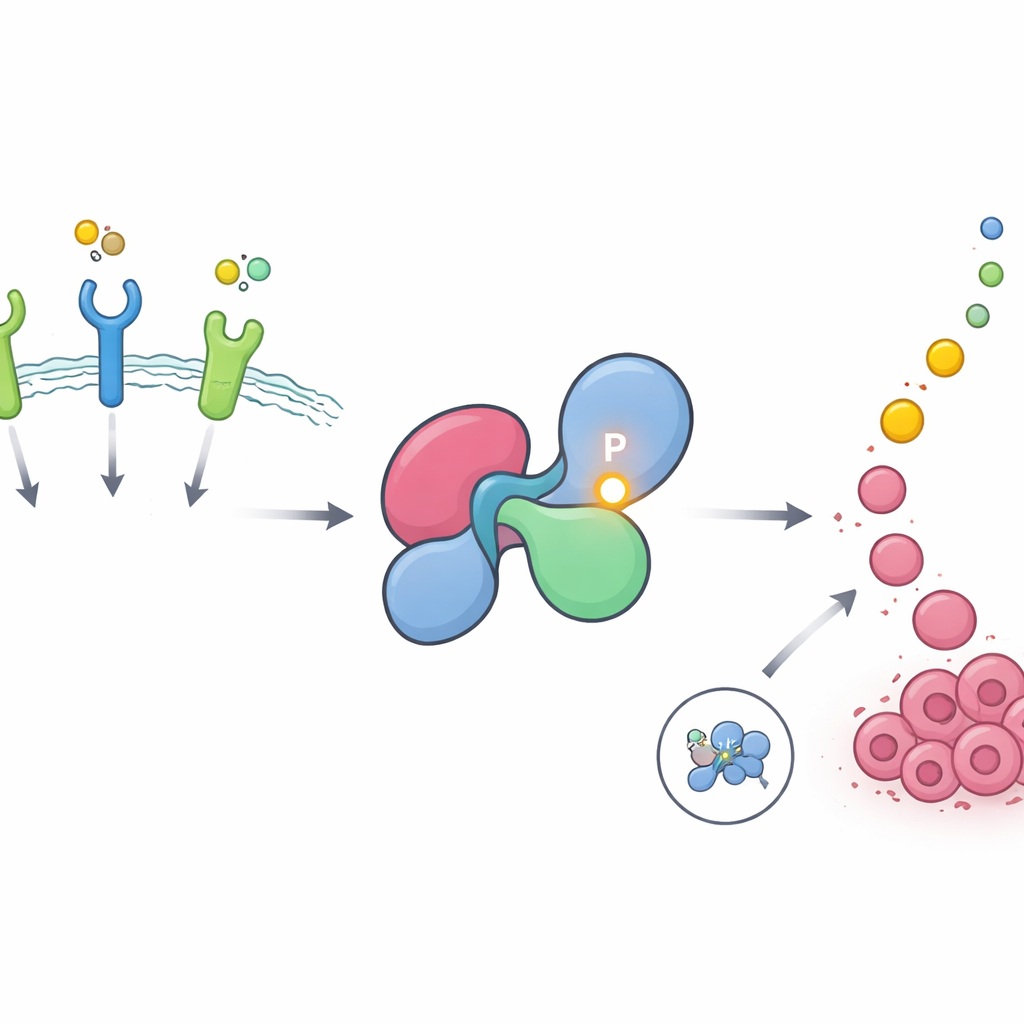
Скрытая «горячая» точка в важном переключателе роста
SHP2 передаёт сигналы от рецепторов на поверхности клетки, называемых рецепторными тирозинкиназами, к пути RAS–MAPK — основному драйверу роста и деления клеток. В здоровых клетках SHP2 в основном находится в выключенном состоянии, свернутый в закрытую конформацию, блокирующую его активный сайт. Он кратковременно открывается при стимуляции рецепторов, а затем снова закрывается. Авторы использовали крупные фосфопротеомные базы данных, чтобы искать сайты белков, которые часто модифицируются добавлением фосфатных групп — распространенным способом включения и выключения сигналов в клетке. Они обнаружили, что одна конкретная позиция в SHP2, тирозин 62, является одной из наиболее интенсивно и повторно фосфорилируемых в человеческом протеоме и особенно обогащена в опухолях, вызванных факторами роста, такими как EGFR и FGFR.
Разные раки — разная зависимость от одного и того же переключателя
Анализируя наборы данных опухолей пациентов, исследователи показали, что фосфорилирование Y62 в SHP2 значительно увеличено в нескольких опухолях, управляемых рецепторами, включая некоторые рак лёгкого, опухоли желчных протоков, головы и шеи, а также опухоли мозга с изменениями в EGFR. Поразительно, что в некоторых случаях рака лёгкого фосфорилирование SHP2 Y62 было даже выше, чем фосфорилирование самого рецептора. Напротив, опухоли, управляемые мутантным KRAS, который активирует тот же путь ниже по каскаду, демонстрировали сниженные уровни фосфорилирования Y62 SHP2. Такая картина указывает, что опухоли, зависящие от сигналов рецепторов, часто усиливают фосфорилирование Y62 в составе своей сигнальной сети, тогда как при мутациях ниже по пути этот конкретный переключатель не требуется.
Как другая семья киназ регулирует эту «горячую» точку
На первый взгляд было естественно предположить, что сами поверхностные рецепторы напрямую модифицируют SHP2 в позиции Y62. Однако при блокировании различных рецепторов таргетными препаратами фосфорилирование Y62 почти не изменялось. Вместо этого модификацию проследили до другой группы ферментов — киназ семейства SRC. С помощью комбинации широких и селективных ингибиторов семейства SRC, клеток с генетическим нокаутом SRC, YES1 и FYN, а также очищенных белков в пробирочных реакциях они показали, что эти киназы непосредственно добавляют фосфатные группы на SHP2 в положении Y62, а также на двух более известных сайтах в хвостовой части SHP2. Это ставит киназы семейства SRC в роль важных посредников между активированными рецепторами и SHP2, формируя ось RTK–SRC–SHP2.
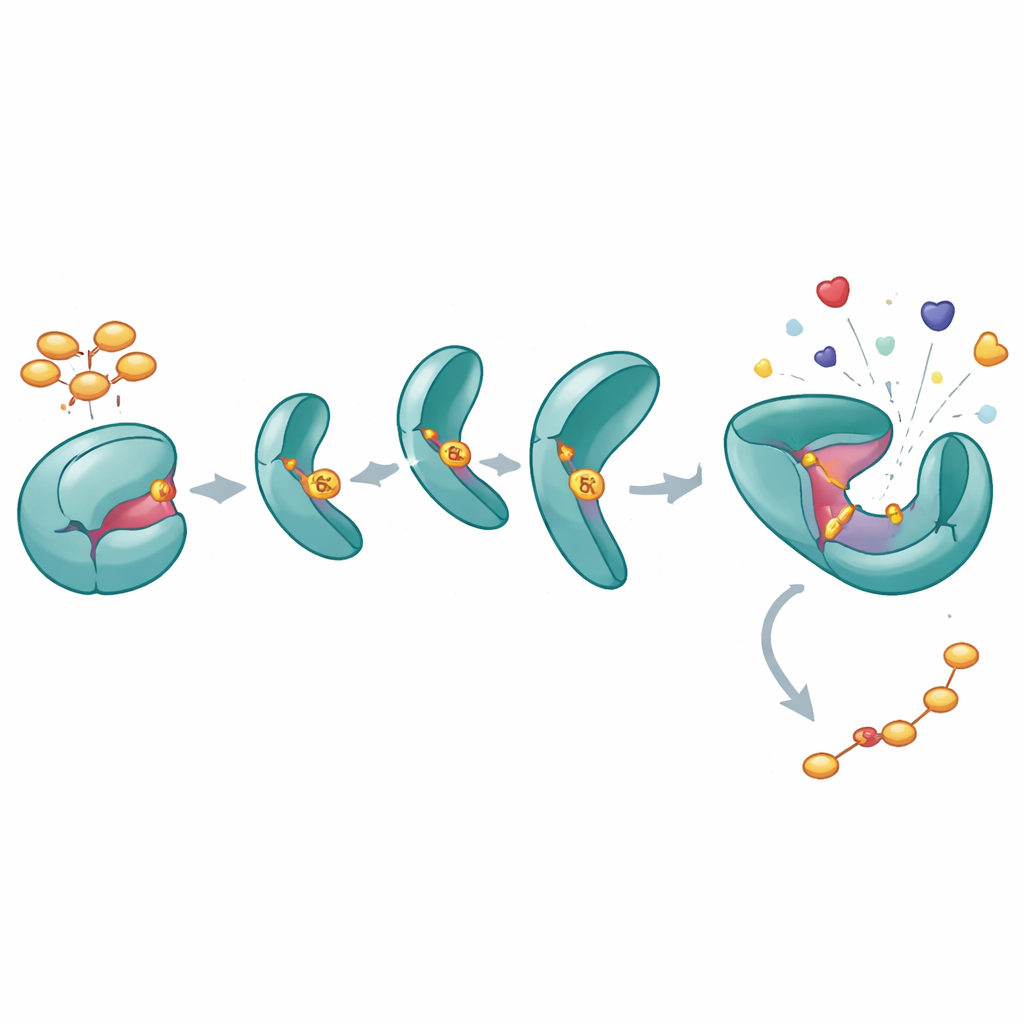
Как одна фосфатная группа держит SHP2 широко открытым
Чтобы понять, что делает фосфорилирование Y62 с SHP2, авторы создали «фосфомиметическую» версию (Y62D), которая ведёт себя так, как будто Y62 постоянно фосфорилирован. Биохимические анализы показали, что этот вариант обладает повышенной каталитической активностью и не реагирует нормально на активирующие пептиды, которые обычно «отпирают» SHP2 из закрытого состояния. Измерения термостабильности и эксперименты по обмену водорода на дейтерий показали, что белок Y62D чаще принимает открытые, гибкие конформации, особенно на интерфейсе между регуляторными и каталитическими доменами. Хотя кристаллическая структура Y62D была зафиксирована в закрытой форме, динамические измерения указывали, что в растворе этот мутант часто переключается в открытое, активоподобное состояние, обходя нормальную автоингибицию.
Почему текущие препараты против SHP2 с трудом работают в клинике
Современные аллостерические ингибиторы SHP2 действуют, стабилизируя закрытую, неактивную форму SHP2, фактически «склеивая» его домены. Авторы показали, что форма SHP2 Y62D менее чувствительна к таким препаратам в очистке белка. В клеточных линиях рака, где нормальный ген SHP2 был заменён на Y62D, сигнальная передача через путь MAPK оставалась высокой даже при обработке тремя различными клиническими ингибиторами SHP2. В этих клетках также поддерживалось фосфорилирование GAB1, ключевого адаптера сигнала, зависящего от SHP2, что подчёркивает функциональную активность SHP2 несмотря на лечение. В совокупности данные поддерживают модель, в которой киназы семейства SRC фосфорилируют SHP2 по Y62, переводя его в открытую, активную конформацию, которую существующие препараты не способны эффективно зафиксировать.
Что это значит для будущих противораковых терапий
Исследование идентифицирует фосфорилирование Y62 SHP2 как распространённый, клинически значимый переключатель, который имитирует эффект постоянных активирующих мутаций, но без изменений в ДНК. Это помогает объяснить, почему опухоли, управляемые факторами роста, могут быть изначально резистентны к текущим ингибиторам SHP2, даже если ген SHP2 в секвенировании выглядит нормальным. Измерение фосфорилирования Y62 может служить биомаркером для прогнозирования того, какие опухоли вряд ли ответят на эти препараты. Более важно, работа подчёркивает SHP2, фосфорилированный по Y62, как отдельную структурную мишень и предлагает, что эффективные стратегии могут требовать либо блокирования киназ семейства SRC вверх по цепочке, либо разработки новых ингибиторов SHP2, которые прямо распознают и блокируют его открытую, фосфорилированную форму.
Цитирование: Karunaraj, P., Scheele, R., Wells, M.L. et al. A hotspot phosphorylation site on SHP2 drives oncoprotein activation and drug resistance. Nat Commun 17, 3383 (2026). https://doi.org/10.1038/s41467-026-70060-8
Ключевые слова: SHP2, фосфорилирование, киназы SRC, MAPK‑сигнальная передача, лекарственная устойчивость