Clear Sky Science · tr
Beta-arrestin 1 aracılı Src aktivasyon mekanizması: Src SH3 domaini üzerinden kriyo-elektron mikroskopisiyle aydınlatıldı
Hücreler Sinyalleri Nasıl Eyleme Dönüştürür
Hücrelerimiz yüzeylerindeki reseptörler aracılığıyla hormonları ve nörotransmitterleri sürekli algılar ve ne zaman yanıt vereceklerine, ne zaman duracaklarına ve hangi iç yolları etkinleştireceklerine karar vermelidir. Bu çalışma, karar verme sürecinin iki kilit oyuncusu olan beta-arrestin 1 ve enzim Src’u ele alarak, bir proteinin diğerinin "açma" düğmesini nasıl fiziksel olarak çevirdiğini atomik ayrıntıda gösteriyor. Bu koreografiyi anlamak, günlük sinyal iletiminin nasıl işlediğini açıklamaya yardımcı olur ve Src’un sıklıkla aşırı aktif olduğu kanser gibi hastalıklarda nelerin yolunda gitmediğine ışık tutabilir.
Trafik Polisi Aynı Zamanda Bir Anahtar
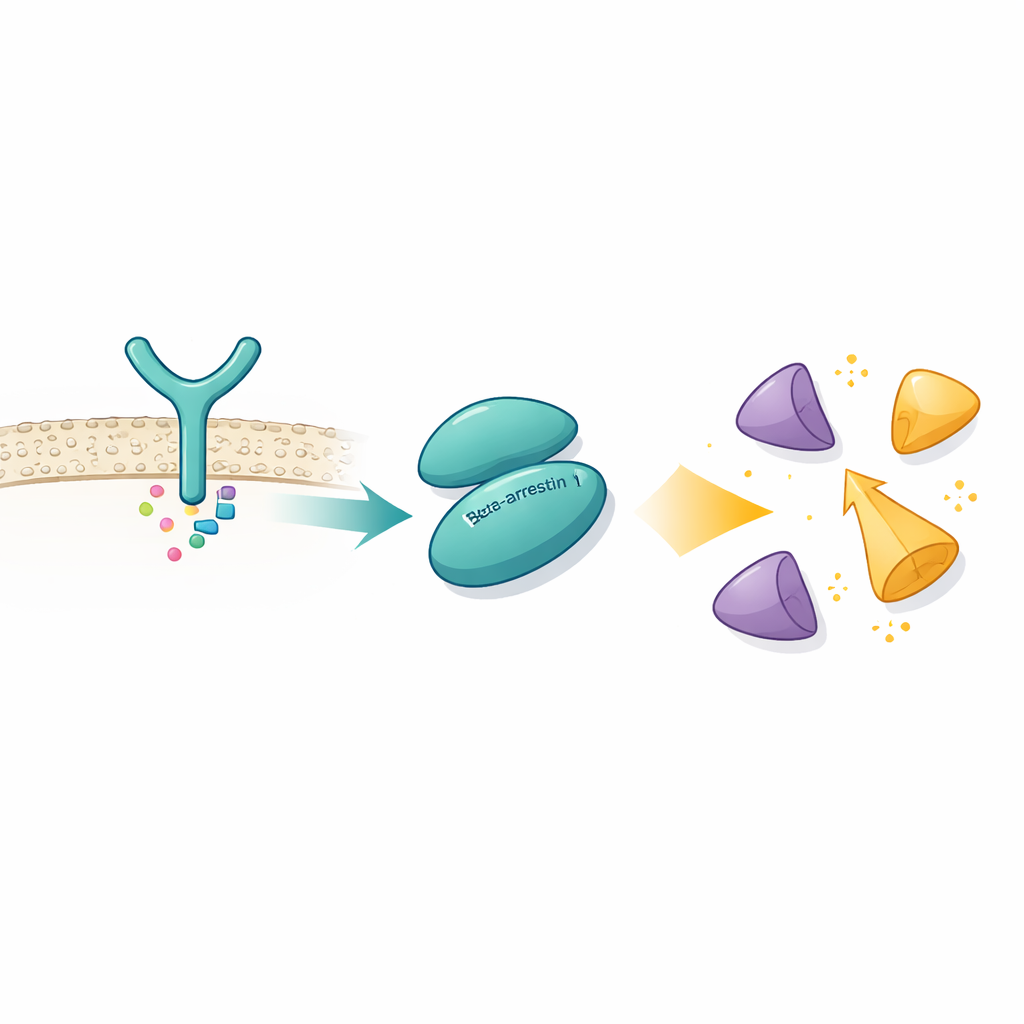
G proteinine bağlı reseptörler (GPCR'ler), görmeden kalp atış hızına kadar pek çok süreci kontrol eden geniş bir hücre yüzeyi algılayıcı ailesidir. Beta-arrestinler uzun süre esasen hücresel trafik polisi olarak düşünülmüştür: etkinleşmiş GPCR'lere tutunur, ilave sinyallemeyi kapatır ve reseptörleri hücre içine yönlendirirler. Ancak son on yılda, beta-arrestinlerin kendi başlarına sinyal taşıyıcıları olarak ortaya çıktığı, GPCR'leri birçok aşağı akış enzime bağlayabildikleri görüldü. En önemli ortaklardan biri, hücre büyümesini, hareketini ve hayatta kalmasını yönlendirebilen bir tirozin kinaz olan Src'tur. Yine de beta-arrestin 1 (β-arrestin 1 veya βarr1) ile Src arasındaki konuşmanın ve aslında Src’u nasıl açtığının kesin biçimi, etkileşimin kısa ömürlü ve görece zayıf olması nedeniyle belirsiz kaldı.
Tek Bir Protein Üzerinde İki Tokalaşma
Yakın-atomik çözünürlükte protein topluluklarını görselleştirebilen kriyo-elektron mikroskopisi kullanarak, yazarlar βarr1'in Src’un SH3 domainine bağlı halini yakaladılar. βarr1'in tek bir temas noktasına dayanmadığını keşfettiler. Bunun yerine, yapısının farklı bölümlerinde iki ayrı tokalaşma sunuyor. Bir site βarr1'in N-terminal bölgesinde yer alır ve SH3 domainleriyle sıkça etkileşen, prolin açısından zengin kısa bir diziyi içerir. İkinci site, orta bir sırt (central crest) olarak adlandırılan bölgede bulunur ve aynı SH3 yüzeyine farklı bir amino asit karışımıyla tutunur. Biyofiziksel ölçümler ve hidrojen-deuteryum değişim deneyleri, SH3 varlığında βarr1'in her iki alanının da korunduğunu doğruluyor; bu durum, bu çift temasların gerçekçi koşullar altında, mühendislik çapraz-bağları olmadan da ortaya çıktığını gösterir.
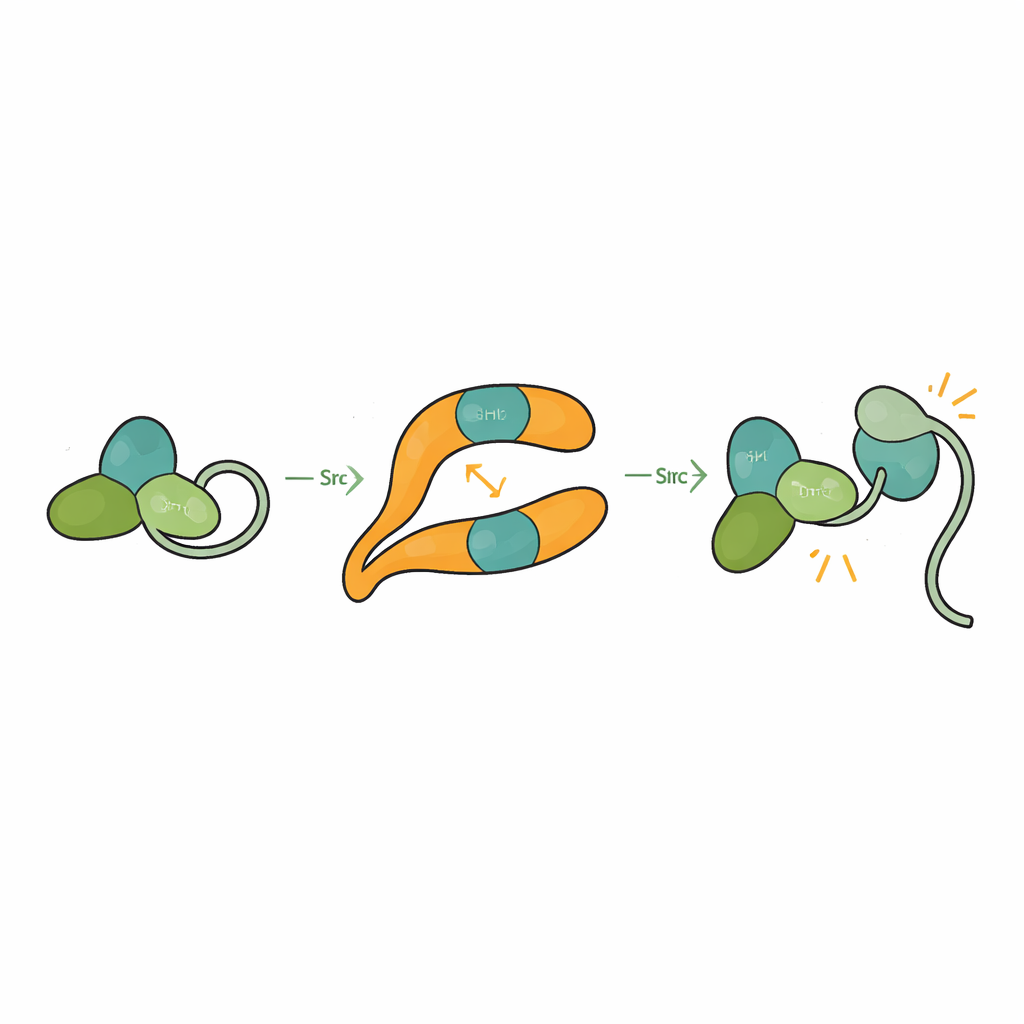
Oto-İnhibit olmuş Bir Enzimi Açığa Çıkarmak
Src normalde SH3, SH2 ve katalitik domainlerinin birbirine paketlendiği ve bir kuyruk segmentinin yapıyı kapalı tutmak için bağlandığı kendi kendini kilitlemiş, yani oto-inhibe halde tutulur. Bu, hücreye zarar verebilecek tesadüfi aktivasyonu önler. Araştırmacılar βarr1'in üç domainli Src formuna bağlı yapısını çözdüklerinde, SH3'ün βarr1 üzerindeki orta sırt sitesine bağlandığında Src'u kapalı tutmaya yardımcı olan iç bağlayıcıyı artık kavrayamadığını gördüler. Katalitik domain daha hareketli hale geliyor ve bütünsel şekil gevşiyor; bu da aktif bir duruma uygun. Biyokimyasal testler, βarr1'in kuyruk bölgesi fosforile olmadığında, yani SH3'ün geçici olarak açığa çıkabileceği daha esnek bir formda Src'e tercihli olarak bağlandığını gösteriyor. SH3 βarr1'e bağlandığında, Src'u sessiz tutan kelepçe aralanır ve Src kendi kendini fosforile ederek tam olarak aktive olur.
Sinyal Yönlendirme İçin Esnek Bir Merkez
Çalışma ayrıca βarr1'in kendisinin katı olmadığını ortaya koyuyor. SH3 bağlandığında, βarr1 içindeki kilit zincirler ve döngüler özellikle orta sırt çevresinde birkaç angström kayar. Bu ince hareketler, βarr1'in GPCR'leri kavrama sıkılığını değiştirebilir. Floresan etiketli βarr1 kullanılarak yapılan deneyler, fazla SH3'ün βarr1'in kendisinin bir bölümünü reseptör çekirdeğine sokma biçimini zayıflatabileceğini gösteriyor; bu konfigürasyonun G protein sinyalini kapatmak için önemli olduğu düşünülüyor. Canlı hücrelerde Src'un aşırı eksprese edilmesi, beta-adrenerjik reseptör aktive edildikten sonra cAMP adlı ikinci habercinin yükselmesinin daha uzun sürmesini sağlayarak duyarsızlaşmanın geciktiğini gösteriyor. Birlikte, bu bulgular yüksek yerel Src düzeylerinin GPCR–βarr1 birleşimlerini tam "kapalı" moddan uzaklaştırabileceğini ve G proteinlerinin daha uzun süre sinyal vermesine izin verebileceğini öne sürüyor.
Sağlık ve Tedavi Açısından Neden Önemli
βarr1'in Src’u iki noktadan nasıl yakalayıp oto-inhibit pozisyonundan çektiğini doğrudan görselleştirerek, bu çalışma βarr1'i sadece pasif bir iskelet değil, aktif bir düzenleyici olarak konumlandırıyor. Tek bir adaptör proteinin, görece zayıf birden çok teması birleştirerek güçlü bir enzimi sağlam ve ayarlanabilir biçimde kontrol edebildiğini gösteriyor. Src'un kanserlerde sıkça fazla eksprese edildiği veya yanlış düzenlendiği düşünüldüğünde, bu aktivasyon yolunu anlamak βarr1–Src iletişimini seçici şekilde bozacak stratejiler geliştirmeye ilham verebilir; bu yaklaşımlar diğer Src işlevlerini kapatmak zorunda kalmayabilir. Daha geniş anlamda, burada ortaya konan çift noktalı tanıma, beta-arrestinlerin birçok ortağıyla nasıl etkileştiğine dair genel bir şablon olabilir ve GPCR sinyalini yararlı yollara yönlendirirken zararlı olanları engelleyecek ilaç tasarımları için yeni açılar sunabilir.
Atıf: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
Anahtar kelimeler: beta-arrestin, Src kinaz, GPCR sinyal iletimi, kriyo-elektron mikroskopisi, hücre sinyalleşmesi