Clear Sky Science · it
Meccanismo dell'attivazione di Src mediata da beta-arrestina 1 tramite il dominio SH3 di Src rivelato dalla crio-microscopia elettronica
Come le cellule trasformano i segnali in azione
Le nostre cellule rilevano costantemente ormoni e neurotrasmettitori tramite recettori sulla loro superficie e devono decidere quando rispondere, quando fermarsi e quali vie interne attivare. Questo studio esamina due protagonisti chiave in quel processo decisionale—beta-arrestina 1 e l’enzima Src—per rivelare, a livello atomico, come una proteina fisicamente accenda l’interruttore di un’altra. Comprendere questa coreografia aiuta a spiegare come funziona la segnalazione quotidiana e può fare luce su ciò che va storto in malattie come il cancro, dove Src è spesso iperattivo.
Un vigile del traffico che è anche un interruttore
I recettori accoppiati a proteine G (GPCR) sono una grande famiglia di sensori di superficie cellulare che controllano processi che vanno dalla visione al battito cardiaco. Le beta-arrestine sono state a lungo considerate principalmente come vigili del traffico cellulari: si attaccano ai GPCR attivati, bloccano la segnalazione ulteriore e guidano i recettori all’interno della cellula. Nell’ultimo decennio, tuttavia, le beta-arrestine sono emerse come vettori di segnale a pieno titolo, in grado di collegare i GPCR a numerosi enzimi a valle. Uno dei partner più importanti è Src, una tirosina chinasi che può promuovere crescita, movimento e sopravvivenza cellulare. Eppure il modo preciso in cui beta-arrestina 1 (β-arrestina 1, o βarr1) dialoga con Src—e in realtà lo attiva—è rimasto un mistero perché l’interazione è fugace e relativamente debole.
Due strette di mano su una stessa proteina
Usando la crio-microscopia elettronica, che può visualizzare assemblee proteiche a risoluzione quasi atomica, gli autori hanno catturato βarr1 legata al dominio SH3 di Src, un piccolo modulo di aggancio presente in molte proteine di segnalazione. Hanno scoperto che βarr1 non si affida a un unico punto di contatto. Invece, offre due strette di mano separate su parti diverse della sua struttura. Un sito si trova nella regione N-terminale di βarr1 e contiene un breve tratto ricco di prolina—amminoacidi che spesso interagiscono con i domini SH3. Il secondo sito, in una regione chiamata cresta centrale, utilizza un diverso mix di amminoacidi per atterrare sulla stessa superficie aromatica del dominio SH3. Misure biofisiche e esperimenti di scambio idrogeno-deuterio confermano che entrambe le aree di βarr1 diventano protette quando SH3 è presente, anche senza legami incrociati ingegnerizzati, mostrando che questi doppi contatti avvengono in condizioni realistiche.
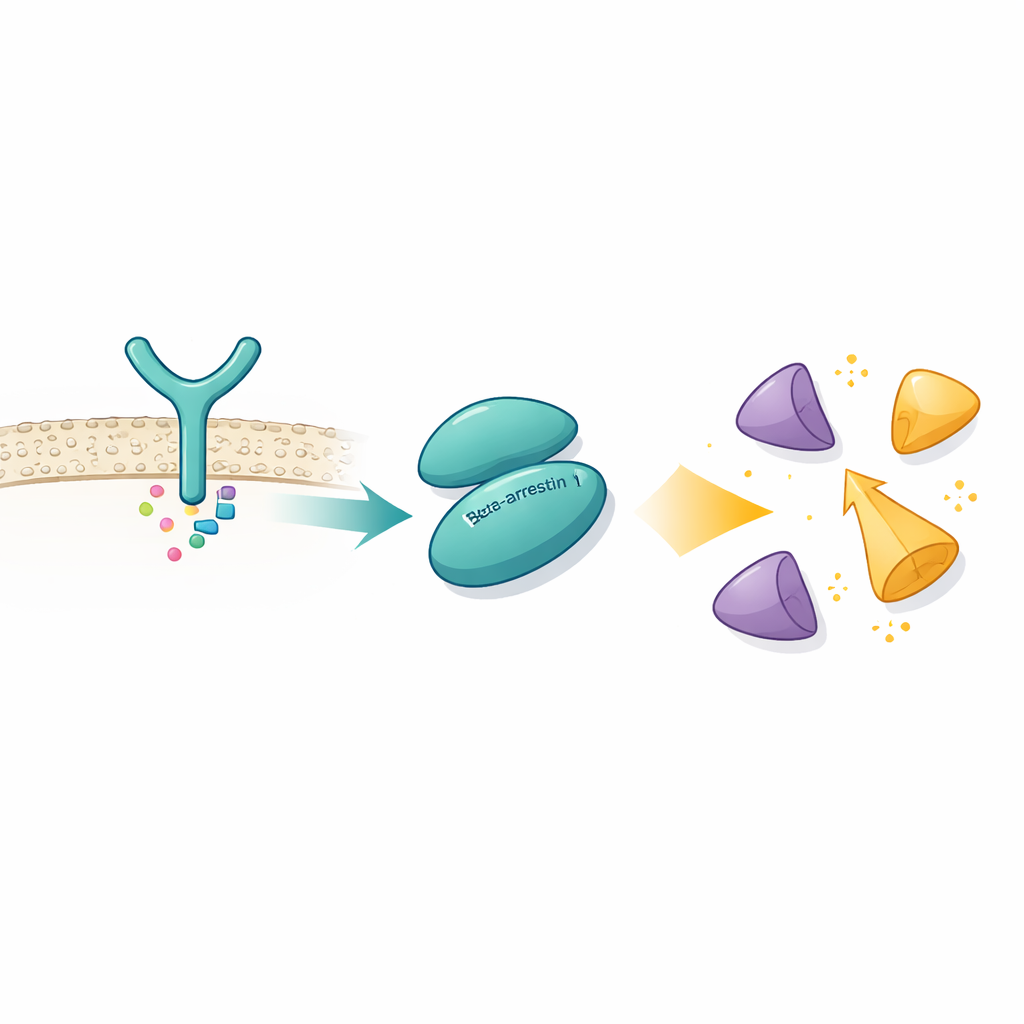
Sbloccare un enzima autoinibito
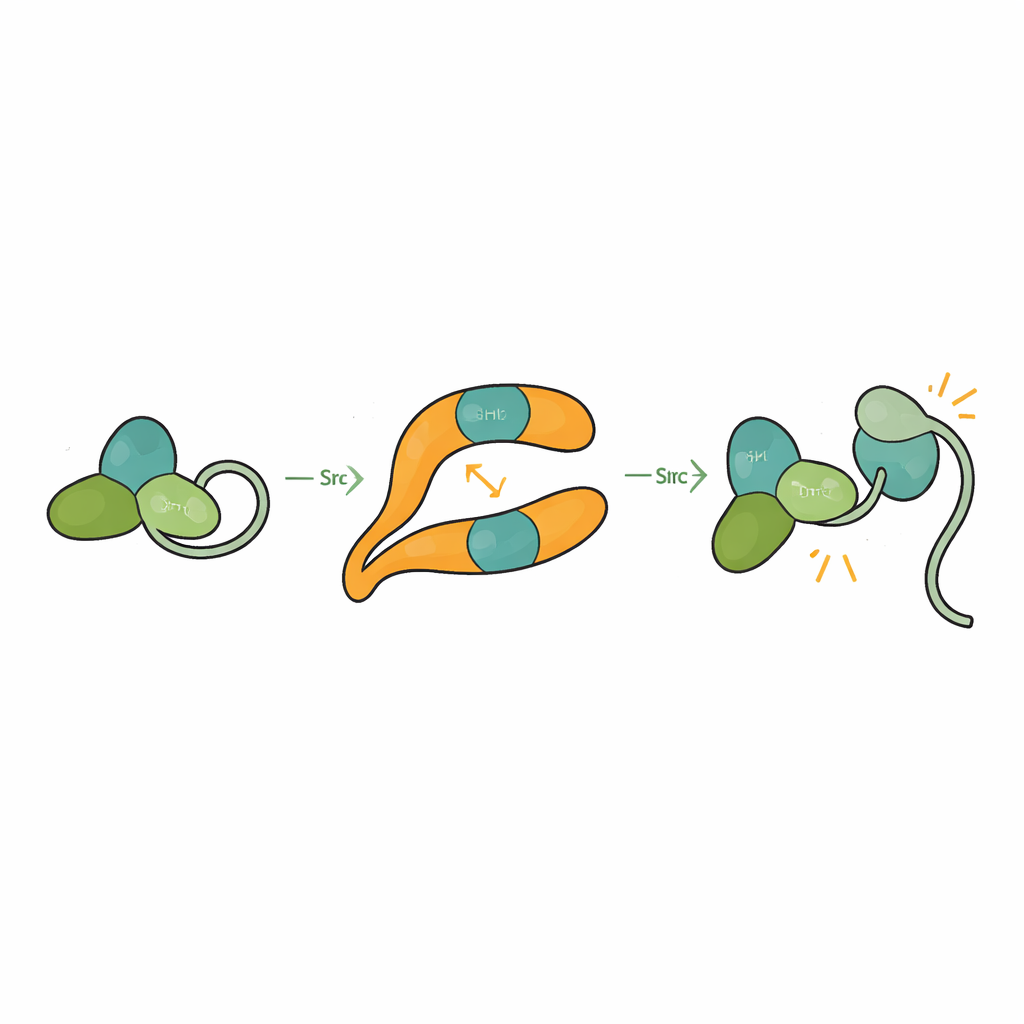
Src è normalmente mantenuto in una forma auto-bloccata, o autoinibita, nella quale i domini SH3, SH2 e catalitico si impaccano tra loro e un segmento della coda tiene la struttura chiusa. Questo previene attivazioni accidentali che potrebbero danneggiare la cellula. Risolvendo la struttura di βarr1 legata a una forma di Src con tre domini, i ricercatori hanno osservato che quando SH3 si aggancia al sito della cresta centrale su βarr1, non può più afferrare il linker interno che aiuta a mantenere Src chiuso. Il dominio catalitico diventa più mobile e la forma complessiva si allenta, coerente con uno stato attivo. Saggi biochimici mostrano che βarr1 si lega preferenzialmente a Src quando la sua coda non è fosforilata, una forma più flessibile che espone momentaneamente SH3. Una volta che SH3 si ancora a βarr1, la morsa che mantiene Src silente viene forzata ad aprirsi, permettendo a Src di autofosforilarsi e attivarsi completamente.
Un hub flessibile per instradare i segnali
Lo studio rivela anche che βarr1 stessa non è rigida. Quando SH3 si lega, fili e anse chiave all’interno di βarr1 si spostano di diversi angstrom, soprattutto intorno alla cresta centrale. Questi movimenti sottili possono modificare quanto saldamente βarr1 afferra i GPCR. Esperimenti con βarr1 marcata fluorescentemente mostrano che un eccesso di SH3 può indebolire il modo in cui βarr1 inserisce parte di sé nel nucleo del recettore, una configurazione ritenuta importante per spegnere la segnalazione tramite le proteine G. Nelle cellule vive, la sovraespressione di Src prolunga l’aumento di un secondo messaggero chiamato cAMP dopo l’attivazione di un recettore beta-adrenergico, indicando una desensibilizzazione ritardata. Nel complesso, questi risultati suggeriscono che alti livelli locali di Src possono spostare gli assemblaggi GPCR–βarr1 lontano dalla modalità completamente "off" e permettere alle proteine G di continuare a segnalare più a lungo.
Perché è importante per salute e terapia
Visualizzando direttamente come βarr1 afferra Src in due punti e lo estrae dalla sua posa auto-inibita, questo lavoro stabilisce βarr1 come un regolatore attivo, non solo uno scaffold passivo. Mostra che una singola proteina adattatrice può combinare molteplici contatti relativamente deboli in un controllo robusto e regolabile su un potente enzima. Poiché Src è frequentemente sovraespresso o mal regolato nei tumori, comprendere questa via di attivazione potrebbe ispirare strategie che interrompono selettivamente la comunicazione βarr1–Src senza spegnere altre funzioni di Src. Più in generale, il riconoscimento a doppio sito qui svelato può essere un modello generale per come le beta-arrestine ingaggiano molti dei loro partner, offrendo nuovi spunti per progettare farmaci che orientino la segnalazione GPCR verso vie benefiche evitando quelle nocive.
Citazione: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
Parole chiave: beta-arrestina, chinasi Src, segnalazione GPCR, crio-microscopia elettronica, segnalazione cellulare