Clear Sky Science · pt
Mecanismo de ativação de Src mediada por beta-arrestina 1 através do domínio SH3 de Src revelado por criomicroscopia eletrônica
Como as Células Transformam Sinais em Ação
Nossas células detectam continuamente hormônios e neurotransmissores por meio de receptores em sua superfície e precisam decidir quando responder, quando parar e quais vias internas ativar. Este estudo examina dois protagonistas-chave nesse processo de tomada de decisão — beta-arrestina 1 e a enzima Src — para revelar, em detalhe atômico, como uma proteína fisicamente “aciona” a outra. Compreender essa coreografia ajuda a explicar como a sinalização cotidiana funciona e pode esclarecer o que dá errado em doenças como o câncer, nas quais o Src frequentemente está hiperativo.
Um Agente de Trânsito que Também é um Interruptor
Receptores acoplados a proteína G (GPCRs) constituem uma enorme família de sensores na superfície celular que controlam processos desde a visão até a frequência cardíaca. Durante muito tempo as beta-arrestinas foram vistas principalmente como agentes de trânsito celular: elas se ligam aos GPCRs ativados, interrompem a sinalização adicional e guiam os receptores para o interior da célula. Na última década, porém, as beta-arrestinas emergiram como transportadoras de sinal por direito próprio, capazes de conectar GPCRs a muitas enzimas downstream. Um dos parceiros mais importantes é o Src, uma tirosina quinase que pode impulsionar crescimento, movimento e sobrevivência celular. Ainda assim, a maneira precisa como a beta-arrestina 1 (β-arrestina 1, ou βarr1) conversa com o Src — e de fato o ativa — permaneceu um mistério porque a interação é fugaz e relativamente fraca.
Dois Apertos de Mão em Uma Só Proteína
Usando criomicroscopia eletrônica, que pode visualizar complexos proteicos em resolução quase atômica, os autores capturaram βarr1 ligada ao domínio SH3 de Src, um pequeno módulo de ancoragem encontrado em muitas proteínas de sinalização. Descobriram que βarr1 não depende de um único ponto de contato. Em vez disso, oferece dois apertos de mão separados em diferentes partes de sua estrutura. Um sítio está na região N-terminal de βarr1 e contém um trecho curto rico em prolina — aminoácidos que frequentemente interagem com domínios SH3. O segundo sítio, numa região chamada crista central, usa uma mistura diferente de aminoácidos para acomodar-se na mesma superfície aromática do domínio SH3. Medidas biofísicas e experimentos de troca hidrogênio–deutério confirmam que ambas as áreas de βarr1 ficam protegidas na presença do SH3, mesmo sem ligações cruzadas artificiais, mostrando que esses contatos duplos ocorrem em condições realistas.
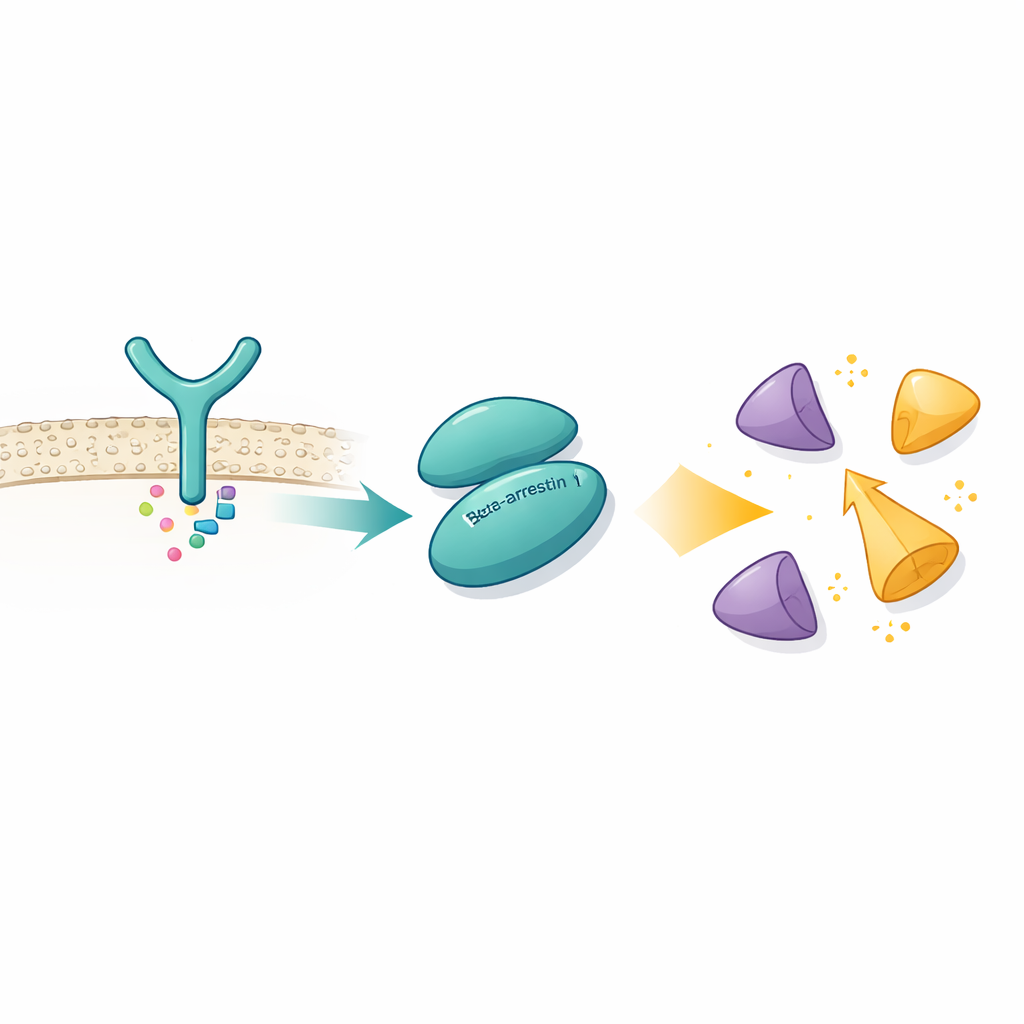
Destravando uma Enzima Autoinibida
Normalmente o Src é mantido em uma conformação auto-bloqueada, ou autoinibida, na qual seus domínios SH3, SH2 e catalítico se empacotam entre si e um segmento de cauda ancora a estrutura fechada. Isso evita ativações acidentais que poderiam danificar a célula. Ao resolver a estrutura de βarr1 ligada a uma forma de Src contendo três domínios, os pesquisadores observaram que, quando o SH3 se engaja com o sítio da crista central em βarr1, ele não consegue mais prender o ligante interno que ajuda a manter o Src fechado. O domínio catalítico torna-se mais móvel e a conformação geral relaxa, consistente com um estado ativo. Ensaios bioquímicos mostram que βarr1 prefere ligar-se ao Src quando sua cauda não está fosforilada, uma forma mais flexível que expõe momentaneamente o SH3. Uma vez que o SH3 se prende a βarr1, a trava que mantém o Src silencioso é forçada a abrir, permitindo que o Src se autofilofosforile e ative-se completamente.
Um Hub Flexível para Roteamento de Sinais
O estudo também revela que a própria βarr1 não é rígida. Quando o SH3 se liga, fitas e loops-chave dentro de βarr1 deslocam-se por vários angstroms, especialmente ao redor da crista central. Esses movimentos sutis podem alterar o grau de aperto com que βarr1 segura os GPCRs. Experimentos com βarr1 rotulada por fluorescência mostram que um excesso de SH3 pode enfraquecer a forma como βarr1 insere parte de si no núcleo do receptor, uma configuração considerada importante para desligar a sinalização por proteínas G. Em células vivas, a superexpressão de Src prolonga o aumento de um segundo mensageiro chamado AMPc após ativação de um receptor beta-adrenérgico, indicando dessensibilização retardada. Em conjunto, essas descobertas sugerem que níveis locais elevados de Src podem deslocar os complexos GPCR–βarr1 para longe do modo totalmente “desligado” e permitir que as proteínas G mantenham a sinalização por mais tempo.
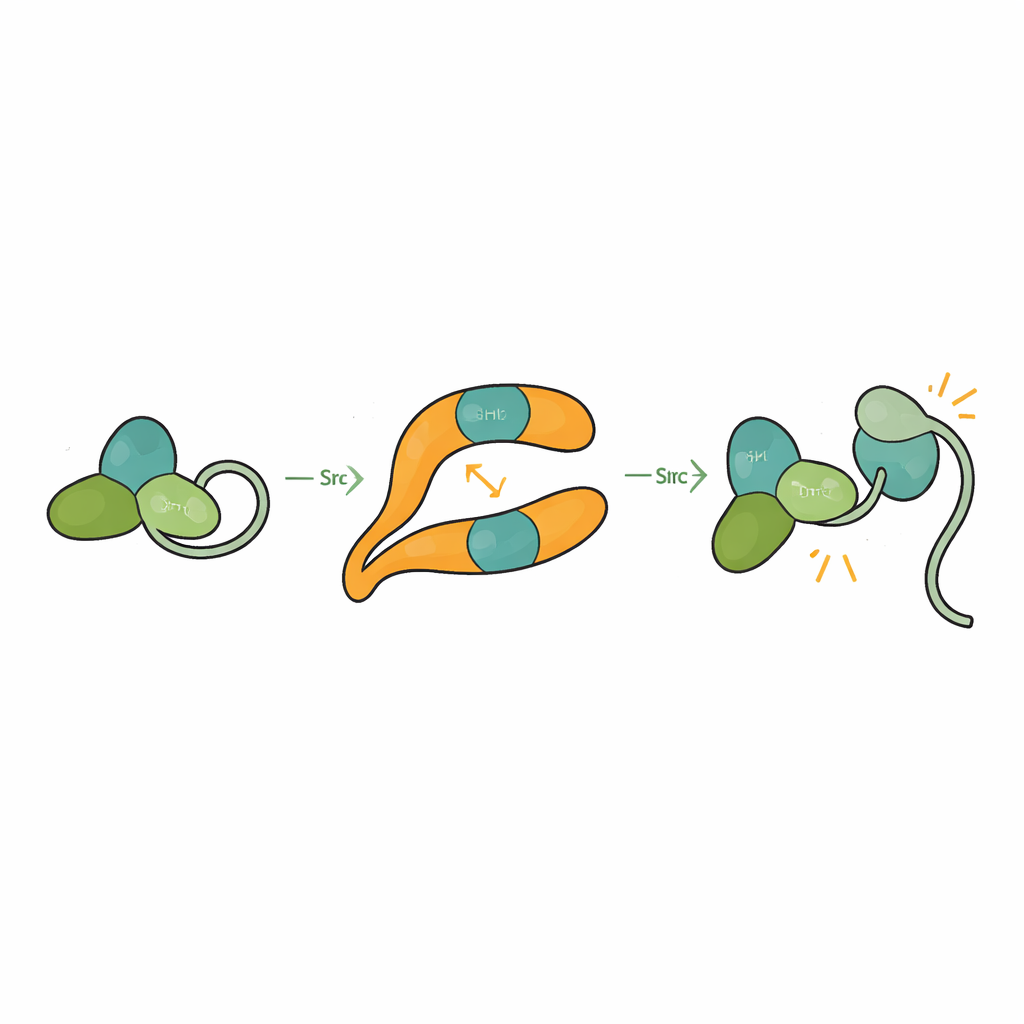
Por Que Isso Importa para Saúde e Terapia
Ao visualizar diretamente como βarr1 agarra o Src em dois sítios e o arranca de sua pose auto-inibida, este trabalho estabelece βarr1 como um regulador ativo, não apenas um andaime passivo. Mostra que um único adaptador pode combinar múltiplos contatos relativamente fracos em um controle robusto e ajustável sobre uma enzima potente. Como o Src é frequentemente superexpresso ou desregulado em cânceres, entender essa via de ativação pode inspirar estratégias que interrompam seletivamente a comunicação βarr1–Src sem desligar outras funções do Src. Mais amplamente, o reconhecimento de dupla interação descoberto aqui pode ser um modelo geral para como as beta-arrestinas envolvem muitos de seus parceiros, oferecendo ângulos novos para projetar drogas que enviesem a sinalização GPCR para vias benéficas enquanto evitam as nocivas.
Citação: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
Palavras-chave: beta-arrestina, quinase Src, sinalização GPCR, criomicroscopia eletrônica, sinalização celular