Clear Sky Science · ar
آلية تفعيل Src بوساطة بيتا-أريستين 1 عبر مجال SH3 في Src مكشوفة بواسطة الميكروسكوب الإلكتروني بالتبريد
كيف تحول الخلايا الإشارات إلى فعل
تستشعر خلايانا باستمرار الهرمونات والناقلات العصبية عبر مستقبلات على سطحها ويجب أن تقرر متى تستجيب ومتى تتوقف وأي المسارات الداخلية تُشغّل. تبحث هذه الدراسة في لاعبين أساسيين في عملية اتخاذ القرار هذه—بيتا-أريستين 1 والإنزيم Src—لتكشف، بتفصيل ذري، كيف يقوم بروتين واحد فعليًا بتشغيل مفتاح "التشغيل" لدى بروتين آخر. يساعد فهم هذا التآزر على تفسير كيفية عمل الإشارات اليومية وقد يسلط الضوء على ما يختل في الأمراض مثل السرطان، حيث يكون Src غالبًا مفرط النشاط.
شرطي مرور هو أيضًا مفتاح تشغيل
مستقبلات مقترنة بالبروتين G (GPCRs) هي عائلة ضخمة من الحساسات على سطح الخلية تتحكم في عمليات تتراوح من الرؤية إلى معدل ضربات القلب. لطالما كانت البيتاأريستينات تُعتبر إلى حد بعيد شرطي مرور خلوي: ترتبط بالمستقبلات المنشَّطة، وتوقف المزيد من الإشارات، وتوجه المستقبلات إلى داخل الخلية. ومع ذلك، خلال العقد الماضي برزت البيتا-أريستينات كحاملات للإشارة بحد ذاتها، قادرة على ربط مستقبلات GPCR بالعديد من الإنزيمات اللاحقة. أحد الشركاء الأهم هو Src، كيناز تيروسين يمكنه دفع نمو الخلايا وحركتها وبقائها. لكن الطريقة الدقيقة التي يتواصل بها بيتا-أريستين 1 (β-arrestin 1، أو βarr1) مع Src—وكيف يقوم فعلاً بتفعيله—ظلت لغزًا لأن التفاعل عابر وضعيف نسبيًا.
مصافحتان على بروتين واحد
باستخدام الميكروسكوب الإلكتروني بالتبريد، الذي يمكنه تصور تجمعات البروتين بدقة قريبة من الذرية، التقط الباحثون βarr1 مرتبطًا بمجال SH3 في Src، وهو وحدة رسو صغيرة توجد في العديد من بروتينات الإشارة. اكتشفوا أن βarr1 لا يعتمد على نقطة تلامس واحدة. بل يقدم مصافحتين منفصلتين على أجزاء مختلفة من بنيته. يجلس أحد الموقعين في المنطقة الطرفية الأمينية لβarr1 ويحتوي على مقطع قصير غني بالبرولين—حوائط أمينية غالبًا ما تتفاعل مع مجالات SH3. الموقع الثاني، في منطقة تُسمى الحد المركزي، يستخدم مزيجًا مختلفًا من الحموض الأمينية لالتحام على نفس السطح العطري لمجال SH3. تؤكد القياسات الفيزيائية الحيوية وتجارب تبادل الهيدروجين-الديتيريوم أن كلا المنطقتين في βarr1 تصبحان محمية عند وجود SH3، حتى من دون روابط مصممة، ما يدل على أن هذه الاتصالات المزدوجة تحدث في ظروف واقعية.
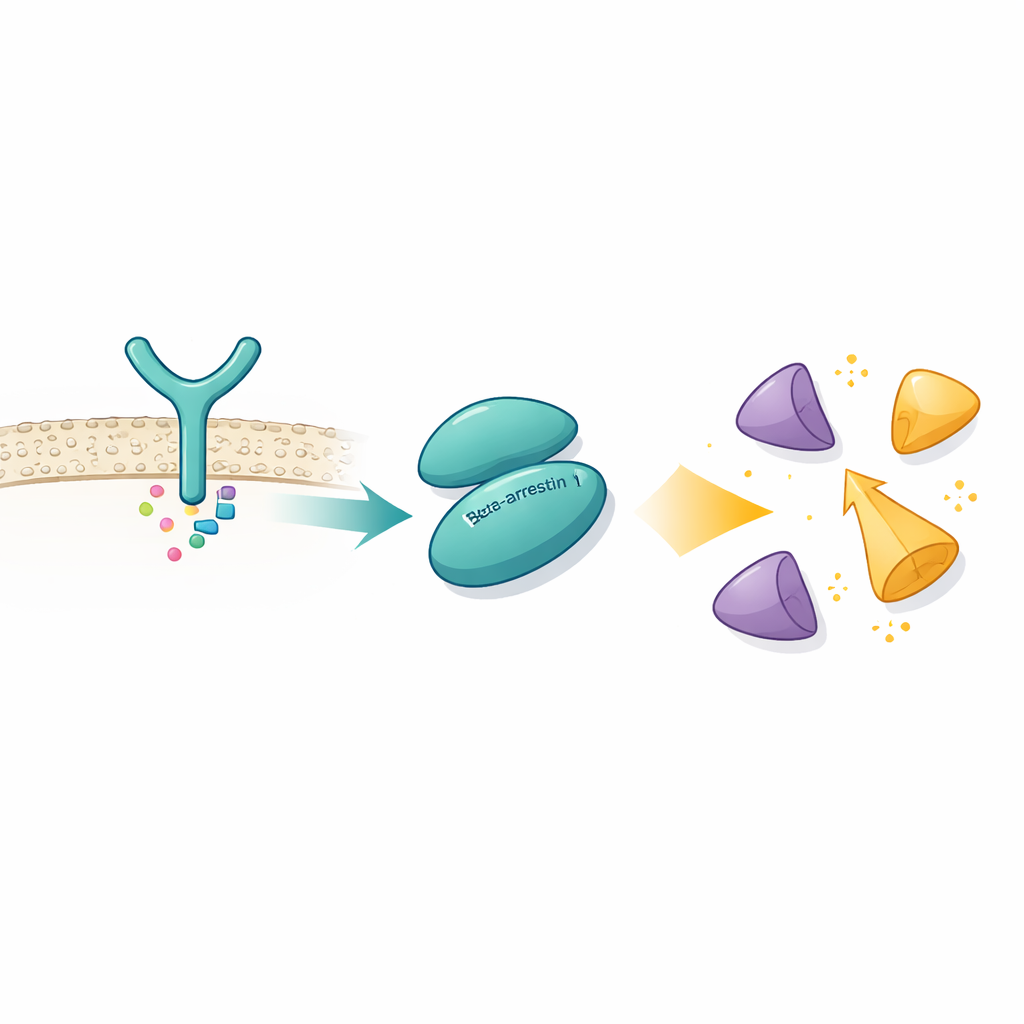
فك قفل إنزيم في حالة تثبيط ذاتي
يُحتفظ بـSrc عادة في شكل مثبّت ذاتيًا، أو معطّل ذاتيًا، حيث تتراص مجالاته SH3 وSH2 والمجال التحفيزي ضد بعضها وتُثبّتها قطعة ذيلية مغلقة. يمنع هذا التثبيت التنشيط العَرَضي الذي قد يضِر الخلية. من خلال حل بنية βarr1 المربوطة بشكل ثلاثي المجالات من Src، رأى الباحثون أنه عندما يلتحم SH3 بموقع الحد المركزي على βarr1، لا يستطيع بعد ذلك أن يمسك بالموصل الداخلي الذي يساعد في إبقاء Src مغلقًا. يصبح المجال التحفيزي أكثر حركة وتُرخى البنية العامة، بما يتوافق مع حالة نشطة. تُظهر التحاليل البايوكيميائية أن βarr1 يربط Src تفضيليًا عندما لا تكون ذيلته مفسفرة، أي في شكل أكثر مرونة يكشف مؤقتًا SH3. بمجرد أن يثبت SH3 على βarr1، يُفتح القفل الذي يبقي Src هادئًا، مما يسمح لـSrc بالتنفس الذاتي للفسفرة والتفعيل الكامل.
مركز مرن لتوجيه الإشارة
تكشف الدراسة أيضًا أن βarr1 نفسه ليس جامدًا. عندما يرتبط SH3، تتحرك شرائح وحلقات رئيسية داخل βarr1 بمقدار عدة أنغسترومات، خاصة حول الحد المركزي. قد تغير هذه الحركات الطفيفة مدى إحكام قبضة βarr1 على مستقبلات GPCR. تُظهر تجارب باستخدام βarr1 الموسوم بفلوورسنت أن فائض SH3 يمكن أن يضعف الطريقة التي يدخل بها βarr1 جزءًا من نفسه إلى نواة المستقبل، وهو تَرتيب يُعتقد أنه مهم لإيقاف إشارات بروتين G. في الخلايا الحية، يؤدي فرط تعبير Src إلى إطالة مدة ارتفاع رسول ثانٍ يدعى cAMP بعد تنشيط مستقبل بيتا-أدرينيرجي، مشيرًا إلى تأخر في فقد الحساسية. معًا، تشير هذه النتائج إلى أن مستويات Src المحلية العالية يمكن أن تميل بتجمعات GPCR–βarr1 بعيدًا عن وضع "الإيقاف" الكامل وتسمح لبروتينات G بمواصلة الإشارة لفترة أطول.
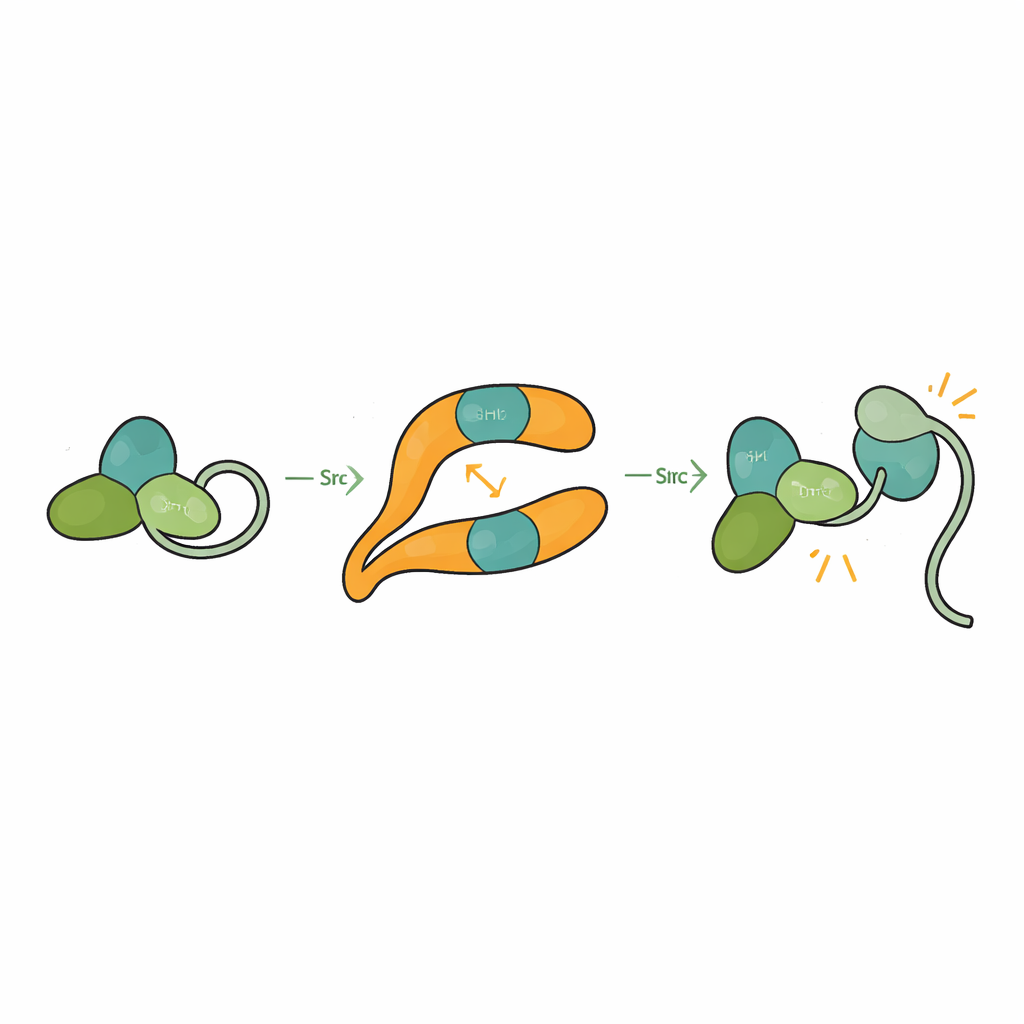
لماذا يهم هذا للصحة والعلاج
من خلال تصور كيفية إمساك βarr1 بـSrc في موقعين وسحبه من وضعه المثبّت ذاتيًا، تؤسس هذه الدراسة لβarr1 كمنظم نشط، لا مجرد هيكل داعم سلبي. تُظهر أن بروتين الموصل الواحد يمكنه جمع اتصالات متعددة نسبياً وضعيفة لتكوين سيطرة قوية وقابلة للضبط على إنزيم قوي. وبما أن Src غالبًا ما يكون مفرط التعبير أو سيئ التنظيم في السرطانات، فإن فهم مسار التفعيل هذا قد يلهم استراتيجيات تعطل انتقائيًا تواصل βarr1–Src دون إيقاف وظائف Src الأخرى. وبشكل أوسع، قد يكون التعرف ثنائي المواقع المكشوف هنا نموذجًا عامًا لكيفية تفاعل بيتا-أريستينات مع العديد من شركائها، مما يوفر زوايا جديدة لتصميم أدوية توجّه إشارات GPCR نحو مسارات مفيدة مع تجنّب المسارات الضارة.
الاستشهاد: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
الكلمات المفتاحية: بيتا-أريستين, كيناز Src, إشارة مستقبلات مقترنة بالبروتين G, الميكروسكوب الإلكتروني بالتبريد, إشارات خلوية