Clear Sky Science · ru
Механизм активации Src через SH3-домен Src, опосредованной бета-аррестином 1, раскрыт методом крио-электронной микроскопии
Как клетки превращают сигналы в действия
Наши клетки постоянно улавливают гормоны и нейротрансмиттеры через рецепторы на своей поверхности и вынуждены решать, когда реагировать, когда прекращать ответ и какие внутриклеточные пути включать. В этом исследовании рассматриваются два ключевых участника процесса принятия решений — бета-аррестин 1 и фермент Src — чтобы показать на атомном уровне, как один белок физически включает «включатель» другого. Понимание этой хореографии помогает объяснить, как работают повседневные сигнальные процессы, и может пролить свет на сбои при заболеваниях, таких как рак, где Src часто гиперактивен.
Регулировщик движения, который также является переключателем
Рецепторы, сопряженные с G-белками (GPCR), — это большая семья сенсоров на поверхности клетки, контролирующая процессы от зрения до частоты сердечных сокращений. Долгое время бета-аррестины считали главным образом «регулировщиками движения»: они прикрепляются к активированным GPCR, прекращают дальнейшую передачу сигнала и направляют рецепторы внутрь клетки. За последнее десятилетие, однако, бета-аррестины предстали как самостоятельные переносчики сигналов, способные связать GPCR с множеством ферментов внизу по цепочке. Одним из важнейших партнеров является Src, тирозинкиназа, способная стимулировать рост клеток, их перемещение и выживание. Тем не менее точный механизм, которым бета-аррестин 1 (β-arrestin 1, или βarr1) контактирует с Src и фактически его активирует, оставался загадкой, поскольку взаимодействие быстрое и относительно слабое.
Два рукопожатия на одном белке
Используя крио-электронную микроскопию, которая может визуализировать белковые комплексы почти с атомным разрешением, авторы зафиксировали βarr1 в связке с SH3-доменом Src — небольшим докинговым модулем, встречающимся во многих сигнальных белках. Они обнаружили, что βarr1 не опирается на единичную точку контакта. Вместо этого он предлагает два отдельных «рукопожатия» на разных участках своей структуры. Один сайт расположен в N-концевой области βarr1 и содержит короткий участок, богатый пролинами — аминокислотами, часто взаимодействующими с SH3-доменами. Второй сайт, в области, называемой центральным гребнем, использует другой набор аминокислот, чтобы занять ту же ароматическую поверхность SH3-домена. Биофизические измерения и эксперименты с обменом водород/дейтерий подтверждают, что обе области βarr1 защищаются при наличии SH3, даже без искусственных кросслинков, что показывает: эти двойные контакты происходят в реалистичных условиях.
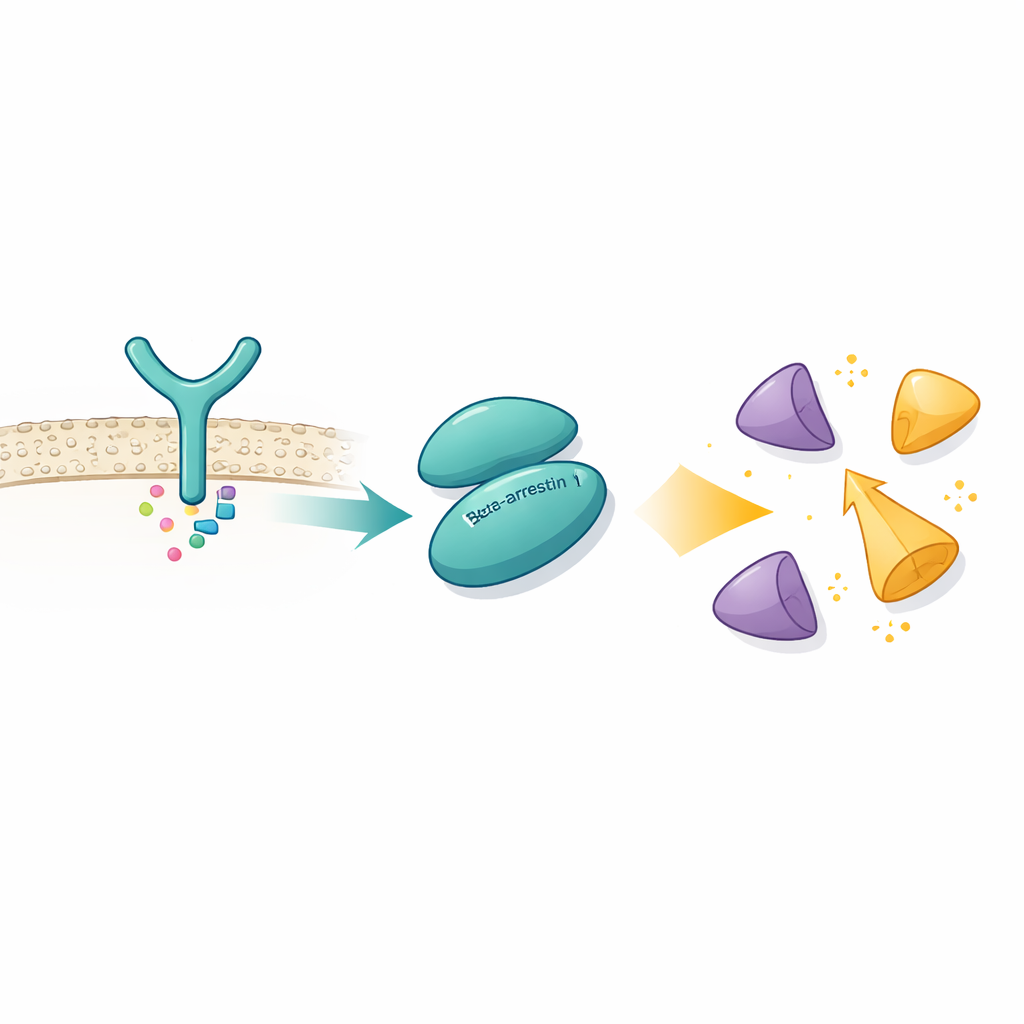
Разблокировка аутоингибированного фермента
Обычно Src удерживается в самозажатой, или аутоингибированной, форме, при которой его SH3-, SH2- и каталитические домены плотно упакованы друг с другом, а хвостовой сегмент фиксирует структуру в закрытом состоянии. Это предотвращает случайную активацию, которая могла бы повредить клетке. Решив структуру βarr1 в комплексе с трехдоменной формой Src, исследователи увидели, что когда SH3 взаимодействует с сайтом центрального гребня βarr1, он уже не может охватить внутреннюю петлю-связку, которая помогает удерживать Src в закрытом состоянии. Каталитический домен становится более подвижным, а общая конформация ослабляется, что согласуется с активным состоянием. Биохимические анализы показывают, что βarr1 предпочитает связываться с Src, когда его хвост не фосфорилирован — в более гибкой форме, которая временно открывает SH3. Как только SH3 захватывает βarr1, зажим, держащий Src в тихом состоянии, приподнимается, позволяя Src аутофосфорилироваться и полностью активироваться.
Гибкий узел для маршрутизации сигналов
Исследование также показывает, что сам βarr1 не является жестким. При связывании SH3 ключевые цепи и петли внутри βarr1 смещаются на несколько ангстрем, особенно вокруг центрального гребня. Эти тонкие движения могут менять силу сцепления βarr1 с GPCR. Эксперименты с флуоресцентно меченым βarr1 демонстрируют, что избыток SH3 может ослаблять вставление части βarr1 в ядро рецептора — конфигурацию, считающуюся важной для выключения G-белкового сигнала. В живых клетках переэкспрессия Src удлиняет рост уровня второго посредника cAMP после активации бета-адренергического рецептора, что указывает на замедленную десенситизацию. В совокупности эти данные предполагают, что высокий локальный уровень Src может смещать комплексы GPCR–βarr1 от полного «выключенного» состояния и позволять G-белкам дольше продолжать передачу сигнала.
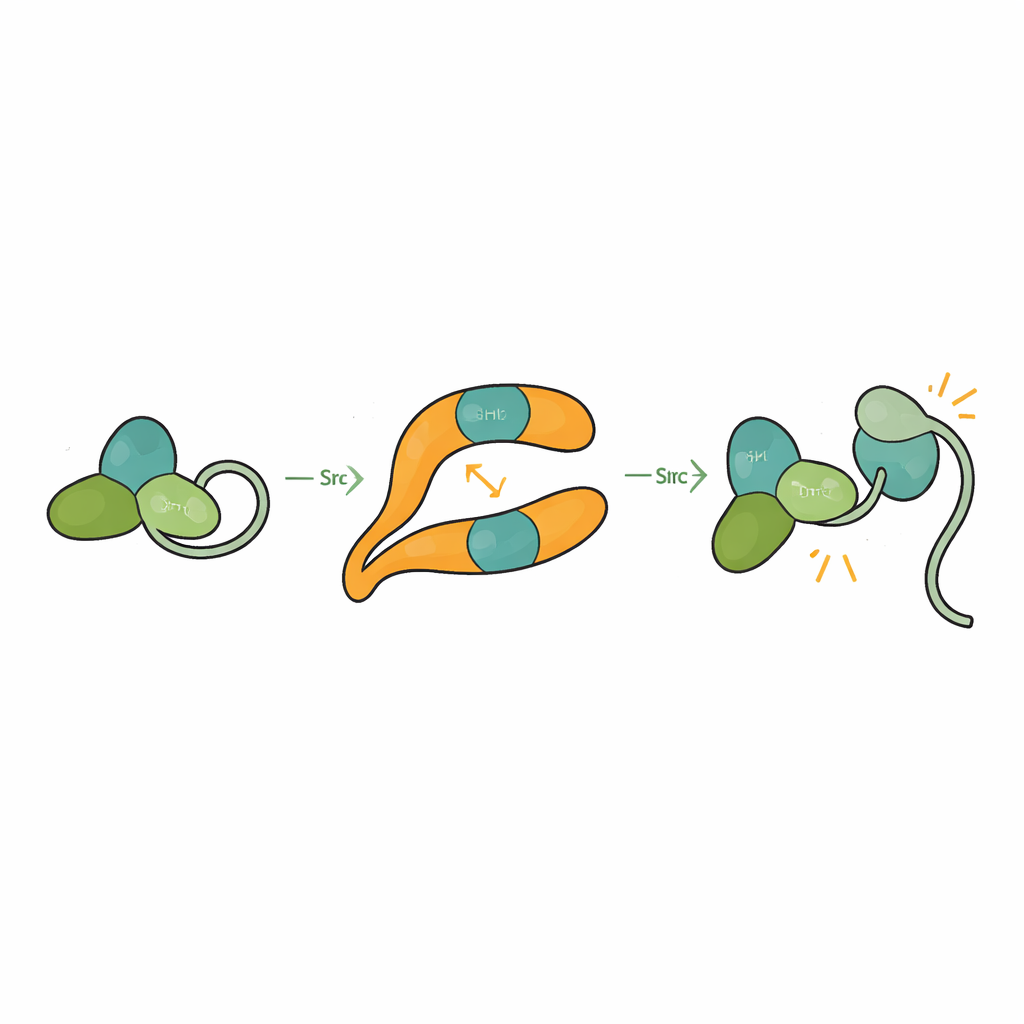
Почему это важно для здоровья и терапии
Непосредственно визуализируя, как βarr1 захватывает Src в двух местах и вытягивает его из самозажатого положения, эта работа устанавливает βarr1 как активного регулятора, а не просто пассивный каркас. Показано, что один адаптерный белок может объединять многочисленные, относительно слабые контакты в надежный и настраиваемый контроль над мощным ферментом. Поскольку Src часто сверхэкспрессирован или неправильно регулируется при раке, понимание этого пути активации может вдохновить стратегии, направленные на селективное разрывание коммуникации βarr1–Src без выключения других функций Src. В более широком смысле обнаруженное здесь распознавание по двум сайтам может быть общей схемой взаимодействия бета-аррестинов со многими их партнерами, предлагая новые подходы к дизайну препаратов, которые смещают сигналы GPCR в пользу полезных путей, избегая вредных.
Цитирование: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
Ключевые слова: бета-аррестин, киназа Src, сигналирование GPCR, крио-электронная микроскопия, клеточная сигнализация