Clear Sky Science · fr
Mécanisme de l’activation de Src médiée par la bêta-arrestine 1 via le domaine SH3 de Src révélé par cryo‑microscopie électronique
Comment les cellules transforment un signal en action
Nos cellules détectent en permanence hormones et neurotransmetteurs via des récepteurs à leur surface et doivent décider quand répondre, quand s’arrêter et quelles voies internes activer. Cette étude s’intéresse à deux acteurs clés de ce processus décisionnel — la bêta‑arrestine 1 et l’enzyme Src — pour révéler, en détail atomique, comment une protéine actionne physiquement l’interrupteur d’une autre. Comprendre cette chorégraphie aide à expliquer le fonctionnement des signaux usuels et peut éclairer ce qui déraille dans des maladies comme le cancer, où Src est souvent hyperactif.
Un agent de circulation qui fait aussi office d’interrupteur
Les récepteurs couplés aux protéines G (GPCR) constituent une vaste famille de senseurs membranaires contrôlant des processus allant de la vision au rythme cardiaque. Les bêta‑arrestines ont longtemps été vues principalement comme des agents de circulation cellulaires : elles se fixent sur les GPCR activés, stoppent la signalisation supplémentaire et dirigent les récepteurs vers l’intérieur de la cellule. Au cours de la dernière décennie, toutefois, les bêta‑arrestines sont apparues comme des vecteurs de signalisation à part entière, capables de relier les GPCR à de nombreuses enzymes en aval. L’un des partenaires les plus importants est Src, une tyrosine‑kinase pouvant stimuler la croissance, la migration et la survie cellulaires. Pourtant, la manière précise dont la bêta‑arrestine 1 (β‑arrestine 1, ou βarr1) communique avec Src — et l’active effectivement — est restée mystérieuse parce que l’interaction est fugace et relativement faible.
Deux poignées sur une même protéine
En utilisant la cryo‑microscopie électronique, capable de visualiser des assemblages protéiques à résolution quasi atomique, les auteurs ont capturé βarr1 liée au domaine SH3 de Src, un petit module d’amarrage présent dans de nombreuses protéines de signalisation. Ils ont découvert que βarr1 ne repose pas sur un seul point de contact. Elle offre au contraire deux poignées distinctes situées sur différentes parties de sa structure. Un site se trouve dans la région N‑terminal de βarr1 et contient un court segment riche en prolines — acides aminés qui interagissent souvent avec les domaines SH3. Le second site, dans une région appelée la crête centrale, utilise un mélange différent d’acides aminés pour se poser sur la même surface aromatique du domaine SH3. Des mesures biophysiques et des expériences d’échange hydrogène‑déutérium confirment que ces deux zones de βarr1 sont protégées en présence du SH3, même sans liaisons croisées artificielles, montrant que ces contacts doubles existent dans des conditions réalistes.
Déverrouiller une enzyme autoinhibée
Src est normalement maintenu dans une conformation auto‑verrouillée, ou autoinhibée, où ses domaines SH3, SH2 et catalytique s’emboîtent et où un segment de queue retient la structure fermée. Cela empêche une activation accidentelle potentiellement délétère pour la cellule. En résolvant la structure de βarr1 liée à une forme à trois domaines de Src, les chercheurs ont observé que lorsque SH3 engage le site de la crête centrale de βarr1, il ne peut plus agripper le linker interne qui contribue à maintenir Src fermé. Le domaine catalytique devient plus mobile et la conformation globale se relâche, compatible avec un état actif. Des essais biochimiques montrent que βarr1 se lie de préférence à Src lorsque sa queue n’est pas phosphorylée, forme plus flexible qui expose momentanément le SH3. Une fois que SH3 se fixe sur βarr1, le verrou maintenant Src est forcé d’ouvrir, permettant l’autophosphorylation de Src et son activation complète.
Un hub flexible pour le routage des signaux
L’étude révèle aussi que βarr1 elle‑même n’est pas rigide. Lorsque SH3 se lie, des brins et des boucles clés au sein de βarr1 se déplacent de plusieurs angströms, en particulier autour de la crête centrale. Ces mouvements subtils peuvent modifier la façon dont βarr1 agrippe les GPCR. Des expériences avec βarr1 marquée par fluorescence montrent qu’un excès de SH3 peut affaiblir l’insertion d’une portion de βarr1 dans le cœur du récepteur, configuration considérée importante pour couper la signalisation via les protéines G. In vivo, la surexpression de Src prolonge l’augmentation d’un second messager appelé AMPc après activation d’un récepteur bêta‑adrénergique, indiquant une désensibilisation retardée. Ensemble, ces résultats suggèrent que des niveaux locaux élevés de Src peuvent faire basculer les assemblages GPCR–βarr1 loin d’un mode « off » complet et permettre aux protéines G de continuer la signalisation plus longtemps.
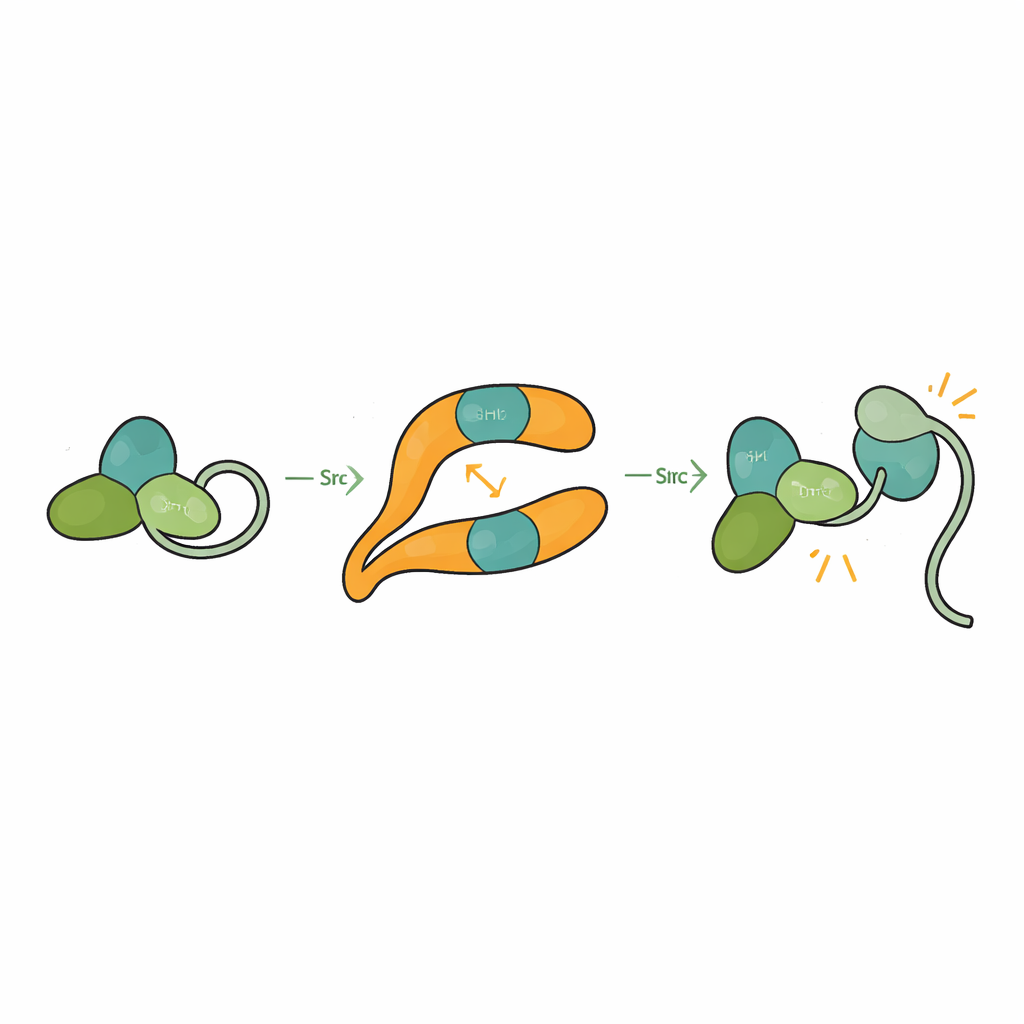
Pourquoi cela compte pour la santé et la thérapie
En visualisant directement comment βarr1 saisit Src en deux points et le tire hors de sa posture autoinhibée, ce travail établit βarr1 comme un régulateur actif, pas seulement comme un échafaudage passif. Il montre qu’un seul adaptateur peut combiner plusieurs contacts relativement faibles en un contrôle robuste et modulable d’une enzyme puissante. Étant donné que Src est fréquemment surexprimé ou mal régulé dans les cancers, comprendre cette voie d’activation pourrait inspirer des stratégies visant à perturber sélectivement la communication βarr1–Src sans éteindre d’autres fonctions de Src. Plus largement, la reconnaissance à deux sites mise en évidence ici pourrait constituer un schéma général expliquant comment les bêta‑arrestines interagissent avec nombre de leurs partenaires, offrant de nouvelles perspectives pour concevoir des médicaments qui orientent la signalisation GPCR vers des voies bénéfiques tout en évitant les effets indésirables.
Citation: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
Mots-clés: bêta-arrestine, kinase Src, signalisation GPCR, cryo‑microscopie électronique, signalisation cellulaire