Clear Sky Science · he
מנגנון ההפעלה של Src המתווכת על ידי בטא-ארסטין 1 דרך תחום SH3 של Src שנחשף בעזרת מיקרוסקופיה קריואלקטרונית
איך תאים ממירים אותות לפעולה
התאים שלנו חשים ללא הפסקה הורמונים ונוירוטרנסמיטורים דרך קולטן על פני הממברנה וחייבים להחליט מתי להגיב, מתי להפסיק ומתי להפעיל מסלולים פנימיים שונים. המחקר הזה בוחן שני שחקנים מרכזיים בתהליך קבלת ההחלטות — בטא-ארסטין 1 והאנזים Src — כדי להראות, בפרטי אטום, כיצד חלבון אחד מפעיל פיזית את "מפתח ההפעלה" של חלבון אחר. הבנת הכוריאוגרפיה הזו מסייעת להסביר כיצד אותות שוטפים פועלים ועלולה להאיר מה משתבש במצבים פתולוגיים כגון סרטן, שם Src לעתים קרובות פעיל ביתר.
שוטר תנועה שהוא גם מפסק
קולטני G protein–coupled (GPCR) הם משפחה עצומה של חיישנים ממברנליים ששולטים בתהליכים החל מן הראייה ועד קצב הלב. בטא-ארסטינים נתפסו במשך זמן רב בעיקר כשוטרי תנועה תאיים: הם נקשרים ל-GPCRs מופעלים, סוגרים המשך איתות ומנחים את הקולטן פנימה לתא. בעשור האחרון, לעומת זאת, התגלו בטא-ארסטינים גם כנושאי אותות בזכות עצמם, המסוגלים לקשר GPCRs לאנזימים רבים בהמשך. אחד השותפים החשובים ביותר הוא Src, טירוזין קינאז שיכול לקדם גדילה תאית, תנועה והישרדות. עם זאת, הדרך המדויקת שבה בטא-ארסטין 1 (β-arrestin 1, או βarr1) מתקשרת עם Src — וכיצד היא באמת מפעילה אותו — נותרה תעלומה כי האינטראקציה קצרה יחסית וחלשה.
שתי לוחיצות יד על חלבון אחד
באמצעות מיקרוסקופיה קריואלקטרונית, שמאפשרת להמחיש צברי חלבונים ברזולוציה כמעט אטומית, החוקרים תפסו את βarr1 קשור לתחום SH3 של Src, מודול דוקר קטן הנמצא בהרבה חלבוני איתות. הם גילו ש-βarr1 לא מסתמך על נקודת מגע יחידה. במקום זאת, הוא מציע שתי לחיצות יד נפרדות בחלקים שונים של המבנה שלו. אתר אחד יושב באזור ה-N-טרמינלי של βarr1 ומכיל רצף קצר עשיר בפרולינים — חומצות אמינו שבחלקן נוטות להיקשר לתחומי SH3. האתר השני, באזור הקרוי ה"גרם המרכזי" (central crest), משתמש בתערובת שונה של חומצות אמינו ונוחת על אותה משטח ארומטי של תחום ה-SH3. מדידות ביופיזיקליות וניסויי חילוף מימן–דיוטריום מאששים ששני האזורים של βarr1 הופכים מוגנים בנוכחות SH3, אפילו ללא קשירות מהונדסת, מה שמראה שהמגעים הכפולים האלה מתרחשים בתנאים מציאותיים.
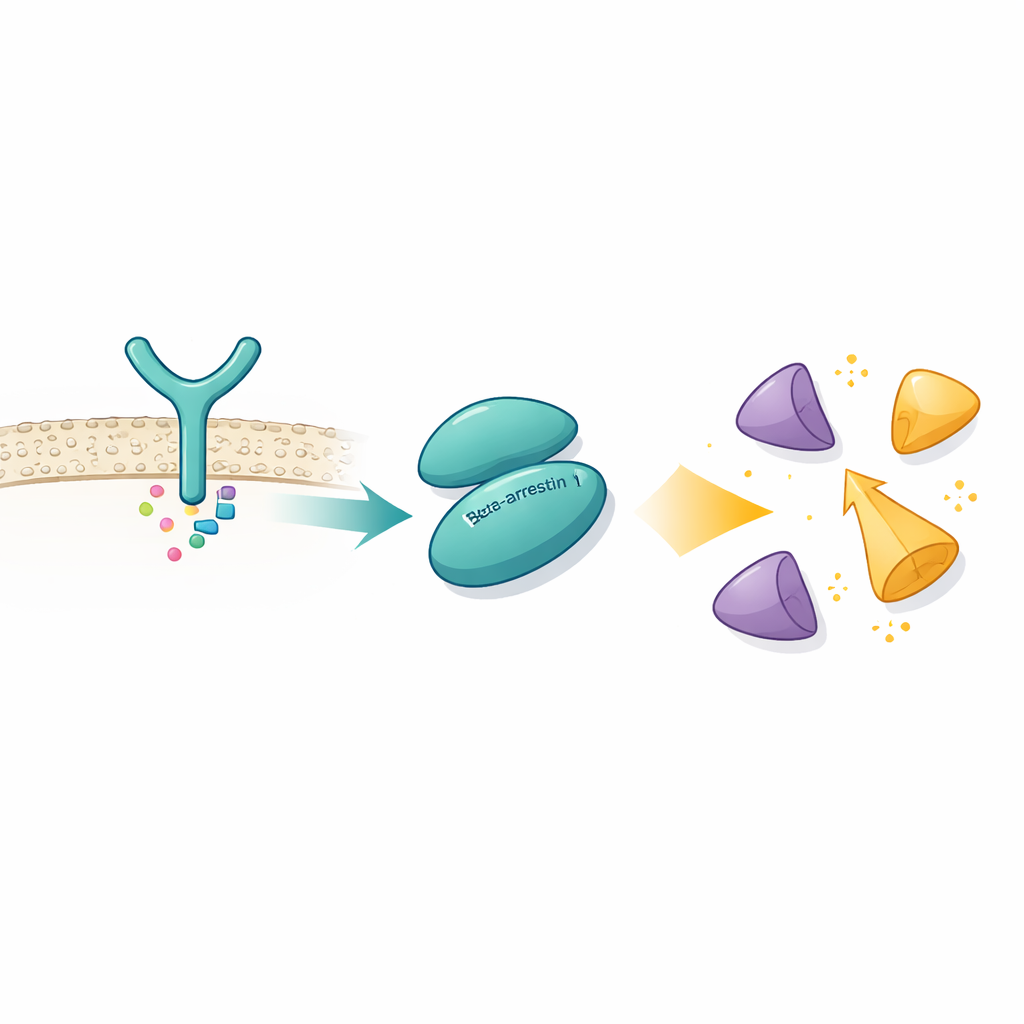
שחרור אנזים באוטואינהיבציה
במצב רגיל Src מוחזק במצב עצמי-נעול, או אוטואינהיביציה, שבו תחומי SH3, SH2 והדומיין הקטליטי נארזים זה בזה וקטע זנב קושר את המבנה לסגירה. זה מונע הפעלה מקרית שעלולה להזיק לתא. על ידי פתרון המבנה של βarr1 קשור לצורת Src בעלת שלושה דומיינים, החוקרים ראו שכאשר SH3 נקשר לאתר הגרם המרכזי של βarr1, הוא כבר אינו יכול לאחוז בקישור הפנימי (internal linker) שעוזר לשמור על Src סגור. תחום הקטליזה נעשה גמיש יותר והצורה הכללית נרפית, בהתאם למצב פעיל. מישורי מבחן ביוכימיים מראים ש-βarr1 מעדיף לקשור Src כאשר זנבו אינו מזורחן — צורה גמישה יותר שחושפת לרגע את SH3. ברגע ש-SH3 ננעל על βarr1, החיבור ששומר על שקט של Src נפתח, מה שמאפשר ל-Src לעבור אוטופוספורילציה ולהתמלא בפעילות.
צומת גמיש לניתוב אותות
המחקר גם מגלה כי βarr1 עצמו אינו קשיח. כאשר SH3 נקשר, סלילים ולולאות מרכזיים בתוך βarr1 זזים בכמה אנגסטרומים, במיוחד סביב הגרם המרכזי. התנועות העדינות האלה עשויות לשנות עד כמה חזק βarr1 אוחז ב-GPCRs. ניסויים עם βarr1 שסומן בפלואורופור מראים שעודף של SH3 יכול להחליש את הדרך שבה βarr1 מחדיר חלק מעצמו לגרעין הקולטן, קונפיגורציה הנחשבת חשובה לסגירת איתות ה-G protein. בתאים חיים, הבעה יתר של Src מאריכה את העלייה במסר השני cAMP לאחר הפעלת קולטן בטא-אדרנרגי, דבר שמצביע על דה-חישה מושהית. יחד, ממצאים אלה מציעים שרמות מקומיות גבוהות של Src יכולות להטות את מרבצי GPCR–βarr1 הרחק ממצב ה"כבוי" המלא ולאפשר ל-G proteins להמשיך לשדר למשך זמן ממושך יותר.
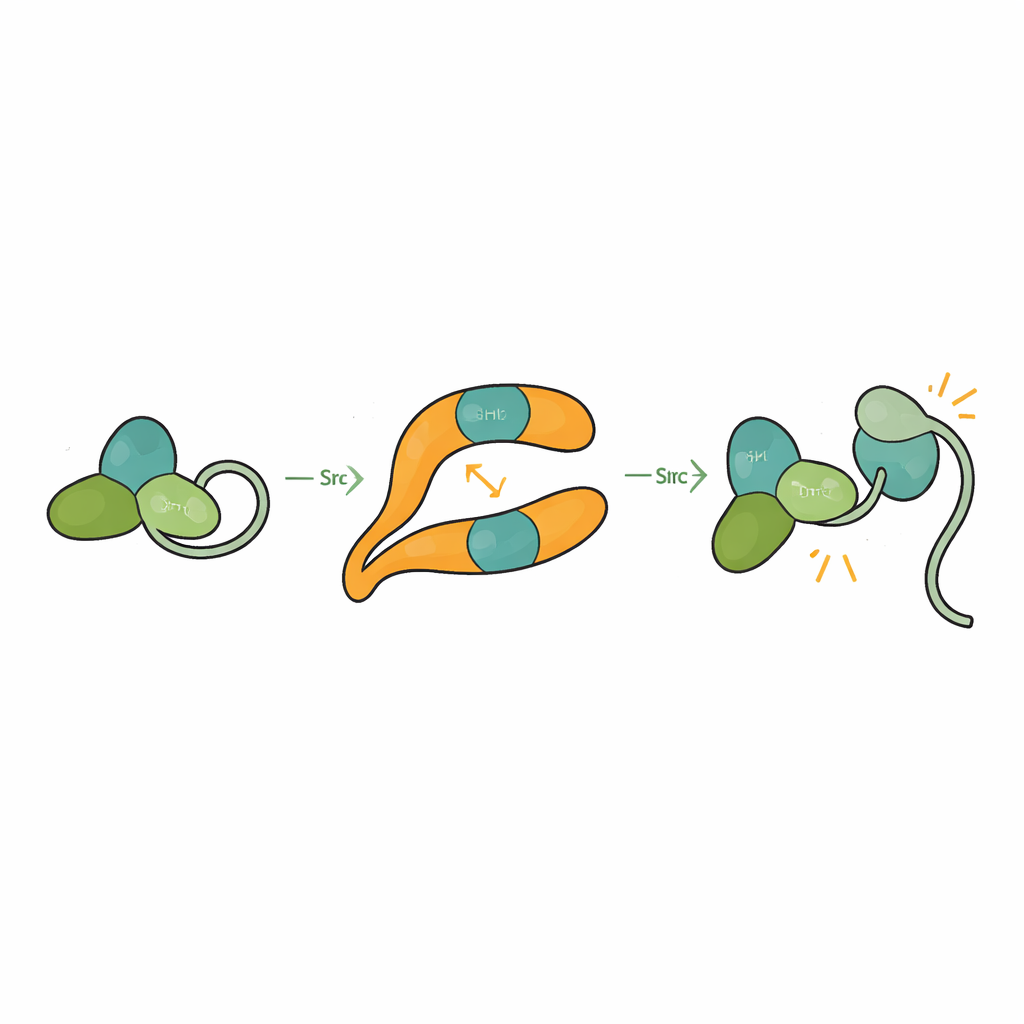
מדוע זה חשוב לבריאות ולטיפול
על ידי המחשה ישירה של איך βarr1 לוכד את Src בשני אתרים ומשוך אותו מתוך תנוחת האוטואינהיבציה שלו, עבודה זו מקימה את βarr1 כמווסת פעיל, לא רק כמתאם פסיבי. היא מראה שחלבון אדפטור יחיד יכול לשלב מספר מגעים יחסית חלשים לשליטה חזקה וניתנת לכוונון על אנזים עוצמתי. מאחר ש-Src לעיתים קרובות מובע יתר או מנוהל באופן לקוי בסרטן, הבנת מסלול ההפעלה הזה עשויה לעורר אסטרטגיות שיפגעו בסלקטיביות בתקשורת βarr1–Src מבלי לכבות פונקציות נוספות של Src. באופן רחב יותר, הזיהוי הכפול של אתרי ההכרה שנחשף כאן עשוי להיות מתווה כללי לאופן שבו בטא-ארסטינים מתקשרים עם רבים מהשותפים שלהם, ומציע זוויות חדשות לעיצוב תרופות המוטות אותות GPCR לכיוונים מועילים מבלי לעודד מסלולים מזיקים.
ציטוט: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
מילות מפתח: בטא-ארסטין, קינאזת Src, אותות GPCR, מיקרוסקופיה קריואלקטרונית, אותות תאיים