Clear Sky Science · es
Mecanismo de activación de Src mediada por beta-arrestina 1 a través del dominio SH3 de Src revelado por criomicroscopía electrónica
Cómo las células convierten señales en acción
Nuestras células detectan continuamente hormonas y neurotransmisores mediante receptores en su superficie y deben decidir cuándo responder, cuándo detenerse y qué vías internas activar. Este estudio examina a dos protagonistas clave en ese proceso de toma de decisiones—beta-arrestina 1 y la enzima Src—para revelar, en detalle atómico, cómo una proteína físicamente acciona el interruptor de otra. Comprender esta coreografía ayuda a explicar cómo funciona la señalización cotidiana y puede arrojar luz sobre lo que falla en enfermedades como el cáncer, donde Src suele estar sobreactivado.
Un agente de tráfico que también es un interruptor
Los receptores acoplados a proteína G (GPCR) son una enorme familia de sensores en la superficie celular que controlan procesos desde la visión hasta la frecuencia cardíaca. Durante mucho tiempo se consideró a las beta-arrestinas principalmente como agentes de tráfico celular: se adhieren a los GPCR activados, cierran la señalización adicional y guían a los receptores hacia el interior de la célula. Sin embargo, en la última década las beta-arrestinas han emergido como portadoras de señales por derecho propio, capaces de conectar los GPCR con numerosas enzimas posteriores. Uno de los socios más importantes es Src, una tirosina quinasas que puede impulsar el crecimiento, el movimiento y la supervivencia celular. Aun así, la manera precisa en que la beta-arrestina 1 (β-arrestina 1, o βarr1) se comunica con Src—y en realidad lo activa—ha permanecido como un misterio porque la interacción es fugaz y relativamente débil.
Dos apretones de manos sobre una proteína
Usando criomicroscopía electrónica, que puede visualizar ensamblajes proteicos a resolución casi atómica, los autores capturaron a βarr1 unido al dominio SH3 de Src, un pequeño módulo de acoplamiento presente en muchas proteínas de señalización. Descubrieron que βarr1 no depende de un único punto de contacto. En su lugar, ofrece dos apretones de manos separados en diferentes partes de su estructura. Un sitio se ubica en la región N-terminal de βarr1 y contiene un tramo corto rico en prolina—aminoácidos que suelen interactuar con dominios SH3. El segundo sitio, en una región denominada cresta central, usa una mezcla diferente de aminoácidos para posarse sobre la misma superficie aromática del dominio SH3. Mediciones biofísicas y experimentos de intercambio hidrógeno-deuterio confirman que ambas áreas de βarr1 quedan protegidas cuando SH3 está presente, incluso sin enlaces cruzados diseñados, lo que muestra que estos contactos duales ocurren en condiciones realistas.
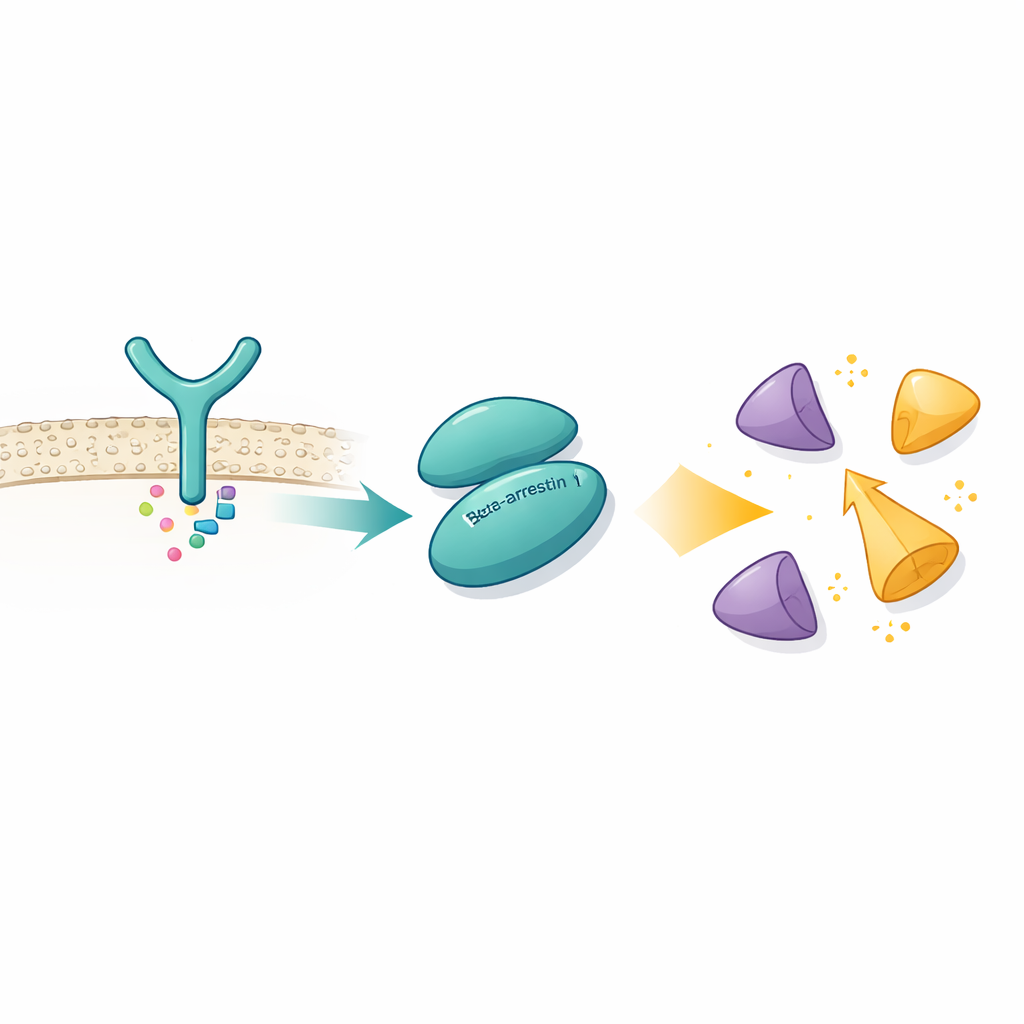
Desbloqueando una enzima autoinhibida
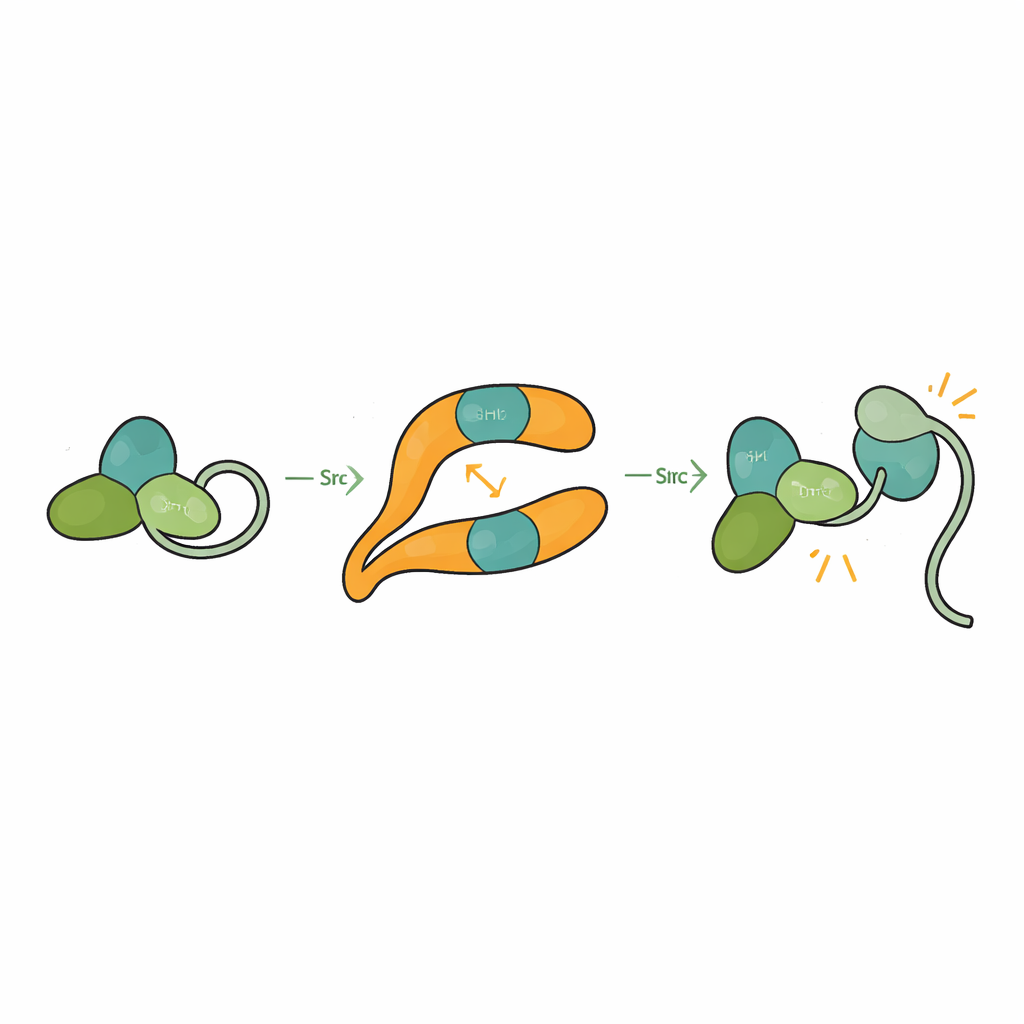
Src normalmente se mantiene en una conformación auto-bloqueada, o autoinhibida, en la que sus dominios SH3, SH2 y catalítico se empaquetan entre sí y un segmento de cola sujeta la estructura cerrada. Esto evita activaciones accidentales que podrían dañar la célula. Al resolver la estructura de βarr1 unido a una forma de Src con tres dominios, los investigadores observaron que cuando SH3 se une al sitio de la cresta central de βarr1, ya no puede sujetar el enlace interno que ayuda a mantener a Src cerrado. El dominio catalítico se vuelve más móvil y la forma global se afloja, coherente con un estado activo. Ensayos bioquímicos muestran que βarr1 se une preferentemente a Src cuando su cola no está fosforilada, una forma más flexible que expone momentáneamente a SH3. Una vez que SH3 se fija en βarr1, la abrazadera que mantiene a Src en silencio se abre, permitiendo que Src se autofosforile y se active por completo.
Un centro flexible para el enrutamiento de señales
El estudio también revela que la propia βarr1 no es rígida. Cuando SH3 se une, hebras y bucles clave dentro de βarr1 se desplazan varios angstroms, especialmente alrededor de la cresta central. Estos movimientos sutiles pueden alterar cuán firmemente βarr1 aferra a los GPCR. Experimentos con βarr1 etiquetada con fluoróforos muestran que un exceso de SH3 puede debilitar la forma en que βarr1 inserta parte de sí misma en el núcleo del receptor, una configuración que se considera importante para apagar la señalización por proteína G. En células vivas, la sobreexpresión de Src prolonga el aumento de un segundo mensajero llamado AMPc tras la activación de un receptor beta-adrenérgico, lo que indica una desensibilización retardada. En conjunto, estos hallazgos sugieren que niveles locales altos de Src pueden inclinar los ensamblajes GPCR–βarr1 lejos del modo completamente “apagado” y permitir que las proteínas G sigan señalando durante más tiempo.
Por qué esto importa para la salud y la terapia
Al visualizar directamente cómo βarr1 atrapa a Src en dos sitios y lo extrae de su postura autoinhibida, este trabajo establece a βarr1 como un regulador activo, no solo como un andamiaje pasivo. Muestra que una única proteína adaptadora puede combinar múltiples contactos relativamente débiles en un control robusto y ajustable sobre una enzima potente. Dado que Src a menudo está sobreexpresado o mal regulado en cánceres, comprender esta vía de activación podría inspirar estrategias que interrumpan selectivamente la comunicación βarr1–Src sin apagar otras funciones de Src. Más ampliamente, el reconocimiento de doble sitio descubierto aquí puede ser un patrón general de cómo las beta-arrestinas se relacionan con muchos de sus socios, ofreciendo nuevas vías para diseñar fármacos que sesguen la señalización de los GPCR hacia rutas beneficiosas evitando las perjudiciales.
Cita: Pakharukova, N., Thomas, B.N., Bansia, H. et al. Mechanism of beta-arrestin 1 mediated Src activation via Src SH3 domain revealed by cryo-electron microscopy. Nat Commun 17, 2973 (2026). https://doi.org/10.1038/s41467-026-69884-1
Palabras clave: beta-arrestina, cinasa Src, señalización GPCR, criomicroscopía electrónica, señalización celular